В данной статье приводится попытка реализации синтеза ароматического соединения (пиридина) из производных бензола и циклических алканов на основе теоретического разъяснения законов и последних исследований в области органической химии.
Ключевые слова: пиридин, алканы, циано-группы.
Пиридин впервые был выделен T. Андерсеном в 1849 из костяного масла; структура пиридина установлена Дж. Дьюаром и P. Кернером в 1869. Применяют данное вещество в синтезе красителей, лекарственных веществ, инсектицидов, в аналитической химии, как растворитель многих органических и некоторых неорганических веществ, для денатурирования спирта [1]. Также пиридин представляет интерес для фармацевтики так как входит в состав некоторых производных лекарственных препаратов (на пример акридин) для производства этакридин лактат.
Химические свойства пиридина определяются наличием ароматической системы и атома азота с неподеленной электронной парой. Пиридин проявляет свойства, характерные для третичных аминов: образует N-оксиды, соли N-алкилпиридиния, способен выступать в качестве сигма-донорного лиганда. Так же пиридин обладает явными ароматическими свойствами, но отличие от бензола, пиридин способен вступать в реакции нуклеофильного замещения, поскольку атом азота оттягивает на себя электронную плотность из ароматической системы, и орто-пара-положения по отношению к атому азота обеднены электронами. Так, пиридин может реагировать с амидом натрия (рис. 1), образуя смесь орто- и пара-аминопиридинов (реакция Чичибабина) [2]:
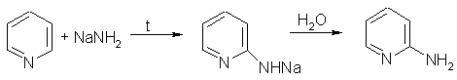
Рис. 1. Реакция Чичибабина
Исходя, из выше перечисленного можно сделать важное умозаключение, если пиридин обладает явным сходством по строению и химическими свойствами с бензолом, то и методы получения данных веществ вероятнее всего схожи.
Основным методом получения пиридина в промышленности — это выделение его из каменноугольной смолы в лабораторных условиях пиридин получают циклизацией из двух молекул ацетилена и одной молекулы циановодорода (рис. 2) (реакция Беннеманна) [2].
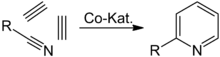
Рис. 2. Реакция Беннеманна
Реакция Беннеманна достаточно эффективна и имеет высокий показатель выхода продукта при повышенной температуре >600 0С. Но имеет и недостатке, во первых алкены в природе встречаются значительно реже алканов, во вторых использованный в синтезе катализатор кабольтонец дорог и сложен в производстве. Поэтому в данной работе предлагается использовать алканы с более дешевым катализатором как способ получения пиридина. Для решения поставленной задачи следует рассмотреть методы получения бензола и изучить химические свойства алканов.
Классическими способами получения бензолам являются: циклизация гексана, дегидрирование циклогексана, реакция Зелинского (из 3-х молекул ацителена) [3]. Нас интересуют первые два метода, поскольку в них содержатся ключевые реагенты алканы.
Рассмотрим реакции по подробней:
1) циклизация гексана:
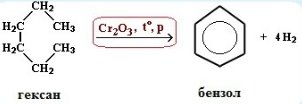
2) дегидрирование циклогексана:
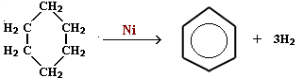
Как видно из данных методик их сходство очевидно, а последний можно даже назвать промежуточным соединением, однако стоит заменить в гексане одну мета-группу (CH3 -) на циано-группу (CN) и синтез бензол превращается в синтез пиридина.
Для дальнейшего разъяснения рассмотрим химические свойства алканов. В данном источнике [4] сказано, что алканы относятся к наиболее инертным в химическом отношении веществам, но главное алканы не проявляют склонности к гетероциклическому разрыву; эти соединения весьма устойчивы к действию ионным реагентов. В то же время неполярные связи алканов способны расщепляется гомолитически при атаке активными свободными радикалами. К таким процессам относят реакции замещения атомов водорода, крекинг, окисление. Здесь наибольший интерес представляют реакции замещения поскольку они более наглядны и хорошо изучены, рассмотрим нитрирование как одно из них.
Алканы нитрируются азотной кислотой как в паровой фазе при температуре 400–500 0С, так и в жидкой. Оба процесса протекают по радикальному механизму, где активной частицей служит нитро — радикал NO2· [4] данная реакция называется реакцией Коновалова. Процесс осуществляется при более низкой температуре (110–140 0С) с использованием разбавленной (10–20 % — й) кислоты. Но если замещение здесь идет на нитро-радикал, то что нам не дает оснований провести тот же процесс только с синильной кислотой, только здесь замещение возможно будет проходить по циано-радикалу CN· поскольку и NO2 — и CN — обладают отрицательным индуктивным эффектом.
Исходя из выше перечисленного можно смело утверждать, что синтез из алканов и производных бензола возможен, однако следует учитывать если реакция замещения идет по водороды данного алкана и циано-группе, то алкан должен состоять из пяти атомов углерода, а не шесть как у бензола, следовательно механизм данного синтеза будет иметь следующий вид:
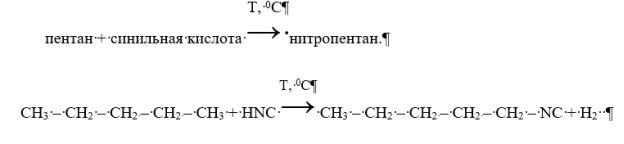
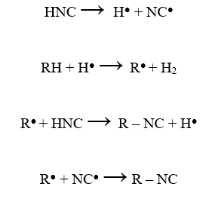
Механизм реакции:
Примечание: R — обозначим как пентан (CH3 — CH2 — CH2 — CH2 — CH3)
циклизация нитропентана с использованием катализатора дихромата калия:
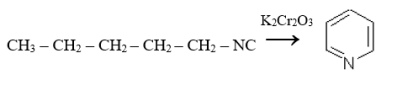
Выводы:
В данной работе мы рассмотрели наиболее оптимальный синтез пиридина, который по всем законам химического взаимодействия более экономичен и менее энергозатратен, конечно, в данной работе не был представлен расчет и проведен эксперимент для полного подтверждения истинности, поэтому в дальнейшем к работе будет представлен термодинамический расчет и результаты проведенного эксперимента.
Литература:
- Карапетьянц М. Х. Дракин С. И. Общая и неорганическая химия. — М.: Химия, 1994.
2. Органический синтез: лабораторный практикум / Н. Н. Быкова, А. П. Кузьмин. — Тамбов: Изд-во Тамб. гос. техн. ун-та, 2007. — 80 с
3. ГОСТ 13647–78. Реактивы. Пиридин. Технические условия.
- Органическая химия: Учеб. Для вузов: В 2 кн./ В. Л. Белобородов, С. Э. ЗуО-64 рабян, А. П. Лузин, Н. А. Тюкавкина; Под ред. Н. А. Тюкавкиной.−2-е изд., стереотип.− М.: Дрофа, 2003.− Кн. 1: Основной курс.−640 с.

