Устойчивость к противомикробным препаратам является глобальной проблемой в борьбе с инфекционными заболеваниями. Ежегодно во всем мире происходит около 700 000 смертей из-за инфекций, устойчивых к антибиотикам. Основываясь на сценариях роста лекарственной устойчивости к основным патогенам учёные подсчитали, что, если не будут приняты меры по борьбе с антибиотикорезистентностью, смертность от таких инфекций к 2050 году может увеличиться до 10 миллионов жизней в год, что соответствует смерти 1 человека каждые 3 секунды. Это приведет к тяжелым последствиям для мировой экономики и значительно понизит уровень жизни населения [1]. На данный момент ведется активный поиск веществ, способных оказывать бактериостатичный и бактерицидный эффект на мультирезистентные штаммы микроорганизмов. По данным многочисленных исследований подобными свойствами обладает усниновая кислота (УК). Она является вторичным метаболитом лишайников и продуцируется в родах Cladonia, Usnea, Lecanora, Ramalina и других. Усниновая кислота обладает высокой биологической активностью, в том числе бактерицидной [2]. Это позволяет в перспективе использовать ее в качестве альтернативы традиционным антибиотикам. Особенно важной является ее активность в отношении возбудителя туберкулёза, так как ситуация с ним становится особенно тревожной: в 105 странах циркулируют возбудители, устойчивые сразу к нескольким антибиотикам, а по данным ВОЗ, такие резистентные штаммы как Mycobacterium tuberculosis в 2014 году были найдены у 480 000 человек [3]. Так как все больше обострилась проблема отсутствия адекватного лечения инфекций, вызванных мультирезистентными штаммами бактерий, выделение и исследования усниновой кислоты проводятся все чаще с целью изучения возможности ее использования в качестве лекарственного средства.
Усниновая кислота является одним из наиболее важных и широко изученных метаболитов лишайников. Её фармакологический потенциал хорошо изучен и задокументирован. Она обладает широким спектром биологической активности, в том числе антибактериальной и цитотоксической, антипролиферативной, противовирусной, противомикробной, противопротозойной, противогрибковой, противопаразитарной, жаропонижающей, ранозаживляющей, анестезирующей, противовоспалительной и противоопухолевые активностью в различных типах клеток. УК обычно встречается во многих видах лишайников в значительно больших количествах, вплоть до 8 % от сухой массы сырья. При извлечении из лишайника усниновая кислота имеет желтый цвет и кристаллическую структуру. В соответствие с общепринятой номенклатурой усниновую кислоту можно назвать 2,6-диацетил-7,9-дигидрокси-8,9-диметил-дибензофуран-1,3(2H,9bH)-дион. Она существует в виде двух энантиомеров: (+) D-усниновая кислота и (-) L-усниновая кислота, что указывает соответственно на проекцию R и S конфигурации угловой метильной группы в положении 9b (Рисунок 1). Было установлено, что энантиомеры проявляют различную биологическую активность [4].
Усниновая кислота обладает высокой липофильностью как в нейтральной, так и в анионной формах из-за ее β-трикетоновых групп, поглощающих отрицательный заряд аниона за счет резонансной стабилизации. Эта липофильность позволяет усниновой кислоте вести себя как мембранный разобщитель подобно 2,4-динитрофенолу. Согласно хемоосмотической теории, такие молекулы легко диффундируют через биологические мембраны в заряженной и нейтральной формах, что приводит к нарушению или разобщению ионных градиентов. Эта разобщающая активность усниновой кислоты была продемонстрирована in vitro в нескольких исследованиях и считается, что она играет важную роль в гепатотоксичности усниновой кислоты. Однако, УК оказывает такое же разобщающее действие на мембраны бактериальных клеток, это составляет основу её антимикробной активности [5].
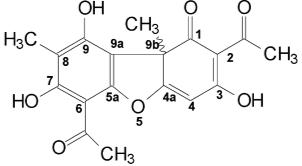
Рис. 1. Структурная формула усниновой кислоты
Усниновую кислоту можно химически синтезировать из метилфлороацетофенона путем окислительной дегидроконденсации с последующим гидролизом в серной кислоте [6]. Из трех гидроксильных групп, присутствующих в молекуле усниновой кислоты, енольный гидроксил в положении 3 (Рисунок 1) имеет наиболее сильный кислотный характер (рКа 4.4) за счет индукционного действия кетогруппы, тогда как гидроксильные группы в положениях 9 и 7 менее кислые, значения рКа 8,8 и 10,7 соответственно [7]. Тем не менее более рациональным методом получения усниновой кислоты является экстракция из лишайников, продуцирующих её в процессе роста.
Классическими методами выделения биологически активных соединений из растительного сырья являются экстракционные с применением органических растворителей. К ним относятся мацерация, перколяция, реперколяция, а также экстракция с использованием аппарата Сокслета. Для выделения лишайниковых кислот используют различные органические растворители: бензол, ацетон, гексан, этанол, петролейный эфир, хлороформ или их смеси для увеличения выхода целевого продукта. Достоинством этих способов является простота исполнения и недорогое оборудование. К недостаткам можно отнести продолжительность процесса экстракции, трудоемкость, а также возможная высокая токсичность и летучесть применяемых органических растворителей. Тем не менее, традиционные методы экстракции остаются наиболее актуальными и востребованными во многих исследованиях на сегодняшний день.
Для данного исследования был выбран метод экстракции в аппарате Сокслета. Он заключается в непрерывной подаче чистого растворителя на сырье, при этом осуществляется циклический слив экстракта. Аппарат Сокслета состоит из колбы, насадки НЭТ и обратного холодильника. В колбу наливают растворитель, в насадку помещают измельчённое сырьё, завернутое в фильтровальную бумагу, сверху устанавливают обратный холодильник для конденсации растворителя. На основании литературных данных о различной растворимости усниновой кислоты для данного исследования в качестве экстрагента был выбран хлороформ (трихлорметан, CHCl3) и ацетон (C3H6O) производителя реактивов ЭКОС-1. При использовании аппарата Сокслета необходимо предварительно притирать шлифы с абразивом для предотвращения утечки растворителя. Кроме того, также важно подобрать смазку для герметизации шлифов с учетом растворяющей способности экстрагента. В данном исследовании использовалась смазка на силиконовой основе. В качестве сырья для выделения усниновой кислоты была использована смесь лишайников рода Usneasp ., преимущественно UsneaBarbata , собранная в Алтайском крае. Талломы лишайника предварительно измельчались до размеров 0,5–1 см в соответствии с данными об оптимизации методики выделения УК, описанной в диссертации Лузиной О. А. [8]. Экстракция проводилась в течение 3 часов при температуре кипения растворителя. Один цикл от начала конденсации до слива растворителя занимал в среднем 15 минут. На 10г измельченного лишайникового сырья использовалось 250 мл растворителя, потери которого в процессе экстракции составили 30 и 50 мл для хлороформа и ацетона соответственно. Для нагрева реакционной смеси использовался колбонагреватель (ЭКРОС ES-4100, 500мл). Полученные экстракты упаривались до объема 40 мл на ротационном испарителе IKA RV10 control.
Выделение чистой усниновой кислоты проводилось методом замены растворителя. Упаренные экстракты разбавлялись этиловым спиртом в соотношении 1:3, выпавшие кристаллы были отделены на воронке Бюхнера, промыты этиловым спиртом и высушены на воздухе. Вес получившегося осадка составил 0,201г и 0,182г для хлороформного и ацетонового экстракта соответственно. Таким образом без учета примесей выход УК от сухого сырья составил 2,01 % и 1,82 % соответственно. В сравнении с другими исследованиями подобный выход можно считать существенным для традиционного метода экстракции.
Идентификация усниновой кислоты проводилась с помощью Фурье ИК спектрометра Tensor 37, УФ-видимого спектрометра UNICO и дифференциального сканирующего калориметра DSC Phoenix F201. ИК спектры кристаллов, полученных из хлороформного и ацетонового экстрактов практически идентичны (Рисунок 2), и совпадают с представленными в литературе данными.
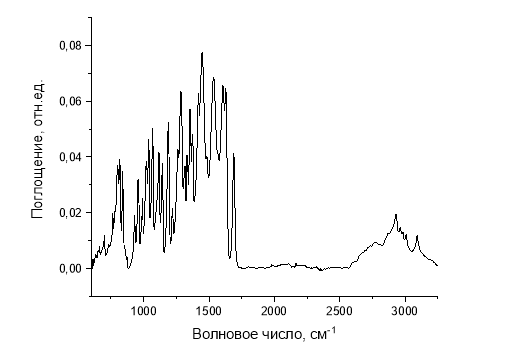
Рис. 2. ИК спектр кристаллов усниновой кислоты
Также были исследованы термические свойства усниновой кислоты. Полученные ДСК кривые кристаллов, выделенных из ацетонового и хлороформного экстрактов представлены на Рисунке 3. Температура плавления стандарта УК по литературным данным составляет 204 °С. Температура плавления полученных кристаллов составила 189 °С и 195 °С для кристаллов УК из хлороформного и ацетонового экстрактов соответственно. Следовательно, в полученных кристаллах имеются примеси, при чём в УК выделенной из хлороформного экстракта они присутствуют в большем количестве.

Рис. 3. ДСК кристаллов усниновой кислоты
Кроме того, экстракты УК были исследованы на УФ-видимом спектрометре UNICO. Полученные УФ спектры ацетонового и хлороформного экстрактов представлены на Рисунке 4. Спектры были сняты с разбавленных в 32 раза экстрактов с использованием кварцевых кювет толщиной в 1мм. Согласно литературным данным максимум поглощения стандарта усниновой кислоты в хлороформе имеет максимум при длине волны 285±2 нм, а в ацетоне 230±2 нм. Следовательно, полученные УФ спектры подтверждают наличие усниновой кислоты в экстрактах в высокой концентрации.

Рис. 4. УФ спектры ацетонового и хлороформного экстрактов
Таким образом экстракция и идентификация усниновой кислоты из лишайникового сырья для дальнейшего изучения её биологически активных свойств может быть осуществлена по методике, описанной в данном исследовании. При этом в качестве растворителя лучше показал себя хлороформ, так как он более полно экстрагировал усниновую кислоту из лишайника. Выход без учета примесей составил 2,01 % от сухой массы талломов. Усниновая кислота является перспективным соединением для изучения и применения в медицине, фармакологии и косметологии в ближайшем будущем.
Литература:
- Amr-review.org
- Соколов Д. Н., Лузина О. А., Салахутдинов Н. Ф. Усниновая кислота: получение, строение, свойства и химические превращения, Успехи химии/Uspekhi Khimii. 2012. Т.81. № 8. С.747–768
- Global tuberculosis report 2016
- A. Galanty, P. Paśko, I. Podolak, Enantioselective activity of usnic acid: a comprehensive review and future perspectives. Phytochemistry Reviews . 18 (2019), pp. 527–548.
- Araújo AA, de Melo MG, Rabelo TK, Nunes PS, Santos SL, Serafini MR, Santos MR, Quintans-Júnior LJ, Gelain DP. Review of the biological properties and toxicity of usnic acid. Nat Prod Res. 2015;29(23):2167–80.
- Barton DHR, Deflorin AM, Edwards OE. The synthesis of usnic acid. J Chem Soc1956; 1956:530–534.
- Ingólfsdóttir K. Usnic acid. Phytochemistry. 2002 Dec;61(7):729–36.
- Лузина О. А. Синтез биологически активных соединений на основе усниновой кислоты: диссертация на соискание учёной степени доктора химических наук: 02.00.03.- Новосибирский институт органической химии, г. Новосибирск, 2016–323с.

