Методика количественного определения суммы аминокислот в листе каштана конского обыкновенного
Авторы: Постоюк Наталья Александровна, Маркарян Артем Александрович, Даргаева Тамара Дарижаповна, Сокольская Татьяна Александровна
Рубрика: 11. Прочие отрасли медицины и здравоохранения
Опубликовано в
международная научная конференция «Новые задачи современной медицины» (Пермь, январь 2012)
Статья просмотрена: 1458 раз
Библиографическое описание:
Постоюк, Н. А. Методика количественного определения суммы аминокислот в листе каштана конского обыкновенного / Н. А. Постоюк, А. А. Маркарян, Т. Д. Даргаева, Т. А. Сокольская. — Текст : непосредственный // Новые задачи современной медицины : материалы I Междунар. науч. конф. (г. Пермь, январь 2012 г.). — Пермь : Меркурий, 2012. — С. 139-141. — URL: https://moluch.ru/conf/med/archive/51/1503/ (дата обращения: 28.04.2024).
Введение
Основными источниками лекарственного сырья в России являются промышленные заготовки от дикорастущих и возделываемых растений, при этом значительную долю составляют закупки по импорту. Перспективным направлением увеличения заготовок отечественного сырья является расширение его сырьевой базы [2,4].
За последнее время уделялось значительное внимание изучению аминокислотного состава в лекарственном растительном сырье. Аминокислоты – органические кислоты, имеющие в своей структуре аминогруппу в α- или других положениях. Аминокислоты являются структурными компонентами белков и составной частью ферментов, витаминов и других, важных для организма органических соединений. Растения синтезируют все аминокислоты, в отличие от организма животного и человека, неспособного синтезировать некоторые из них (незаменимые аминокислоты). Дефицит незаменимых аминокислот организм человека восполняет с растительной пищей. Аминокислоты необходимы для полноценной работы головного мозга, являясь предшественниками нейромедиаторов [1,3,5].
Перспективным источником создания лекарственных препаратов на основе лекарственного сырья является каштан конский обыкновенный.
Материалы и методы
В качестве объекта исследования использовали образцы листа каштана конского обыкновенного, собранного в парковой зоне города Москвы осенью 2010 г. Для определения суммы аминокислот в листьях была использована методика, основанная на реакции взаимодействия аминокислот с раствором нингидрина и последующем спектрофотометрировании полученного окрашенного комплекса при длине волны около 570 нм. В ходе эксперимента нами была уточнена длина волны максимума поглощения окрашенного комплекса с нингидрином глютаминовой кислоты и водного извлечения из листьев каштана.
Брали 5,0000 г (точная навеска) растительного сырья, измельченного до размера частиц, проходящих сквозь сито с диаметром отверстий 2 мм, помещали в колбу вместимостью 100 мл, прибавляли 50 мл воды дистиллированной и нагревали с обратным холодильником на кипящей водяной бане в течение часа. Охлаждали, извлечение фильтровали через обеззоленный фильтр в мерную колбу вместимостью 100 мл. Объем доводили до метки водой, перемешивали (исследуемый раствор).
Около 0,0500 г (точная навеска) кислоты глютаминовой помещали в мерную колбу вместимостью 100 мл, растворяли в 20-30 мл воды и доводили раствор водой до метки (РСО).
0,5 мл исследуемого раствора помещали в мерную колбу вместимостью 50 мл, прибавляли 1 мл 0,25% раствора натрия карбоната, 2 мл спиртового раствора нингидрина и нагревали 10 минут на кипящей водяной бане. После охлаждения раствор доводили водой до метки. Параллельно в мерную колбу вместимостью 50 мл помещали 2 мл раствора РСО кислоты глютаминовой. Оптическую плотность полученных растворов измеряли на спектрофотометре при длине волны 568 нм в кювете с толщиной слоя жидкости 10 мм относительно воды. Содержание суммы аминокислот в сырье в % Х, в пересчёте на кислоту глютаминовую. Рассчитывали по формуле:
Х = D* ∙ М ∙ 50 ∙ 2 ∙ 50 ∙ 100, где
D ∙ m ∙ 0,5 ∙ 100 ∙ 50 ∙ (100 - W)
D* – оптическая плотность испытуемого раствора, в нм;
D – оптическая плотность РСО глютаминовой кислоты, в нм;
М – масса РСО глютаминовой кислоты, в г;
m – масса сырья, в г;
W – потеря массы при высушивании сырья, в %.
Результаты и обсуждения
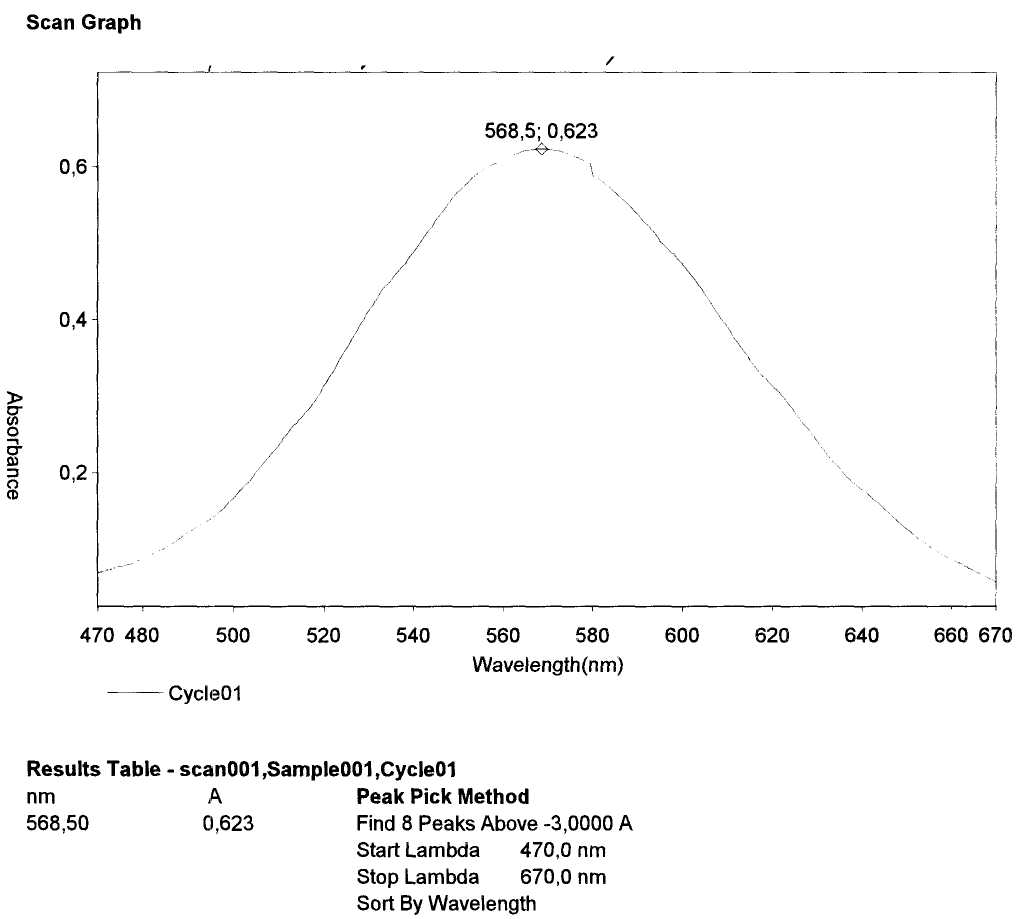
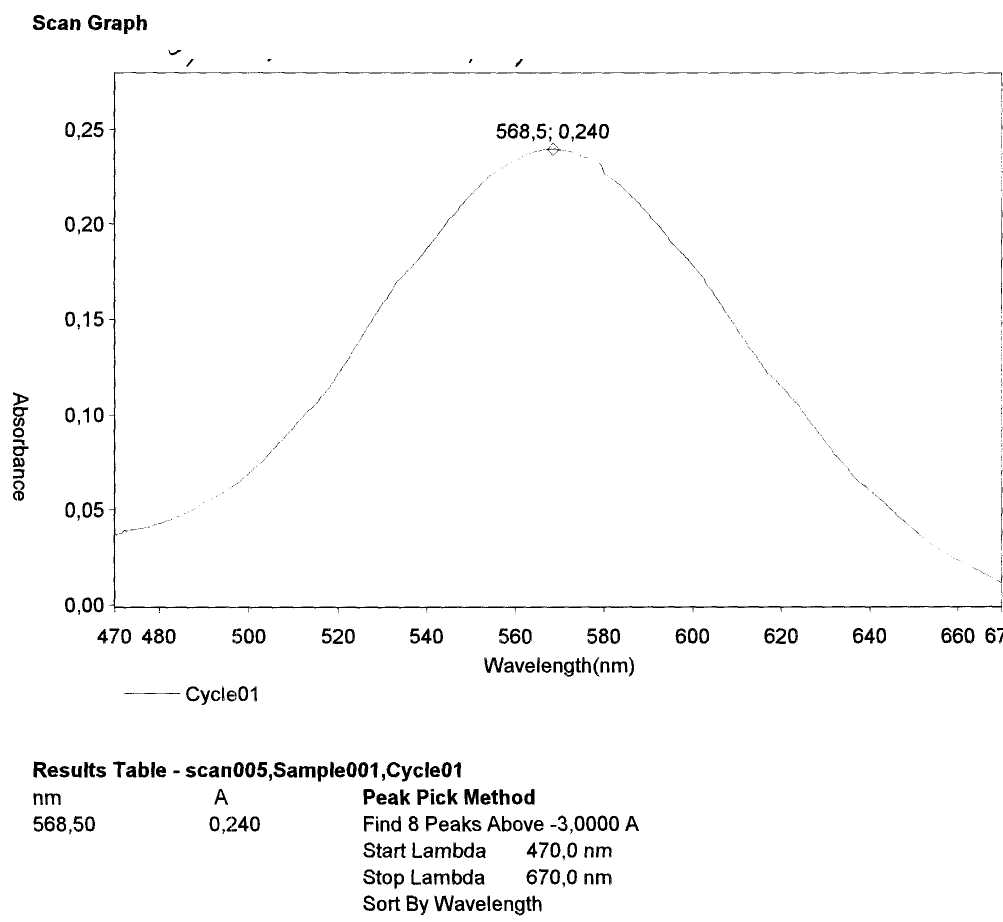
По полученным данным комплекс глютаминовой кислоты и нингидрина имеет максимум поглощения при длине волны 568±2 нм. Комплекс водного извлечения с нингидрином имеет максимум поглощения при длине волны 568,5 ±2нм (рис. 1 и 2).
Рис. 1. УФ-спектр комплекса водного раствора РСО глютаминовой кислоты с раствором нингидрина
Рис. 2. УФ-спектр комплекса водного извлечения из листьев каштана с раствором нингидрина.
С использованной разработанной методикой проанализированы образцы листа каштана конского обыкновенного и показаны в таблице 1 и 2.
Таблица 1
Результаты количественного определения суммы аминокислот в листьях каштана, в пересчёте на глютаминовую кислоту.
|
Образец |
Содержание аминокислот, в % |
|
1 |
0,76 |
|
2 |
0,76 |
|
3 |
0,77 |
|
4 |
0,78 |
|
5 |
0,78 |
|
_ Х% |
0,77 |
Таблица 2
Метрологические характеристики результатов спектрофотометрического количественного определения аминокислот, в пересчете на глютаминовую кислоту.
|
Наименование |
n |
f |
Р% |
t (Р,f) |
_ Х% |
S2 |
S |
_ &#; Х |
_ E% |
|
Показатели |
5 |
4 |
95 |
2,78 |
0,77 |
0,0001 |
0,01 |
0,0124 |
1,61 |
Согласно проведенным исследованиям, в листьях каштана конского обыкновенного, количественное содержание свободных аминокислот колеблется в пределах около 0,77%.
Достоверность предложенной методики определения суммарного содержания аминокислот подтверждена опытами с добавками кислоты глютаминовой. Результаты опытов представлены в таблице 3.
Относительная ошибка опытов с добавками находится в пределах случайной ошибки предложенной методики, что свидетельствуют об отсутствии систематической ошибки методики.
Таблица 3
Результаты количественного определения аминокислот в листьях каштана с добавками
глютаминовой кислоты
|
Содержание аминокислот в навеске, мг |
Добавлено глютаминовой кислоты, мг |
Должно быть, мг |
Найдено глютаминовой кислоты, мг |
Ошибка
|
|
|
Абсолютная, мг |
Относительная, % |
||||
|
0,85 |
0,1 |
0,95 |
0,94 |
-0,01 |
-1,06 |
|
0,85 |
0,2 |
1,05 |
1,04 |
-0,01 |
-0,96 |
|
0,85 |
0,3 |
1,15 |
1,14 |
+0,01 |
+0,87 |
Результаты статистической обработки проведенных опытов свидетельствует о том, что ошибка единичного определения суммы аминокислот, в пересчете на глютаминовую кислоту в листе каштана конского обыкновенного с доверительной вероятностью 95%, составляет ±1,61%.
Таким образом, разработана методика количественного определения суммы аминокислот в листе каштана конского обыкновенного с использованием спектрофотометрии.
Выводы
Подобраны оптимальные условия методики для спектрофотометрического определения суммы аминокислот листа каштана конского обыкновенного по реакции с нингидрином.
Разработана методика количественного определения суммы аминокислот в пересчете на РСО глютаминовой кислоты.
Количественное содержание суммы аминокислот в пределах 0,77% (в пересчете на глютаминовую кислоту).
Ошибка единичного определения с доверительной вероятностью 95% составляет ±1,61%.
Литература:
Гринштейн Дж., Виниц М. Химия аминокислот и пептидов, пер. с англ., [М.], 1965;
Гончарова Т.А., Гончарова Т. А. Энциклопедия лекарственных растений:— М.: Изд. дом "МСП", 1997.
Дзюба В.Ф., Николаевский В.А. Щербаков В.М. Коренская И.М. Лекарственные растения в фитотерапии Практическое пособие. - Воронеж: Изд-во ВГУ, 2004. - 83 с.
Р.М. Середин С.Д. Соколов Лекарственные растения и их применения Ставрополь, 1969.
Березов Т.Т., Коровкин Б.Ф. Биологическая химия. — М.: Медицина, 1983. — С. 426-579.
Похожие статьи
Никотиновая кислота как объект фармацевтической химии
D – оптическая плотность РСО глютаминовой кислоты, в нм. определения суммы аминокислот в листе каштана конского обыкновенного с использованием спектрофотометрии. Использование метода Лоури для количественного определения...
Изучение аминокислотного состава разных сортов меда из...
Пробоподготовка. Содержание аминокислот исследовали в водных растворах меда.
Содержание суммы аминокислот в сырье в % Х, в пересчёте на кислоту глютаминовую. Сравнительный анализ искусственного и натурального мёда и его...
Использование метода Лоури для количественного определения...
Для этого в мерную колбу вместимостью 25 мл вносили, соответственно, 0,1, 0,2, 0,3, 0,4 … 1 мл раствора СОП альбумина, прибавляли по 5 мл реактива Фолина, доводили водой до метки, выдерживали 30 минут и измеряли оптическую плотность полученных растворов в...
Влияние экзогенных аминокислот на растения озимой пшеницы...
Семена пшеницы замачивались в течение 1 мин в водных растворах аминокислот трех концентраций: , , моль/л.
Масса надземной части растений под действием аминокислот изменялась в большей степени, чем длина растений.
Биохимический состав протеинового концентрата из зеленых...
Аминокислотный состав ПЗК (табл. 2) свидетельствует о том, что по биологической ценности протеин ПЗК равноценен протеину рыбной муки. В протеине ПЗК содержится меньше лизина, метионина и цистина, но больше остальных незаменимых аминокислот...
Спектрофотометрическое определение скандия(III)...
Рис.2. Зависимость оптической плотности растворов комплекса cкандия(Ш) от рН в присутствии и отсутствие
Полученный осадок растворяют в воде, фильтруют в колбе емкотью 50 мл и разбавляют водой до метки.
Извлечение скандия, тория и РЗЭ фосфиноксидом...
Определение флавоноидов в траве Володушки золотистой...
Навеску измельченной травы 1,0 г помещали в круглодонную колбу, добавляют 100 см3 70 % этанола и 2 мл соляной кислоты и нагревают на водяной бане с обратным холодильником в течение 1 часа 30 мин. Раствор количественно переносили в мерную колбу на 100 см3 и...
Определение β-каротина в нативной биомассе дрожжей...
Навеску подвергали многократной экстракции гексаном, ацетоном и петролейным эфиром конец которой определяли по неизменности оптической плотности
переносили в мерную колбу на 25 мл, доводили объем до метки и фотометрировали при длине волны 450 нм.
Влияние некоторых аминокислот на рост Rhodococcus erythropolis...
Добавление в среду аминокислот вызывало прирост оптической плотности суспензии бактерий в 3 раза и более. Наименьшим рост-стимулирующим эффектом обладал триптофан – вероятно, что он расходуется клетками как предшественник для синтеза фитогормона...
Похожие статьи
Никотиновая кислота как объект фармацевтической химии
D – оптическая плотность РСО глютаминовой кислоты, в нм. определения суммы аминокислот в листе каштана конского обыкновенного с использованием спектрофотометрии. Использование метода Лоури для количественного определения...
Изучение аминокислотного состава разных сортов меда из...
Пробоподготовка. Содержание аминокислот исследовали в водных растворах меда.
Содержание суммы аминокислот в сырье в % Х, в пересчёте на кислоту глютаминовую. Сравнительный анализ искусственного и натурального мёда и его...
Использование метода Лоури для количественного определения...
Для этого в мерную колбу вместимостью 25 мл вносили, соответственно, 0,1, 0,2, 0,3, 0,4 … 1 мл раствора СОП альбумина, прибавляли по 5 мл реактива Фолина, доводили водой до метки, выдерживали 30 минут и измеряли оптическую плотность полученных растворов в...
Влияние экзогенных аминокислот на растения озимой пшеницы...
Семена пшеницы замачивались в течение 1 мин в водных растворах аминокислот трех концентраций: , , моль/л.
Масса надземной части растений под действием аминокислот изменялась в большей степени, чем длина растений.
Биохимический состав протеинового концентрата из зеленых...
Аминокислотный состав ПЗК (табл. 2) свидетельствует о том, что по биологической ценности протеин ПЗК равноценен протеину рыбной муки. В протеине ПЗК содержится меньше лизина, метионина и цистина, но больше остальных незаменимых аминокислот...
Спектрофотометрическое определение скандия(III)...
Рис.2. Зависимость оптической плотности растворов комплекса cкандия(Ш) от рН в присутствии и отсутствие
Полученный осадок растворяют в воде, фильтруют в колбе емкотью 50 мл и разбавляют водой до метки.
Извлечение скандия, тория и РЗЭ фосфиноксидом...
Определение флавоноидов в траве Володушки золотистой...
Навеску измельченной травы 1,0 г помещали в круглодонную колбу, добавляют 100 см3 70 % этанола и 2 мл соляной кислоты и нагревают на водяной бане с обратным холодильником в течение 1 часа 30 мин. Раствор количественно переносили в мерную колбу на 100 см3 и...
Определение β-каротина в нативной биомассе дрожжей...
Навеску подвергали многократной экстракции гексаном, ацетоном и петролейным эфиром конец которой определяли по неизменности оптической плотности
переносили в мерную колбу на 25 мл, доводили объем до метки и фотометрировали при длине волны 450 нм.
Влияние некоторых аминокислот на рост Rhodococcus erythropolis...
Добавление в среду аминокислот вызывало прирост оптической плотности суспензии бактерий в 3 раза и более. Наименьшим рост-стимулирующим эффектом обладал триптофан – вероятно, что он расходуется клетками как предшественник для синтеза фитогормона...