Cognitive impairment is a polyethological syndrome.
The main causes of cognitive impairment:
–stroke
–dyscirculatory encephalopathy
–brain tumor.
Pituitary infarction occurs due to hemorrhage or ischemia, most often in patients with pituitary macroadenoma, and headaches and nausea may occur.
PURPOSE. To present a clinical case of a patient with dementia on the background of Skien-Simmonds syndrome associated with pituitary macroadenoma, to analyze domestic and publications on methods of optimal treatment of dementia on the background of advanced pituitary apoplexy.
The analysis of domestic publications for the period 2011–2025 is carried out. The following databases were used: PubMed, eLibrary.RU, Frontiers platform. The search was conducted by keywords in Russian and English: dementia, pituitary gland, pituitary adenoma, Skien-Simmonds syndrome, akatinol memantine, NMDA receptors. The search depth for publications is 14 years, from 2011 to 2025 years.
A clinical case is presented.
To achieve a rapid clinical effect, complex therapy was recommended: antioxidant (mexidol in ampoules), NMDA receptor antagonists (akatinol memantine in tablets), the key role in this case is played by the appointment of the original form of memantine — akatinol memantine. The results of akatinol memantine therapy: increased general activity, increased ability to memorize new information, increased total nighttime sleep duration, decreased forgetfulness of current events, decreased apathy, decreased daytime sleepiness, and improved the overall quality of life of the patient.
A case of dementia associated with pituitary apoplexy on the background of its macroadenoma is presented. A significant sustained improvement in function was achieved as a result of the addition of acatinol memantine in a daily dose of 20 mg on an ongoing basis to complex therapy.
The presented clinical case is an example of the successful use of a drug that reduces NMDA receptor stimulation in terms of restoring cognitive functions, and therefore it is advisable to include an NMDA receptor antagonist (akatinol memantine) in the treatment regimen early to accelerate the patient's return to full-fledged activity. The main cause of dementia in this case is a pituitary infarction associated with a pituitary macroadenoma.
Keywords: dementia, pituitary gland, pituitary adenoma, Skien-Simmonds syndrome, akatinol memantine, NMDA receptors.
Введение
Когнитивные функции обеспечивают:
– темп познавательной деятельности;
– процесс обучаемости;
– речь;
– планирование и принятие решений;
– узнавание эмоций и мотивов поведения окружающих людей [1].
Основные причины развития когнитивных нарушений:
– инсульт;
– дисциркуляторная энцефалопатия;
– опухоль головного мозга [1].
У 25–30 % больных после перенесенного инсульта (даже нетяжелого) в течение года развивается деменция, у 30–70 % — умеренные когнитивные расстройства. Инсульт вдвое увеличивает риск заболеваемости деменцией [2].
Часто нарушения сна могут привести к нарушению запоминания новых событий — основному симптому деменции, особенно на поздних этапах жизни. При этом люди с когнитивными нарушениями спят больше днем и меньше — ночью, так как возникает нарушение работы соответствующих нейронов в гипоталамусе и стволе мозга [3].
Классификация видов памяти:
– мгновенная — удержание информации в полученном виде (длительность — 0,1–0,25 секунды);
– кратковременная — сохранение информации (от нескольких секунд до нескольких минут) после однократного ее восприятия;
– долговременная — хранение информации в течение длительного времени [4].
Деменцией является затрудняющее обыденную жизнь нарушение памяти и еще одной из когнитивных функций: восприятие, внимание, память, счет, речь или мышление [5].
Раньше всего при этом страдает кратковременная память (возникают забывчивость, привычка класть вещи не на те места, проблемы при использовании телефона), что сразу замечается родственниками [5].
Степени тяжести деменции:
– легкая (умеренная): постоянное умеренное снижение памяти, но затруднения возникают лишь в сложных видах деятельности;
– умеренно тяжелая: резкое нарушение ориентации и снижение способности выполнять привычные действия;
– тяжелая: полная зависимость от окружающих в повседневной жизни [6].
Помимо двигательных нарушений, достаточно часто встречаются координаторные нарушения разной степени выраженности, например неустойчивость при поворотах [6].
Для психических расстройств, связанных с поражением префронтальных отделов лобной доли, характерны:
– расторможенность со стороны эмоционально-волевой сферы: несдержанность, плоские шутки, дурашливость;
– апато-абулический синдром (синдром Серейского): аспонтанность, адинамия, абулия (безразличие к окружающему миру), выражающиеся в безынициативности, пассивности, снижении двигательной активности [7].
Неврологические осложнения гормонально неактивных опухолей гипофиза
Аденомы гипофиза составляют 14 % внутричерепных новообразований. Практически всегда доброкачественные, они возникают преимущественно из клеток передней доли гипофиза [8]. На томографических исследованиях обнаруживается картина увеличения размеров турецкого седла (более 15 мм), истончения его спинки, углубление его дна, оссификатов в нем либо углубление параселлярной области [9].
Гормонально неактивные опухоли гипофиза не сопровождаются развитием гормональных эндокринных расстройств, выявляются с одинаковой частотой у мужчин и женщин, составляют 25–43 % от всех опухолей гипофиза [10].
Основные жалобы у больных с гормонально неактивными опухолями гипофиза: головные боли, головокружение, снижение памяти, слабость, утомляемость, сонливость [10]. Также при аденомах гипофиза могут возникать нарушения функции гипоталамуса (при супраселлярном росте): расстройство ритма сна и бодрствования, нарушение аппетита [11]. Если аденома гипофиза по диаметру более 1 см, то это макроаденома; если менее —микроаденома [12].
Инфаркт гипофиза возникает вследствие кровоизлияния или ишемии чаще всего у больных с макроаденомой гипофиза, при этом могут возникнуть головные боли, тошнота. В ряде случаев возможно консервативное лечение, если отсутствуют неврологические проявления данной патологии [13].
Гипоталамо-гипофизарная недостаточность (гипопитуитаризм) развивается из-за повреждения аденогипофиза с последующим развитием гормональных нарушений. Одна из причин его возникновения — инфаркт гипофиза (септико-эмболический инфаркт, или апоплексия гипофиза, или синдром Шиена — Симмондса) [14]. Одним из проявлений синдрома Шиена — Симмондса является снижение работоспособности и толерантности к физическим нагрузкам [14].
Цель
Представить клинический случай пациента с деменцией на фоне синдрома Шиена — Симмондса, ассоциированного с макроаденомой гипофиза, провести анализ отечественных и зарубежных публикаций о методах оптимального лечения деменции на фоне развившейся апоплексии гипофиза.
Материалы и методы
Проведен анализ неврологических изданий за период 2011–2025 гг.
Представлен клинический случай.
Результаты и обсуждение
Непрерывное развитие медицины позволяет получать дополнительные данные об эффективности комплексной терапии в плане лечения деменции.
Назначение препаратов с мультимодальным механизмом действия исключает полипрагмазию и позволяет положительно влиять на различные звенья патогенеза поражения головного мозга как органа — мишени артериальной гипертензии. Одним из таких лекарственных средств является мексидол — оригинальный препарат этилметилгидроксипиридина сукцината. Это оригинальный препарат, противоишемическое действие которого реализуется за счет его выраженных антигипоксантных, антиоксидантных и мембранопротекторных свойств. Он подавляет развитие глутаматной эксайтотоксичности нейронов, снижает концентрацию конечных продуктов пероксидации и других субстратов свободнорадикального окисления при ишемии мозга, способствует синтезу и активации HIF-1 в условиях гипоксии [15]. Мексидол создает энергетическую почву для успешной работы мозга, при этом не вызывая замедления метаболизма [16]. Важно отметить, что мексидол не вызывает синдрома обкрадывания, в отличие от ряда ноотропов [17].
Ключевым при лечении данной патологии стало использование препаратов, одним из которых является оригинальная форма мемантина — акатинол мемантин.
Концепцией патогенетического механизма возникновения деменции является глутаматергическая. При недостаточности глутамата нарушается закрепление процесса запоминания, но при повышении его концентрации он действует как нейротоксин — активация NMDA-глутаматных рецепторов приводит к массивному поступлению в нейроны кальция, и возникающая утрата нейронов приводит к дальнейшим когнитивным расстройствам. Таким образом, препараты, снижающие эту стимуляцию, применяются для защиты от нейродегенерации.
Акатинол мемантин является единственным представителем антидементных препаратов, в основе действия которого лежит селективное блокирование глутаматных NMDA-рецепторов и улучшение выживаемости ацетилхолинергических нейронов [18]. Изредка данный препарат оказывает легкий психоактивирующий эффект, поэтому его нецелесообразно назначать на ночь [19]. В настоящее время не установлено возникновение синдрома отмены акатинола мемантина [20]. Именно дополнительной стимуляцией синтеза дофамина можно объяснить, что акатинол мемантин корректирует аффективные нарушения, в частности уменьшает апатию [21].
Положительный эффект терапии акатинолом мемантином в отношении когнитивных и эмоциональных расстройств развивается в течение трех месяцев терапии и остается стабильным в течение шести месяцев [22]. Акатинол мемантин отличается высоким уровнем безопасности по сравнению с другими препаратами [23].
Описание клинического случая
Представлен случай развития деменции, ассоциированной с апоплексией гипофиза (в анамнезе макроаденома гипофиза).
Клиническая картина на момент начала терапии: снижение памяти на текущие события; снижение внимания; выраженная сонливость, не проходящая после отдыха; снижение аппетита, настроения и интереса к жизни; нарушение походки (пациентку шатает вправо-влево), затруднение самообслуживания (из-за выраженной сонливости, не проходящей после отдыха, а также из-за постоянной забывчивости пациентка не могла самостоятельно есть, одеваться, заниматься домашними делами).
Значительное уменьшение сонливости, апатии, головокружения, улучшение кратковременной памяти достигнуты в результате лекарственной терапии: антигипоксанты (мексидол в ампулах), антагонисты NMDA-рецепторов (акатинол мемантин в таблетках). В данном случае ключевая роль отводится терапии антагонистами NMDA-рецепторов (акатинол мемантин в таблетках).
Пациентка: женщина, 78 лет (1947 г. р.).
Анамнез жизни: пациентка росла и развивалась без особенностей.
Анамнез заболевания: со слов сына (в сопровождении которого была на приеме), 29.01.2020 пациентка в связи с жалобами на головокружение и слабость самостоятельно прошла МРТ головного мозга (рис. 1, рис. 2, рис. 3).
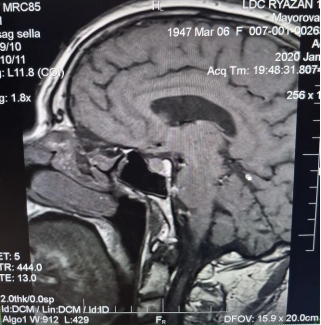
Рис. 1. МРТ головного мозга (T1 sag sella)
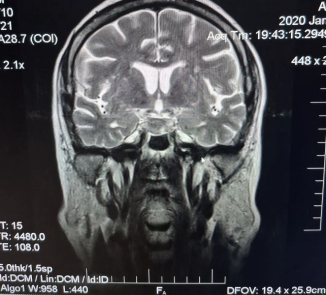
Рис. 2. МРТ головного мозга (T2 Cor)

Рис. 3. Заключение МРТ головного мозга от 29.01.2020
При этом гормональная активность не исключалась. Пациентка была затем проконсультирована нейрохирургом, заключившим, что «показаний к оперативному лечению нет» (при этом или заключение не было предоставлено, или пациентка не помнит, куда его положила).
Со слов сына, в анамнезе у пациентки гипертоническая болезнь. В 2022 г. на фоне повышения артериального давления (АД) до 200/100 мм рт. ст. отметила приступ выраженного головокружения, сопровождавшегося тошнотой, не связанной с приемом пищи, из-за чего не могла самостоятельно встать с кровати. Вызвала скорую медицинскую помощь, была доставлена в нейрососудистое отделение по месту жительства, где по результатам РКТ головного мозга диагноз «острое нарушение мозгового кровообращения» был исключен.
Затем, в 2022 г., лечилась стационарно в условиях терапевтического отделения по месту жительства с диагнозом «гипертоническая болезнь 3-й степени, 4-я степень риска сердечно-сосудистых осложнений, кризовое течение» (при этом или снимки и выписки не были предоставлены, или пациентка не помнит, куда их положила).
Затем, 17.12.2022, прошла МРТ головного мозга (рис. 4, рис. 5, рис. 6).
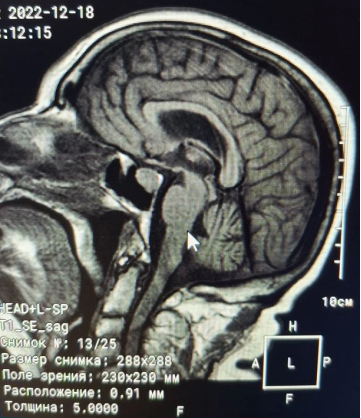
Рис. 4. МРТ головного мозга (T1 SE sag)
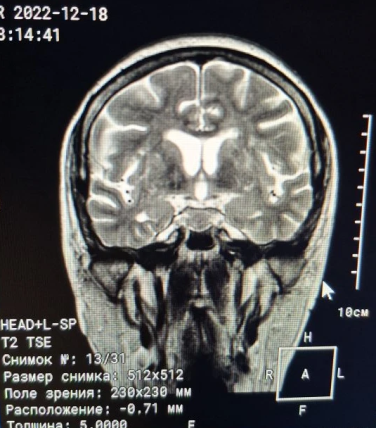
Рис. 5. МРТ головного мозга (T2 TSE)

Рис. 6. Заключение МРТ головного мозга от 17.12.2022
Затем, с 16.02.2023 по 28.02.2023, лечилась также в условиях неврологического отделения по месту жительства с диагнозом «цереброваскулярная болезнь вследствие гипертонической болезни и атеросклероза, хроническая ишемия мозга 3-й степени, умеренный вестибуло-атактический синдром, перманентный цефалгический синдром, декомпенсация». Динамика была положительной: значительно уменьшилось головокружение, пациентка стала самостоятельно вставать с кровати, ходить. Проводилась следующая терапия: нейропротекторная, витаминотерапия, сосудорасширяющая, антигипертензивная, антиагрегантная, гиполипидемическая, физиолечение.
Со слов сына, пациентка, начиная с 2022 г., стала заговариваться и часто забывать, куда положила вещи; смеяться без видимой причины; также без видимых причин возникла дневная сонливость, не проходившая после отдыха; ухудшился сон: она стала спать 3–4 часа вместо 6–7, часто просыпаться по ночам без видимой причины. Пациентка не обращалась к неврологу по месту жительства до 2024 г. — «было некогда»; но в 2024 г. отметила резкое нарастание вышеописанных симптомов плюс возникла частая плаксивость, резко ухудшилось настроение (на фоне смерти мужа). К психологу и психиатру по данному поводу не обращалась.
С 18.03.2024 по 29.03.2024 пациентка находилась в условиях дневного стационара ГБУ РО «ОКБ имени Н. А. Семашко» с диагнозом «цереброваскулярная болезнь на фоне гипертонической болезни, церебральный атеросклероз, хроническая ишемия мозга 2-й степени, выраженный синдром церебрастении и вестибулопатии». После перенесенного острого нарушения мозгового кровообращения была проведена нейропротекторная и сосудорасширяющая терапия. В 2021, 2023 и 2024 гг. не проходила МРТ головного мозга — «было некогда».
Далее, 18.04.2025 пациентка отметила повышение АД до 160/90 мм рт. ст., после которого возникли резкие слабость, сонливость, тошнота, отсутствие аппетита; 25.04.2025 самостоятельно прошла МРТ головного мозга (рис. 7, рис. 8, рис. 9):
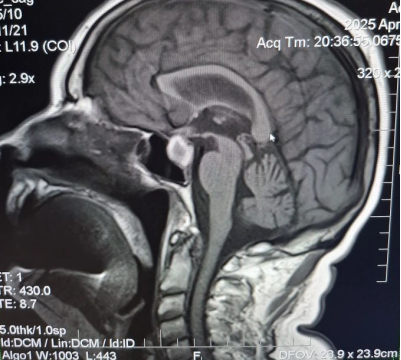
Рис. 7. МРТ головного мозга (T1 SE sag)
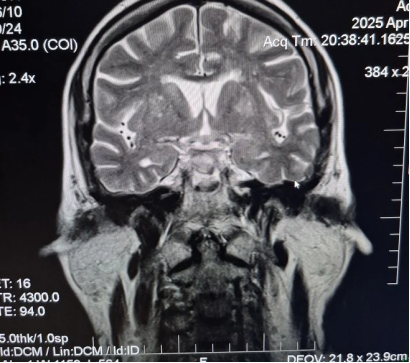
Рис. 8. МРТ головного мозга (T2 Cor)

Рис. 9. Заключение МРТ головного мозга от 25.04.2025
Затем пациентка обратилась за консультацией к нейрохирургу по месту жительства — или заключение не было предоставлено, или пациентка его потеряла. Со слов пациентки, она была направлена на консультацию к нейрохирургу НМИЦ нейрохирургии им. академика Н. Н. Бурденко для определения тактики лечения.
Пациентка 14.05.2025 была проконсультирована эндокринологом по месту жительства: были диагностированы вторичная надпочечниковая недостаточность и вторичный гипотиреоз; была назначена заместительная терапия гидрокортизоном (кортеф) — 10 мг в 8:00 и 5 мг в 16:00, а также терапия левотироксином натрия (L-Тироксин) — 25 мкг утром. На этом фоне пациентка отметила улучшение самочувствия, по данным от 30.04.2025:
– тиреотропный гормон — 0,076 мкМЕ/мл (норма — 0,27–4,2);
– пролактин — 192 мкМЕ/мл (норма — 102–496);
– адренокортикотропный гормон — 10,7 пг/мл (норма — 7,2–63,3);
– соматотропный гормон — 0,59 нг/мл (норма — меньше 5,0);
– кортизол — 26,0 нмоль/л (норма — 138–635).
Она была направлена на консультацию к нейрохирургу НМИЦ нейрохирургии им. академика Н. Н. Бурденко (19.05.2025). Ее состояние было расценено как апоплексия аденомы гипофиза; показаний к удалению опухоли на момент консультации не выявлено; была высокая вероятность резорбции погибшей опухоли; рекомендованы проведение МРТ головного мозга в ближайшее время и далее, через 4–6 месяцев, повторная консультация нейрохирурга в НМИЦ нейрохирургии имени академика Н. Н. Бурденко, стационарное лечение и обследование в специализированном эндокринологическом отделении.
В тот же день, 19.05.2025, пациентка была проконсультирована эндокринологом ФГАОУ ВО Первый МГМУ им. И. М. Сеченова. В результате выявлены гипопитуитаризм как следствие апоплексии макроаденомы гипофиза, вторичный гипотиреоз, вторичный гипокортицизм, соматотропная недостаточность; показано стационарное лечение в клинике эндокринологии УКБ № 2 Первого МГМУ им. И. М. Сеченова.
После этого, с 26.05.2025 по 05.06.2025, пациентка прошла лечение в условиях стационара в эндокринологическом терапевтическом отделении № 2 УКБ № 2 Первого МГМУ им. И. М. Сеченова с диагнозом «гипопитуитаризм, развившийся в исходе апоплексии макроаденомы гипофиза (18.04.2025); вторичный гипотиреоз в фазе медикаментозной компенсации; вторичный гипокортицизм; вторичный гипогонадизм; артериальная гипертензия 3-й степени повышения АД; 4-я степень риска сердечно-сосудистых осложнений». Наблюдалась положительная динамика при проведении следующей терапии: L-Тироксин 50 мкг утром, кортеф 10 мг утром и 5 мг днем. Улучшилось общее самочувствие, рекомендовано проведение МРТ головного мозга в ближайшее время и далее через 4–6 месяцев.
Затем, в июне 2025 г., обратилась к неврологу по месту жительства (пришла в сопровождении сына). Объективный статус: снижение конвергенции, менингеальных симптомов нет, сухожильные рефлексы (СХР) живые (D = S), координаторные пробы выполняет неуверенно, в позе Ромберга выраженное пошатывание, резко астенизирована, рефлексы орального автоматизма есть, снижение памяти и внимания (легко отвлекается во время расспроса), смеется и плачет невпопад, атактическая походка (выраженное пошатывание вправо-влево при ходьбе), спит 6 часов с перерывами (с ее слов). Пациентка была протестирована по следующим неврологическим шкалам:
- тест рисования часов:
– круг правильной формы (1 балл);
– числа от 1 до 12 (1 балл);
– числа внутри круга (1 балл);
– равный интервал между числами (1 балл);
– правильное расположение чисел 12, 3, 6, 9 (1 балл);
– разная длина часовой и минутной стрелок (1 балл);
– неверное положение начала и конца стрелок (0 баллов).
Итог — 6 баллов (норма — 12 баллов) [24];
- опросник самооценки памяти Макнера и Кана:
– забывает номера телефонов (2 балла — иногда);
– не помнит, куда положила вещи (3 балла — часто);
– не может в тексте найти место, которое читала, после перерыва (2 балла — иногда);
– пишет на бумаге список вещей для покупок, чтобы не забыть (1 балл — редко);
– из-за забывчивости пропускает встречи (1 балл — редко);
– забывает о предстоящих делах (1 балл — редко);
– забывает имена родственников (2 балла — иногда);
– трудно сосредоточиться на выполняемой работе (3 балла — часто);
– трудно вспомнить содержание только что просмотренного фильма (3 балла — часто);
– не узнаёт друзей (1 балл — редко);
– теряет нить разговора при общении (2 балла — иногда);
– забывает имена и фамилии новых друзей (3 балла — часто);
– во время общения трудно сосредоточиться (3 балла — часто);
– забывает, какой сегодня день недели (1 балл — редко);
– пишет с ошибками (3 балла — часто);
– нередко отвлекается (4 балла — очень часто);
– необходимо несколько раз послушать фразу для ее запоминания (4 балла — очень часто);
– трудно зафиксировать внимание во время чтения (3 балла — часто);
– забывает, что ей говорили (2 балла — иногда);
– трудно сосчитать сдачу с денежной суммы (2 балла — иногда);
– делает домашние дела очень медленно (2 балла — иногда);
– чувствует пустоту в голове (2 балла — иногда);
– забывает, какое сегодня число (2 балла — иногда);
– не помнит, выключила ли плиту (2 балла — иногда).
Итог — 54 балла (норма — 43 балла);
- оценка апатии — рейтинговая шкала апатии Лилля (LARS):
– снижение повседневной деятельности — выраженное;
– безынициативность — выраженная;
– мотивация — слабая;
– равнодушие — выраженное;
– недостаточность самооценки — выраженная [26].
Пациентке была назначена следующая терапия:
– мексидол — 4 мл внутримышечно раз в день ежедневно до 16:00 в течение 10 дней;
– акатинол мемантин — 20 мг утром после еды ежедневно в течение месяца.
Также был назначен повторный осмотр через месяц.
Далее, 09.07.2025, психолог диспансерного отделения ГБУ РО «ОПКБ имени Н. Н. Баженова» провел пациентке экспериментально- психологическое исследование, которое показало снижение активности процессов с нарушением их динамики, легким снижением объема памяти, умеренным снижением уровня интеллекта, а также изменение личности по органическому типу.
На следующий день, 10.07.2025, пациентка была осмотрена психиатром диспансерного отделения ГБУ РО «ОПКБ имени Н. Н. Баженова», который диагностировал органическое расстройство личности с умеренно выраженными когнитивными нарушениями.
В июле 2025 г. пациентка прошла повторный осмотр (пришла в сопровождении сына). Объективный статус: снижение конвергенции, менингеальных симптомов нет, СХР живые (D = S), координаторные пробы выполняет неуверенно, в позе Ромберга умеренное пошатывание, умеренно астенизирована, рефлексы орального автоматизма есть, снижение памяти и внимания (легко отвлекается во время расспроса), смеется и плачет невпопад (чуть меньше, чем месяц назад), атактическая походка (умеренное пошатывание вправо-влево при ходьбе). Пациентка стала более активной, стала немного улыбаться, охотнее отвечать на вопросы, стала спать на час больше — 7 часов — и с меньшими перерывами (с ее слов). Она была протестирована вновь по следующим неврологическим шкалам:
- тест рисования часов. Итог — 6 баллов (норма — 12 баллов), без динамики, по сравнению с июнем 2025 г.;
- опросник самооценки памяти Макнера и Кана. Итого — 48 баллов (норма — 43 балла). По сравнению с тестом в июне 2025 г.:
– лучше стала запоминать номера телефонов — 1 балл вместо 2;
– проще стало читать — 1 балл вместо 2;
– лучше стала запоминать имена родственников — 1 балл вместо 2;
– улучшилась концентрация во время общения — 2 балла вместо 3;
– меньше стала отвлекаться — 3 балла вместо 4;
– уменьшилась пустота в голове — 1 балл вместо 2;
- оценка апатии — рейтинговая шкала апатии Лилля (LARS):
– снижение повседневной деятельности — умеренное;
– безынициативность — выраженная;
– мотивация — умеренная;
– равнодушие — умеренное;
– недостаточность самооценки — выраженная.
Пациентке было рекомендовано продолжить прием акатинола мемантина в дозе 20 мг утром после еды ежедневно в течение месяца и прийти на повторный осмотр через месяц (не отметила побочных эффектов во время приема акатинола мемантина).
В августе 2025 г. она прошла повторный осмотр (пришла одна). Объективный статус: снижение конвергенции, менингеальных симптомов нет, СХР живые (D = S), координаторные пробы выполняет неуверенно, в позе Ромберга легкое пошатывание, легко астенизирована, рефлексы орального автоматизма есть, снижение памяти и внимания (меньше отвлекается во время расспроса), не смеется и не плачет невпопад, атактическая походка (легкое пошатывание вправо-влево при ходьбе). Пациентка стала более активной, стала чаще улыбаться, охотнее отвечать на вопросы, стала спать 8 часов и перерывы значительно уменьшились (с ее слов). Она была протестирована вновь по следующим неврологическим шкалам:
- тест рисования часов. Итог — 8 баллов (норма — 12 баллов). По сравнению с тестом в июне и июле, верно изобразила положение начала и конца стрелок;
- опросник самооценки памяти Макнера и Кана. Итого — 44 балла (норма — 43 балла). По сравнению с тестом в июле:
– лучше стала запоминать имена родственников — 0 баллов вместо 1;
– улучшилась концентрация во время общения — 1 балл вместо 2;
– меньше стала отвлекаться — 2 балла вместо 3;
– уменьшилась пустота в голове — 0 баллов вместо 1;
- оценка апатии — рейтинговая шкала апатии Лилля (LARS):
– снижение повседневной деятельности — легкое;
– безынициативность — умеренная;
– мотивация — выраженная;
– равнодушие — легкое;
– недостаточность самооценки — умеренная.
Динамика количества баллов по месяцам (тест рисования часов и опросник самооценки памяти Макнера и Кана) показана на рис. 10.
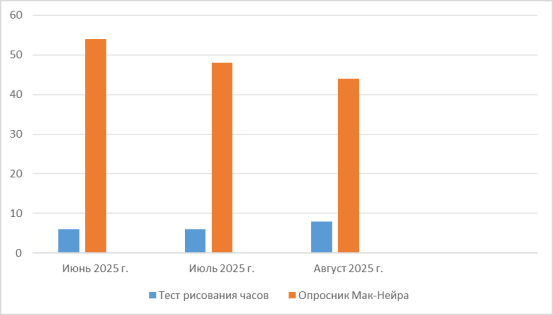
Рис. 10. Динамика количества баллов по месяцам (тест рисования часов и опросник самооценки памяти Макнера и Кана)
Таблица 1
Оценка апатии по шкале Лилля (динамика по месяцам)
|
Недостаточность самооценки |
Равнодушие |
Снижение повседневной деятельности |
Безынициативность |
Мотивация | |
|
Июнь 2025 г. |
Выраженная |
Выраженное |
Выраженное |
Выраженная |
Слабая |
|
Июль 2025 г. |
Выраженная |
Умеренное |
Умеренное |
Выраженная |
Умеренная |
|
Август 2025 г. |
Умеренная |
Легкое |
Легкое |
Умеренная |
Выраженная |
Пациентке было рекомендовано продолжить прием акатинола мемантина в дозе 20 мг утром после еды на постоянной основе и пройти повторный осмотр через шесть месяцев (побочных эффектов на фоне данной терапии не отметила).
Заключение
Представленный клинический случай является примером успешного применения препарата, в основе действия которого лежит блокирование глутаматных NMDA-рецепторов. Основной причиной развития деменции в данном случае является апоплексия гипофиза на фоне макроаденомы гипофиза, в связи с этим целесообразно раннее включение в схему терапии антагониста NMDA-рецепторов (акатинола мемантина в таблетированной форме) для ускорения процесса возвращения пациента к полноценной бытовой деятельности, так как, помимо влияния на когнитивные функции, данный препарат повышает активность и степень бытовой независимости больных [27].
Литература:
- Неврология : национальное руководство. Том 1 / под редакцией Е. И. Гусева, А. Н. Коновалова, В. И. Скворцовой. — Москва: ГЭОТАР-Медиа, 2018. — 880 с.
- Путилина М. В. Рациональная фармакотерапия хронической ишемии головного мозга : клинические рекомендации / М. В. Путилина, Н. В. Теплова. — Москва : МЕДпресс-информ, 2020. — 549 с.
- Грайпель Э. А. Деменции и когнитивные нарушения у взрослых. — Москва : ГЭОТАР-Медиа, 2025. — 128 с.
- Фролова Е. В. Нарушение когнитивных функций в пожилом возрасте : руководство для врачей / Е. В. Фролова, А. Ю. Емелин, В. Ю. Лобзин. — Москва : ГЭОТАР-Медиа, 2023. — 208 с.
- Голубев В. Л. Неврологические синдромы : руководство для врачей / В. Л. Голубев, А. М. Вейн. — Москва : МЕДпресс-информ, 2019. — 736 с.
- Одинак М. М. Нарушение когнитивных функций при цереброваскулярной патологии / М. М. Одинак, А. Ю. Емелин, В. Ю. Лобзин. — Санкт-Петербург : Спецлит, 2022. — 229 с.
- Тибекина Л. М. Асимметричный мозг. Психические, психофизиологические и клинические аспекты / Л. М. Тибекина, М. А. Алимова, Т. А. Шумакова. — Санкт-Петербург : ЭЛБИ — СПб, 2018. —123 с.
- Гусев Е. И. Неврология и нейрохирургия : учебник в 2-х томах. Том 2. Нейрохирургия / Е. И. Гусев, А. Н. Коновалов, В. И. Скворцова. — 4-е издание. — Москва : ГЭОТАР-Медиа, 2018. — 403 с.
- Латышева В. Я. Неврология и нейрохирургия / В. Я. Латышева, Б. В. Дривотинов, М. В. Олизарович. — Минск : Вышэйшая школа, 2013. — 511 с.
- Неврология : национальное руководство. Том 2 / под редакцией Е. И. Гусева, А. Н. Коновалова, В. И. Скворцовой. — Москва: ГЭОТАР-Медиа, 2019. — 432 с.
- Берлит П. Неврология. — Москва : МЕДпресс-информ, 2023. — 664 с.
- Древаль А. В. Эндокринология. — Москва : ГЭОТАР-Медиа, 2019. — 544 с.
- Аденомы гипофиза: современные принципы диагностики и лечения / Л. И. Астафьева, И. В. Чернов, И. В. Чехонин [и др.] // Нейрохирургия. — 2020. — Том 22, № 4. — С. 94–111.
- Дедов И. И. Эндокринология / И. И. Дедов, Г. А. Мельниченко, В. В. Фадеев. — Москва : ГЭОТАР-Медиа, 2007. — 432 с.
- Остроумова О. Д. Мозг — орган — мишень артериальной гипертензии / О. Д. Остроумова, А. И. Кочетков. — Научно-практическая конференция «Мультидисциплинарный подход в решении сложных вопросов полиморбидных пациентов», 2025. — URL: https://1med.tv/archive/npk-multidistsiplinarnyy-podkhod-v-reshenii-slozhnykh-voprosov-polimorbidnykh-patsientov/mozg-organmishen-arterialnoy-gipertenzii-kochetkov/ (дата обращения: 27.03.2026)
- Гусев Е. И. Хроническая цереброваскулярная недостаточность / Е. И. Гусев, Е. И. Чуканова, А. С. Чуканова. — Москва : АСТ 345, 2019. — 189 с.
- Ковальчук В. В. Теоретические предпосылки и практические аспекты адекватного ведения и эффективной реабилитации пациентов после инсульта. — Москва : АСТ 345, 2021. — 423 с.
- Моритц А. А. Роль иммуновоспалительных факторов в развитии негативной симптоматики при шизофрении / А. А. Моритц, П. С. Теребова, М. В. Иванов // Журнал неврологии и психиатрии имени С. С. Корсакова. — 2024. — № 11. — С. 42–48.
- Яхно Н. Н. Деменции : руководство для врачей / Н. Н. Яхно, В. В. Захаров, А. Б. Локшина [и др.]. — Москва : Медпресс-информ, 2010. — 86 с.
- Неврология. Клинические рекомендации / Минздрав. — Москва : ГЭОТАР-Медиа, 2025. — 776 с.
- Додементные когнитивные расстройства: современные подходы к терминологии, диагностике и лечению / Е. Е. Васенина, Д. А. Гуторова, И. М. Смирнова [и др.] // Фарматека. — 2018. — Том 25, № 14. — С. 8–17.
- Эффективность акатинола мемантина у пациентов с недементными когнитивными расстройствами. Результаты многоцентрового клинического наблюдения / Н. Н. Яхно, И. С. Преображенская, В. В. Захаров [и др.] // Российский неврологический журнал. — 2019. — № 3. — С. 37–44.
- Междисциплинарная неврология / под редакцией Ал. Б. Данилова, Ан. Б. Данилова. — Москва : Ремедиум, 2021. — 384 с.
- Клинические шкалы в неврологии / под общей редакцией О. С. Левина. — Москва : МЕДпресс-информ, 2023. — 272 с.
- Левин О. С. Клинические шкалы в неврологии / О. С. Левин, Е. Е. Васенина, О. А. Ганькина [и др.]. — Москва : МЕДпресс-информ, 2019. — 192 с.
- Стал С. М., Морриссетт Д. Э. Иллюстрации доктора Стала. Болезнь Альцгеймера и другие деменции. — Москва : ГЭОТАР-Медиа, 2023. — 240 с.
- Левин О. С. Основные лекарственные средства, применяемые в неврологии. — Москва : МЕДпресс-информ, 2022. — 400 с.

