Медь активно участвует в биологическом круговороте и входит в число жизненно важных микроэлементов. При недостатке или отсутствии меди в растениях уменьшается содержание хлорофилла, растение перестает плодоносить, листья желтеют, могут погибнуть. В оптимальных концентрациях медь способствует росту и развитию растений и повышает их холодостойкость [1]. Азотсодержащие соединения являются составными компонентами в производстве фармакологических, поверхностно-активных, моющих средств, стимуляторов роста растений, антикоррозионных веществ, бактерицидных препаратов, гербецидов и др. [2].
Исходя из этого синтез комплексных соединений, содержащих азот и медь, представляет значительный интерес в плане получения новых биологически активных веществ. Синтезированы координационные соединения меди (II) ацетилкарбамидом [3]. Авторами установлено, что в координационных соединениях меди (II) с ацетилкарбомидом последний координирован монодентатно через карбамидный атом кислорода.
Авторами разработаны новые теоретические и экспериментальные подходы для изучения комплексообразования меди (II) с органическими соединениями, содержащими в качестве донорных атомы азота и кислорода. Исследовано комплексообразование меди (II) с пенициллинами и β-лактамными антибиотиками рН-метрическим методом. Во всех случаях соотношение Сu(II):L в титруемых растворах составило 1:5, что позволило учесть возможность образования полилигандных комплексов [4].
В работе [5] описано изучение бинарных комплексов N-фосфонометилглицина с меди (II) методами потенциометрии и электронной спектроскопии, а также определение влияния аминокислоты на процесс комплексообразования.
Авторами исследованы комплексообразующие свойства поли-N,N-диаллиламиноэтановой кислоты на ионы меди и кобальта при низких концентрациях полимера и ионов металлов в растворе [6]. Определены условия образования продуктов взаимодействия полимера с ионами меди и кобальта, что позволяет управлять характеристиками комплексообразующих свойств поли N,N-диаллиламиноэтановой кислоты.
Авторами изучено комплексообразование гидрохлорида глюкозамина (ГХГА) с нитратами меди и цинка [7]. Установлено, что комплекс образуется быстро и состав его не изменяется во времени. Определены отношение чисел молей металла, вошедших в комплекс с ГХГА, константа реакции комплексообразования.
Анализ литературных материалов показывает, что процессы образования комплексов полимеров с металлами (Cu, Co) привлекает внимание многих исследователей.
Водорастворимые олигомеры на основе морфолина и эпихлоргидрина являются перспективными макромолекулярными лигандами для комплексообразования с металлами. Они содержат в структуре четвертичный атом азота и кислород, которые могут вступать в донорно-акцепторные взаимодействия с катионами переходных металлов.
Целью данного параграфа являлся исследование комплексообразования между олигомером на основе морфолина и эпихлоргидрина с медью (II).
УФ-исследование проведено на приборе Specord 210 имеющий точность фотометрии UV с дихромат калием в соответствии с Ph.Eur ≤ ± 0,01. Параметры изменения были следующим: спектральный диапазон измерения 190–1000 нм, щель 1 нм, скорость сканирования 2 нм в секунду.
Реакцию комплексообразования исследовали в растворах бидистиллированной воды. Изучение комплексообразования олигомера (лиганда) с медью проводили в водной среде. К 2,5 мл водного раствора олигомера (10–3–10–5 моль/л) при перемешивании при комнатной температуре прибавляли 2,5 мл раствора нитрата меди (10–3–10–5 моль/л). После смешивания исходных реагентов сразу снимали спектры поглощения. Растворы готовили по точной навеске на бидистиллированной воде. Комплексы с медью выделены в индивидуальном состоянии при добавлении олигомера морфолина (МФ) с эпихлоргидрином (ЭХГ) к водному раствору нитрата меди.
Обычно связь между ионом металла и полимерным лигандом осуществляется посредством донорно-акцепторного взаимодействия с образованием координационной связи (хелатные комплексы) или замещением протона лиганда ионом металла с образованием ионной связи. Ионы металлов являются акцепторами; атомы O-, -N, -S, -F, -Cl полимерной цепи, предоставляющие пару электронов для образования связи, являются донорами.
Комплексообразование олигомера морфолина с эпихлоргидрином (1) и нитрата меди (II) оценивалось по изменению спектров поглощения. Комплексообразующие свойства олигомера на основе морфолина с эпихлоргидрином были исследованы спектрофотометрическим методом с использованием водных растворов Cu(NO3)2 на катионы Cu+2 [8, 9].
Комплексообразующие свойства Cu+2 в водных растворах исследовали определением зависимости оптической плотности раствора (А) от длины волны (λ) в зависимости оптической плотности от концентрации водного раствора олигомера. Сначала приготовили серии растворов в интервале концентрации соли металла олигомера (10–3–10–5 моль/л). Далее определены максимальные значения длин волн (λmax) от оптической плотности (А) водных растворов исходных реагентов и комплекса (рис.1).
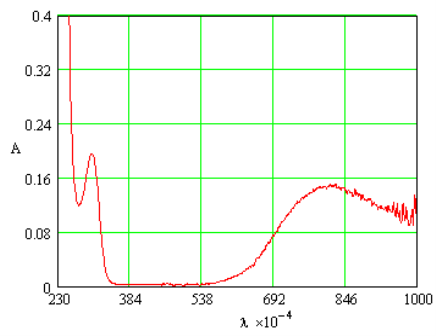
Рис. 1. Зависимость оптической плотности водного раствора Cu(NO3)2 от длины волны
Полученные данные показывают, что максимальное значение λmax находится примерно в интервале 240 нм для олигомера и 790 нм для ионов меди. В электронных спектрах смесей олигомера с Cu(NO3)2 наблюдается появление новой полосы в интервале 540–690 нм, что указывает на образование комплексного соединения (рис.2).
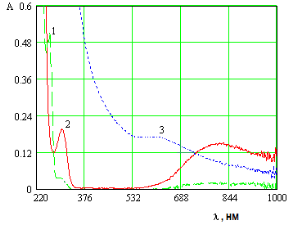
Рис. 2. Зависимость оптической плотности (А) от длины волны (λ): 1-олигомер на основе морфолина с эпихлоргидрином; 2-нитрат меди; 3-смесь олигомера (I) с Cu(NO3)2
Далее проведены исследования комплексообразования при [Cu(NO3)2]=const с увеличением концентрации олигомера для полного связывания ионов металлов в исследуемый комплекс (рис.3). При увеличении концентрации олигомера происходит увеличение оптической плотности постепенное смещение данного максимума в длинноволновую область. Во всех исследуемых системах электронные спектры имеют общий характер изменения. Смещение полосы поглощения в длинноволновую область указывает на связывание олигомера в комплексное соединение.
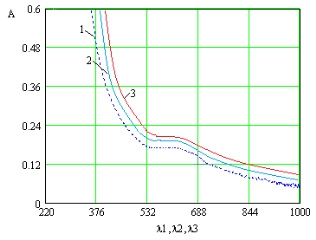
Рис. 3. Зависимость оптической плотности раствора Cu(NO3)2 и его смесей с олигомером: [Cu(NO3)2]=0,001 моль/л=cost от длины волны. Концентрация олигомера, моль/л: 1–0,0001; 2–0,001; 3–0,01
В ходе исследования были определены молярный коэффициент светопоглощения, состав комплекса и константа устойчивости по формуле ελ=А/С х l, где ελ- молярный коэффициент светопоглощения лучей, А-значение (табл.1).
Как видно из таблицы с увеличением концентрации раствора электролита наблюдается резкое повышение молярного коэффициента светопоглощения, что свидетельствует о полном связываете ионов Cu+2.
Таблица 1
Значение молярного коэффициента светопоглощения растворами комплексов, Т=20 оС
|
ελ=А/С |
Концентрация раствора |
||
|
0,0001М |
0,001М |
0,01М |
|
|
Олигомер на основе морфолина с ЭХГ |
2490 |
4700 |
7680 |
Cостав реагента — ион металла определяли методом «насыщения». Сущность метода заключается в установлении зависимости величины D от концентрации одного из компонентов при постоянной концентрации второго компонента и наоборот (рис.4).
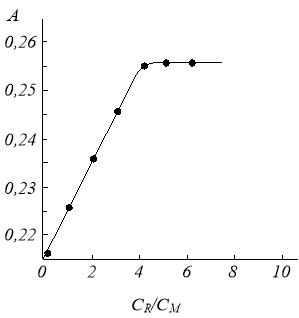
Рис. 4. Зависимость оптической плотности растворов комплекса от состава для 0,01М раствора Сu(NO)2
Как видно из рисунка 9, точка излома на кривой отвечает отношению стехиометрических концентраций реагирующих веществ в точке Хэкв — абсциссе точки эквивалентности. Также видно из рисунка, что увеличением концентрации реагирующих веществ во всех рассмотренных случаях оптическая плотность растет до определенных значений, далее остаётся постоянной величиной, что свидетельствует об образовании устойчивого комплекса.
Структуру синтезированного комплексного соединения исследовали ИК-спектральным анализом (рис.5). Сравнение спектров взаимодействия олигомера с ионами меди и исходного олигомера показывают, что основное строение олигомерного продукта не перетерпивает существенных изменений, однако наблюдается некоторое смещение полос поглощения (рис.5,6). В ИК-спектре олигомера на основе морфолина с ЭХГ наблюдаются валентные колебания связи NH в области 3393 см -1, слабые полосы в области 2871–2960 см-1 относятся к аммониевому катиону, веерные колебания NH связи в области 866 см-1; колебания связей СО при 1114 см-1, а С-N при 1069 см1.
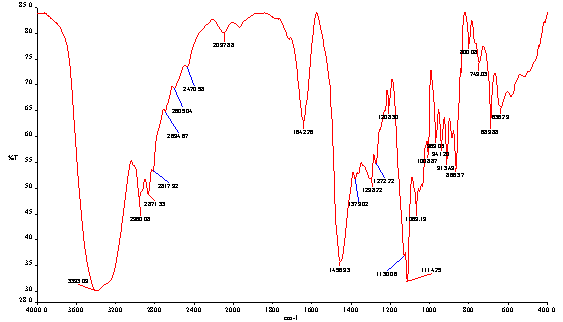
Рис. 5. ИК-спектр синтезированного олигомера на основе морфолина и эпихлоргидрина
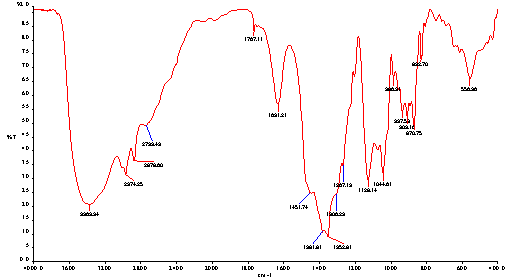
Рис. 6. ИК-спектр синтезированного комплекса на основе олигомера морфолина и эпихлоргидрина с нитратом меди
На основе результатов ИК-спектроскопии предложена предпологаемая структура синтезированного комплексного соединения.
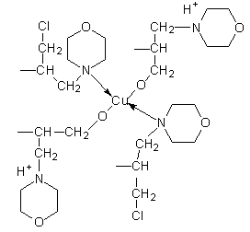
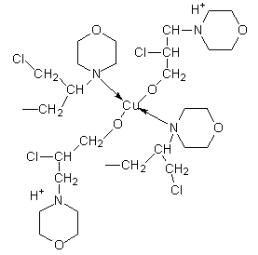
Таким образом, спектрофотометрическими исследованиями изучено взаимодействие олигомера на основе морфолина и эпихлоргидрина с нитратом меди. Установлено, что синтезированные олигомеры на основе морфолина с эпихлоргидрином обладают достаточно высокими комплексообразующими свойствами на катионы меди.
Литература:
- Харитонова Е. В., Журавлев О. Е., Червинец В. М., Ворончихина Л. И., Демидова М. А. Синтез и антимикробная активность тетрахлорферратов четвертичного аммония, пиридиния и морфолиния. Химико-фармацевтический журнал, 2012. –№ 5. –С.6–8.
- Клячин А. И., Румянцева О. И. Опыт применения препарата тиотриазолин (морфолиний-метил-триазолил-тиоацетат) у больных с алкогольным поражением печени. Журн. Вопросы наркологии. 2011. –№ 3. –С.63–68.
- Козьминых Е. Н., Козьминых В. О., Махмудов Р. Р., Одегова Т. Ф., Беляев А. О. Синтез, противомикробная и анальгетическая активность 4-арил-2-N-морфолино-4-оксо-2-бутеновых кислот. Химико-фармацевтический журнал, 2004. –Т.38. –№ 8. –С.25–26.
- Гатаулина, Г. А. Кутырев, И. С. Низамов, М. П. Кутырева Функционализация гиперразветвленных полиэфирополиолов вторичными аминами. Тез. докл. X Научной конференции молодых ученых, аспирантов и студентов научно-образовательного центра Казанского (Приволжского) федерального университета «Материалы и технологии XXI века». Казань, 2011. — С.33.
- М. П. Кутырева, А. Г. Гатаулина, Г. А. Кутырев, И. С. Низамов, Н. А. Улахович Полиядерные комплексы меди(II) с полидентатными нанолигандами на основе аминопроизводных гиперразветвленных полиэфиров. Журн. общей химии. — 2011. — Т.81, Вып.7. — C. 1187–1190.
- А. Р. Гатаулина, А. Р. Мухаметзянова, М. П. Кутырева, Г. А. Кутырев, Н. А. Улахович. Биологически активные полиэфирополиамины и их металлокомплексы. Тез. докл. XVIII Всероссийской конференции «Структура и динамика молекулярных систем». — Казань, 2011. — С.99.
- Бродский М. С., Макаров А. П. Способ получения n-метилморфолин-n-оксида. Патент РФ № 2061690, 1996.
- Залелова А. К., Пономаренко О. В., Манкей Б. М., Хамзина С. С. Изучение производных на основе соединений ряда фурана и ортомуравьинного эфира. Валихановские чтения-17: Сборник материалов Международной научно-В 17 практической конференции. — Кокшетау, 2013. –С. 28–31.







