Методы и значение цитогенетического исследования плодного материала как заключительного этапа пренатальной диагностики
Авторы: Меренова Светлана Владимировна, Белоусова Светлана Евгениевна, Назарова Евгения Николаевна, Валиуллова Жанна Жиенбаевна, Ольшевская Татьяна Борисовна
Рубрика: 11. Прочие отрасли медицины и здравоохранения
Опубликовано в
III международная научная конференция «Медицина: вызовы сегодняшнего дня» (Москва, январь 2016)
Дата публикации: 06.01.2016
Статья просмотрена: 5631 раз
Библиографическое описание:
Методы и значение цитогенетического исследования плодного материала как заключительного этапа пренатальной диагностики / С. В. Меренова, С. Е. Белоусова, Е. Н. Назарова [и др.]. — Текст : непосредственный // Медицина: вызовы сегодняшнего дня : материалы III Междунар. науч. конф. (г. Москва, январь 2016 г.). — Москва : Буки-Веди, 2016. — С. 77-79. — URL: https://moluch.ru/conf/med/archive/193/9427/ (дата обращения: 27.04.2024).
В патологии развития человека одно из важных мест принадлежит нарушениям наследственного аппарата. Самопроизвольные аборты, рождение детей с тяжелыми аномалиями развития, мужское и женское бесплодие, многие патологические состояния постнатального периода, в том числе и хромосомные болезни, обусловлены изменениями генома. По некоторым оценкам общий генетический груз в популяции оценивается величиной в 5–5,5 %, из которых на долю новорожденных приходиться около 1,5 %. При этом значительная часть нарушений онтогенеза связана с числовыми или структурными аберрациями всего генома или отдельных хромосом, и может быть выявлена цитогенетическими методами. Таким образом, цитогенетические исследования играют важную роль в диагностике многих патологических состояний на разных стадиях онтогенеза человека. Особое значение они приобретают, если проводятся еще до рождения. Именно в этот период хромосомные болезни можно не только диагностировать, но и предупредить путем элиминации плодов с нарушениями кариотипа. Профилактика рождения детей с хромосомными болезнями составляет главную задачу такого научно-практического направления как пренатальная диагностика.
Пренатальная диагностика (ПД) наследственных и врожденных болезней— новый раздел медицинской генетики, возникший в 80-е годы ХХ в. на стыке клинических дисциплин (акушерство, гинекология, неонатология) и фундаментальных наук (генетика человека, цитогенетика, молекулярная биология, эмбриология, биохимия, патофизиология). В плане практической медицины ПД представляет собой комплекс врачебных мероприятий и диагностических методов, направленных на выявление морфологических, структурных, функциональных или молекулярных нарушений внутриутробного развития человека. Последние проявляются в виде изолированных или множественных врожденных уродств, дизрупций, дезформаций, недоразвитий, хромосомных или моногенных болезней, в виде пороков или дисфункций жизненно важных систем, органов и тканей, которые приводят к гибели плода или к тяжелым, нередко смертельным, заболеваниям в постнатальном периоде. [1,с.289]
Основные методы и подходы, применяемые в ПД наследственных и врожденных болезней, включают комплекс обследований, главной целью которых является отбор беременных в группы высокого риска рождения детей с врожденной и наследственной патологией, которые нуждаются в углубленных дополнительных лабораторных исследованиях. Одно из них — кариотипирование плода. Кариотипирование — цитогенетическое исследование, позволяющее определить численные и структурные отклонения хромосомного набора.Клиническими показаниями для цитогенетической пренатальной диагностики являются следующие состояния:
наличие хромосомной аномалии у предыдущего ребенка в семье;
мертворожденный ребенок с хромосомной аномалией, совместимой с жизнью;
хромосомные перестройки, хромосомный мозаицизм или анеуплодия по половым хромосомам у родителей;
результаты исследования сыворотки крови у матери, указывающей на повышенный риск хромосомной аномалии у плода;
возраст матери;
выявленные при ультразвуковом исследовании аномалии плода;
подозрение на мозаицизм плода при предыдущем цитогенетическом исследовании;
подозрение на наличие синдрома с хромосомной нестабильностью. [3, с.29]
Материалом для этих исследований служат биоптат ворсин хориона, плаценты (11–18 неделя) и пуповинная кровь плода (21–22 неделя). Полученные результаты дают возможность постановки диагноза на ранних сроках беременности с точностью до 99,8 %, предупреждая развитие осложнений беременности и угрозы здоровью матери, увеличивают шанс рождения здорового поколения.
Одним из важнейших факторов, влияющих на выбор типа клеток плода для конкретного пренатального цитогенетического исследования, является показание, по которому беременной женщине рекомендована пренатальная цитогенетическая диагностика.
Хромосомные препараты, получаемые из ворсинчатой ткани, при ряде методических преимуществ (возможность исследования кариотипа плода в 1 триместре беременности быстрота и простота исследования), обладают и некоторыми недостатками. Главные из них — меньшее, чем в культуре лимфоцитов, количество метафазных пластинок в препарате, пригодных для исследования, не всегда хорошая морфология хромосом, и как правило, плохое дифференциальное окрашивание хромосом.
Кроме того, при исследовании хромосомных препаратов из ворсин можно столкнуться с мозаицизмом, ограниченным плацентой. Клетки хориона относятся к внезародошевым оболочкам и обособляются от эмбриобласта в процессе эмбриогенеза очень рано. При делении клеток в них, независимо от клеток эмбриобласта, могут происходить события, приводящие к постзиготичесому нерасхождению хромосом и образованию клона клеток с иным, чем у плода кариотипом. Таким образом, кариотип клеток ворсин может не всегда соответствовать истинному кариотипу плода. Так образуется мозаицизм, ограниченный плацентой, который встречается примерно в 1 % наблюдений и может привести к ложному диагнозу. Клетки крови плода, как и все клетки соединительной ткани, являются производными эмбриобласта и наиболее полно отражают кариотип плода.
При подозрении на наличие у плода структурных хромосомных перестроек, (при семейном носительстве структурных хромосомных перестроек), а так же при наличии у плода во 2 триместре беременности комплекса пороков или отклонений в развитии, выявленных при УЗИ, рекомендуется осуществление цитогенетического исследования на основании хромосомного анализа культуры лимфоцитов пуповинной крови. На этих препаратах возможно осуществление анализа большого количества метафазных пластинок с требуемой морфологией. [2, с. 66–67]. Данный метод исследования предусматривает выдачу результата анализа в течение 5 дней, т. к. время от посева культуры в питательную среду до фиксации материала (инкубация) составляет 72 часа.
Использование «прямых» хромосомных препаратов из ворсин хориона может быть рекомендовано при прочих показаниях (старший репродуктивный возраст женщин, предыдущий ребенок с синдромом Дауна или другими хромосомными аберрациями), когда чаще всего можно ожидать численные аберрации хромосом [2, с. 67].
При работе с тканью ворсинчатого хориона наша лаборатория использует метод анализа «прямых» препаратов, который основан на исследовании спонтанно делящихся клеток цитотрофобласта без их предварительного культивирования. Метод приготовления хромосомных препаратов плода удобен, прост в выполнении и сравнительно дешев, т. к. не требует длительного культивирования клеток [2.с.64.] Срок выдачи результата анализа составляет 2–3 дня. Клетки ворсинчатого хориона, плаценты доступны для традиционного цитогенетического анализа с 10–20 недели беременности. Однако, как показали исследования, оптимальные сроки для кариотипирования плода по ворсинам хориона 11–15 недель, так как, пограничное состояние цитотрофобласта «хорион-плацента» дает низкое количество и качество метафазных пластинок, и малую пригодность хромосом для стандартной окраски.
Для хромосомного анализа крови плода используют стандартную методику стимулирования лимфоцитов фитогемагглютинином (ФГА). Этот метод дает наиболее адекватное представление о хромосомном статусе плода и настоятельно рекомендуется для кариотипирования плода в случае хромосомного мозаицизма в плаценте.
Подавляющее большинство ПД во всем мире и в России проводится после 10-й недели, преимущественно во II триместре беременности (15–25-я недели). Именно в этот период осуществляются все основные операции с целью получения плодного материала для последующих лабораторно-диагностических мероприятий [1, с289.].
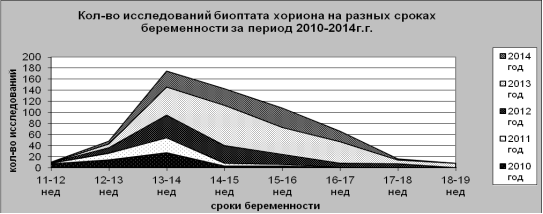
Проанализировав сроки беременности женщин поступивших на инвазивную диагностику, мы получили следующие результаты (таблица 1). На графике хорошо видно, что в основном исследования проводились на сроках 13–14 недель. Количество инвазивных процедур, проводимых на сроках превышающих 16 недель, невелико. Но именно они вносят лепту в процент неинформативных исследований, так как, получить достаточное количество митозов и выдать полноценный результат, работая на материале плаценты (17–18 недель), значительно сложнее. Анализ показал, что на протяжении пяти лет процент неинформативных исследований остается стабильным и составляет около 6 %.
 5
5
За период 2010–2014г.г. отделением пренатальной диагностики цитогенетической лаборатории МГК было произведено 853 исследования. Из них 578 исследований ворсин хориона, и 275 — кордоцентезы. В результате обнаружено 137 случаев хромосомной патологии, что составляет 16 % от всех проведенных исследований. 77 % от всей выявленной патологии приходится на трисомии по различным аутосомам — 106 случаев, среди них 73 случая трисомии 21(с-м Дауна), 20 — трисомия 18 (с-м Эдвардса), 13 — трисомия 13 (с-м Патау).
Кроме трисомий по аутосомам было выявлено 12 случаев патологии по половым хромосомам (8,7 %): моносомия по Х- хромосоме (45, Х — с-м Шерешевского-Тернера) — 10 случаев, с-м Клайнфельтера (47,ХХУ) — 2 случая.
Известно, что полиплоидия является одной из самых частых причин замирания беременности и спонтанных абортов на ранних сроках, несмотря на это нами было выявлено 2 случая тетраплоидии (92,ХХХХ) и 6 — триплоидий (69,ххх) в условиях пролонгированных беременностей. Все случаи полиплоидии выявлены в материале ворсин хориона у женщин, прошедших скрининг 1 триместра. Пролонгация данных беременностей, скорее всего, связана с наличием нормального клона клеток в тканях эмбриона. Но и в этом случае прогноз таких беременностей однозначен.
Среди плодов, у которых не обнаружено хромосомного дисбаланса, выявлено 4 случая носительства сбалансированных транслокаций, две из которых являются робертсоновскими: 45,ХУ, der (13;14), 45,ХУ, der (D;21), 46,ХХ, t(6;7)(q26;q22), 46,ХХ, t (2;5)(q37;q24).
Итог биохимического и УЗ-скрининга — расчет индивидуального риска по хромосомной патологии плода. Но наличие высоких рисков не является стопроцентной гарантией того, что плод, который носит женщина, имеет хромосомную патологию. И при высоких рисках плод может оказаться здоровым, и при пограничных — иметь измененный кариотип. Окончательный ответ на этот вопрос может дать только цитогенетическое исследование плодного материала.
Литература:
- Баранов В. С., Кузнецова Т. В. Цитогенетика эмбрионального развития человека: Научно-практические аспекты / Баранов В. С., Кузнецова Т. В. — СПб: Издательство Н-Л, 2006. — 640 с.: 141 ил.
- Цитогенетические методы диагностики хромосомных болезней. Методическое пособие для врачей. / Е. К. Гинтер, Т. В. Золотухина, В. Г. Антоненко, Н. В. Шилова, Т. Г. Цветкова, Л. Ю. Жулева. — Москва 2009: 82с. с ил.
- Рекомендации по обеспечению качества и надежности цитогенетических исследований. Европейские стандарты для цитогенетических исследований конститутивных и приобретенных хромосомных аномалий. /. Постоянная рабочая группа организации «Цитогенетики и общество» Европейской цитогенетической ассоциации (Е. С. А.). Материал подготовлен В. Г. Антоненко, и И. Г. Лильп при участии Т. В. Золотухиной, М. А. Курниковой, АА.Степановой, М. Г. Твороговой, Н. В. Шиловой, Л. Ю. Заранкиной
Похожие статьи
Беременность малого срока и ретрохориальная гематома...
ворсина хориона, пренатальная диагностика, хромосомная аномалия, плод, предыдущий ребенок, постнатальный период, плодный материал, кариотип плода, ворсинчатый хорион, хромосомная патология.
Значение трехмерной визуализации в первом триместре...
[5, 6]. При проведении трехмерного исследования исключается возможность диагностической ошибки при измерении шейной складки, используемой для диагностики хромосомных аномалий плода. [7, 8].
Перинатальные исходы при макросомии плода
Наиболее распространенной причиной перинатальной патологии является крупный плод.
По данным ВОЗ частота родов с крупным плодом за период с 1990 по 2007 гг. возросла с 8% до 12%.
Материалы и методы: Для анализа перинатальных исходов при макрососмии плода...
Исходы беременности и родов при макросомии плода
Ранняя диагностика хромосомной патологии плода по программе OSCAR Гнецкая В.А., Курцер М.А. 2010г 24-28 стр.
При крупном плоде осложнения родов встречаются в два раза чаще, чем при рождении детей с нормальной массой тела.
Строение плаценты у первородящих после аборта в анамнезе
Патогистологические особенности плаценты как универсального показателя состояния плода проанализированы на основе
Также нами выявлены, преждевременное созревание ворсин, инволютивно-дистрофические процессы во всех микроструктурах ворсинчатого хориона и...
Анализ перинатальных исходов у женщин с внутриутробным...
Внутриутробное инфицирование плода, как заболевание, осложняющее развитие плода и здоровье новорожденного.
Аномалии развития нервной системы у детей, рожденных от...
К группе риска развития инфекционной патологии у матери, плода и новорожденного относится...
Профилактика и коррекция плацентарной недостаточности...
...ткани, предотвращает развитие дефектов васкуляризации, нарушения созревания хориона и в
Окончательным и самым достоверным методом диагностики патологических изменений в
и 36 нед беременности (период выраженной диссоциации прибавки массы плода и...
Аномалии развития нервной системы у детей, рожденных от...
Их следует отличать от постнатальных (госпитальных) инфекций новорожденных.
Данный комплекс инфекций может привести к внутриутробной гибели плода, вызвать аномалии его развития. Велик шанс родить ребенка с пороками развития нервной, сердечно — сосудистой...
Клинико-диагностическое значение фактора роста плаценты...
Таким образом, станет возможна разработка ранних методов диагностики, а, следовательно, в будущем и мер, направленных на профилактику плацентарной недостаточности и синдрома задержки роста плода.
Материал иметоды исследования.
Похожие статьи
Беременность малого срока и ретрохориальная гематома...
ворсина хориона, пренатальная диагностика, хромосомная аномалия, плод, предыдущий ребенок, постнатальный период, плодный материал, кариотип плода, ворсинчатый хорион, хромосомная патология.
Значение трехмерной визуализации в первом триместре...
[5, 6]. При проведении трехмерного исследования исключается возможность диагностической ошибки при измерении шейной складки, используемой для диагностики хромосомных аномалий плода. [7, 8].
Перинатальные исходы при макросомии плода
Наиболее распространенной причиной перинатальной патологии является крупный плод.
По данным ВОЗ частота родов с крупным плодом за период с 1990 по 2007 гг. возросла с 8% до 12%.
Материалы и методы: Для анализа перинатальных исходов при макрососмии плода...
Исходы беременности и родов при макросомии плода
Ранняя диагностика хромосомной патологии плода по программе OSCAR Гнецкая В.А., Курцер М.А. 2010г 24-28 стр.
При крупном плоде осложнения родов встречаются в два раза чаще, чем при рождении детей с нормальной массой тела.
Строение плаценты у первородящих после аборта в анамнезе
Патогистологические особенности плаценты как универсального показателя состояния плода проанализированы на основе
Также нами выявлены, преждевременное созревание ворсин, инволютивно-дистрофические процессы во всех микроструктурах ворсинчатого хориона и...
Анализ перинатальных исходов у женщин с внутриутробным...
Внутриутробное инфицирование плода, как заболевание, осложняющее развитие плода и здоровье новорожденного.
Аномалии развития нервной системы у детей, рожденных от...
К группе риска развития инфекционной патологии у матери, плода и новорожденного относится...
Профилактика и коррекция плацентарной недостаточности...
...ткани, предотвращает развитие дефектов васкуляризации, нарушения созревания хориона и в
Окончательным и самым достоверным методом диагностики патологических изменений в
и 36 нед беременности (период выраженной диссоциации прибавки массы плода и...
Аномалии развития нервной системы у детей, рожденных от...
Их следует отличать от постнатальных (госпитальных) инфекций новорожденных.
Данный комплекс инфекций может привести к внутриутробной гибели плода, вызвать аномалии его развития. Велик шанс родить ребенка с пороками развития нервной, сердечно — сосудистой...
Клинико-диагностическое значение фактора роста плаценты...
Таким образом, станет возможна разработка ранних методов диагностики, а, следовательно, в будущем и мер, направленных на профилактику плацентарной недостаточности и синдрома задержки роста плода.
Материал иметоды исследования.











