О возможности использования пластинчатого тканеэквивалентного фантома для верификации дозового распределения в лучевой терапии
Авторы: Селиванов Максим Германович, Александрук Александр Геннадьевич, Четвериков Сергей Федорович, Пономарев Андрей Сергеевич
Рубрика: 4. Медицинские материалы, средства и изделия
Опубликовано в
V международная научная конференция «Медицина и здравоохранение» (Казань, май 2017)
Дата публикации: 15.03.2017
Статья просмотрена: 402 раза
Библиографическое описание:
Селиванов, М. Г. О возможности использования пластинчатого тканеэквивалентного фантома для верификации дозового распределения в лучевой терапии / М. Г. Селиванов, А. Г. Александрук, С. Ф. Четвериков, А. С. Пономарев. — Текст : непосредственный // Медицина и здравоохранение : материалы V Междунар. науч. конф. (г. Казань, май 2017 г.). — Казань : Бук, 2017. — С. 30-33. — URL: https://moluch.ru/conf/med/archive/240/12004/ (дата обращения: 26.04.2024).
В статье рассмотрены строение и принцип действия радиохромной плёнки, описано её применение в клинической дозиметрии, в частности в пластинчатом тканеэквивалентном фантоме; описаны преимущества и недостатки ионизационной камеры, метода лучевой терапии с модулированной интенсивностью.
Ключевые слова: лучевая терапия, клиническая дозиметрия, радиохромная плёнка, тканеэквивалентный фантом, система планирования, ионизационная камера, фантомные пластины
Количество злокачественных заболеваний среди населения пожилого и молодого возраста с каждым годом растёт. По данным Всемирной организации здравоохранения каждый год от онкологических заболеваний в мире умирают более 8 млн. человек [1]. Исследования и разработки новых приборов и методов для лечения опухолей и их внедрение в клиническую практику позволит повысить качество помощи, оказываемой онкологическим больным, и повысить качество их дальнейшей жизни, что, несомненно, является делом первоочередной важности.
На сегодняшний день существует несколько видов лечения рака: хирургическое лечение, химиотерапевтическое лечение, гормональная терапия, лучевая терапия и различные их комбинации.
Эффективным способом лечения злокачественных новообразований является лучевая терапия, главной задачей которой является захват в объём облучения максимального количества раковых клеток при минимальном включении в этот же объём здоровых клеток.
При лечении раковых опухолей с помощью излучения врач-радиотерапевт описывает режим лечения, который включает в себя величину однократной дозы за фракцию, количество фракций и суммарную терапевтическую дозу за весь курс лучевой терапии. Основной задачей при этом является уничтожение или контроль опухолевых клеток при минимизации осложнений вследствие повреждения нормальных тканей.
В настоящее время широкое развитие получила лучевая терапия с модулированной интенсивностью. Данный метод заключается в том, что с помощью специальных компьютерных систем (систем планирования) составляется пространственное распределение дозы излучения таким образом, чтобы уничтожить только раковые клетки, не повреждая здоровые ткани и органы. Данный вид терапии подразумевает под собой изменение положения источника излучения относительно пациента для получения максимальной точности.
Для проведения оптимального лечения доза излучения должна доставляться с высокой точностью. Контроль качества распределения доз осуществляется с помощью клинической дозиметрии. Определить величину дозы вне среды невозможно. В лучевой терапии окружающей средой являются либо тело пациента, либо фантом. Фантомом называется конструкция из особого материала, воспроизводящего дозиметрические свойства тканей пациента для отдельных видов излучения. Существуют два типа фантомов: геометрические, которые упрощают анатомию человека до простых геометрических фигур, и антропоморфные [2]. Внутрь фантома на расчётную глубину помещают специальные приборы — дозиметры, которые регистрируют величину падающей дозы, симулируя поглощение клетками опухоли.
Для проведения клинической дозиметрии используют разные виды дозиметров. Широко используемым видом являются ионизационные камеры, являющиеся “золотым стандартом” клинической дозиметрии. Отклик ионизационной камеры известен и экспериментально исследован лучше, чем у других детекторов. Однако, она далека от идеального универсального дозиметра [3] и не всегда в состоянии удовлетворить высоким требованиям измерения поглощённых доз из-за своих конструкционных особенностей и размеров.
Полупроводниковые детекторы являются относительно новым типом дозиметров и широко входят в клиническую практику благодаря своим малым размерам. Основным недостатком диодов является то, что они теряют свои свойства при накоплении полученной дозы из-за разрушения структуры. Из-за высокого атомного номера диода по сравнению с водой диоды не являются тканеэквивалентными для энергий фотонов ниже энергии 60Co, что ограничивает их применение для рентгеновского диапазона.
Ионизационные камеры или полупроводниковые детекторы в некоторых случаях не обеспечивают необходимого пространственного разрешения. Основным недостатком ионизационной камеры является то, что она измеряет ионизацию только в одной точке за один раз, что делает крайне трудоёмким и продолжительным процесс измерения поперечных профилей дозного распределения. Помимо этого, ионизационная камера не приспособлена для дистанционной лучевой терапии с генерацией полей неправильной формы (например, при использовании многолепесткового коллиматора), так и для интраоперационной лучевой терапии. Для решения этой проблемы были разработаны массивы ионизационных камер, имеющих разрешение порядка 1 мм.
Однако, ввиду своих размеров, ионизационные массивы не позволяют оценить пространственное распределение доз в трёх направлениях при единичной экспозиции. Решением этой проблемы может являться плёночная дозиметрия. В качестве интегрирующего дозиметра плёнка удобна для проведения дозиметрии подвижного облучения, например, при использовании динамических клиньев, секторном и ротационном облучении [2], а также при лучевой терапии с модулированной интенсивностью.
Для проведения дозиметрии высоких доз разработаны радиохромные плёнки [2]. Дозиметрия с использованием радиохромных самопроявляющихся плёнок позволяет добиться точности менее миллиметра [4]. Данные плёнки являются тканеэквивалентными и практически не имеют энергетической зависимости в диапазоне энергий фотонного излучения медицинского линейного ускорителя. Такие плёнки не реагируют на видимый свет, что упрощает работу с ними [3]. Плёнка имеет низкую чувствительность к энергии ионизирующего излучения и может быть использована для дозиметрии как фотонных, так и электронных пучков. Современные радиохромные плёнки содержат двойной слой эмульсии, поэтому воздействие окружающей среды на неё минимально. Непосредственно перед облучением плёнка представляет собой прозрачный, бесцветный “лист”. Когда она подвергается воздействию ионизирующего излучения, запускается реакция полимеризации, в результате чего производится краситель-полимер определённого цвета. Количество полимера и глубина изменения цвета пропорциональна поглощённой дозе в активном слое. Поскольку процесс полимеризации не передаётся от кристалла к кристаллу, а также отсутствует процесс проявления после воздействия излучения, который мог бы изменить размер или форму частиц, то данные плёнки имеют микронное разрешение. Получение данных о дозе производится при помощи сканнера планшетного типа с опцией сканирования прозрачных оригиналов. Работа с такими плёнками относительно проста, но требует соблюдения определённых правил. Одним из самых распространённых применений их в клинике является верификация индивидуальных лечебных планов. Пространственное разрешение ограничено главным образом только применяемым при работе оборудованием.
Основными недостатками радиохромных плёнок являются:
- Невозможность повторного использования плёнки;
- Ухудшение качества изображения в течение длительного промежутка времени;
- Длительный процесс измерения для стабилизации изменения цвета.
При применении пластинчатого тканеэквивалентного фантома в плёночной дозиметрии можно добиться получения нескольких дозных распределений на разных глубинах при одной экспозиции. Кроме того, применение такого типа фантома позволяет сократить время дозиметрического исследования, также плёнка обеспечивает высокое пространственное разрешение.
Предлагаемый твердотельный геометрический пластинчатый тканеэквивалетный фантом представляет собой набор фантомных пластин 30×30 см, что обеспечивает достаточное рассеяние фотонов в материале для полей большинства размеров, используемых в лучевой терапии [2]. Толщина используемых фантомных пластин может быть 0,2; 0,3; 0,5; 1 см, что позволяет врачу-радиологу менять их последовательность для достижения расчётной глубины исследуемого участка. Последние 10 сантиметров предназначены для рассеивания проходящего излучения согласно [5].
Пользователь может выбрать любой материал в качестве дозиметрического фантома: воду, полистирен или акриловый пластик (оргстекло). Дозиметрические измерения, проводимые в водном фантоме, занимают большое количество времени. А дозиметры, применяемые в таких фантомах, нуждаются в обязательной защите от воды. С другой стороны, в отличие от воды, полистирен или акрил не являются полностью тканеэквиалентными средами, поэтому необходима корректировка геометрии калибровки пучка в фотонной дозиметрии высоких энергий и использование поправочных коэффициентов в дозиметрии высоких энергий [3]. Материал, который будет использоваться в фантоме — оргстекло. Оно имеет несколько преимуществ:
- Является тканеэквивалетным;
- Твердотельное исполнение;
- Относительная дешевизна материала.
Соединение фантомных пластин между собой осуществляется с помощью четырёх штырей и соответствующих гаек, с помощью которых они закрепляются на конструкции. Скрепление гайками позволяет нивелировать воздушные зазоры между пластинами. Воздушные зазоры искажают получение результатов ввиду того, что воздух не является тканеэквивалентной средой.
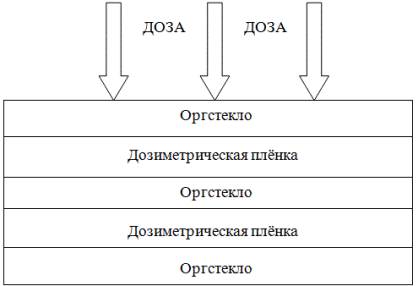
Рис. 1. Схематичное изображение работы фантома
Все фантомы являются заменителями, и конечная цель их применения заключается в том, чтобы предсказать конечную дозу в теле пациента. В идеальном случае нужно оценивать дозу на самом пациенте, но по очевидным причинам это не всегда возможно и в значительной степени ограничено облучаемой поверхностью пациента [2].
Анализ литературы показывает, что проблема рассматривалась достаточно широко [6,7,8]. В то же время целый ряд методических вопросов, связанных с созданием фантома и получением практических данных остаётся мало разработанным. К этим вопросам прежде всего стоит отнести:
- Использование поправочных коэффициентов ввиду не полной тканеэквивалентности плёнки и материала фантома;
- Использование в качества материала плексигласа или полистирола влечёт за собой дополнительное накладывание пластинок металла в связи с эффектом накопления электрического заряда.
В заключение стоит отметить, что предложенный фантом позволит за одну экспозицию получать данные дозного распределения сразу на нескольких глубинах, позволяя тем самым значительно сократить время исследования. В конструкции фантома детали съемные и легкозаменяемые, что важно при возможном выходе из строя оборудования.
Литература:
- Рак: основные цифры и факты // Всемирная организация здравоохранения. URL: http://www.who.int/cancer/ru/ (дата обращения: 12.12.2016).
- Ратнер Т. Г., Бочарова И. А., Брегадзе Ю. И., Коконцев А. А. Определение поглощенной дозы при дистанционной лучевой терапии. — Вена: МАГАТЭ, 2004. — 269 с.
- Клиническая дозиметрия фотонных и электронных пучков медицинских ускорителей на основе полимерных плёнок Gafchromic EBT-3 // Бесплатная электронная библиотека. URL: http://konf.x-pdf.ru/18meditsina/282180–1-klinicheskaya-dozimetriya-fotonnih-elektronnih-puchkov-medicinskih-uskoriteley-osnove-polimernih-plenok-gafchromic-ebt.php (дата обращения: 12.12.2016).
- Кузнецова Е. В., Грищук Д. Д., Понежа Т. Е. Получение и анализ двумерных дозовых распределений с помощью радиохромных плёнок // Медицинская физика. — 2012. — № 1. — С. 27–33.
- TRS 398 Dosimetry protocol for radiotherapy // ACADEMIA. URL: http://www.academia.edu/4177066/TRS_398_DOSIMETRY_PROTOCOL_ FOR_RADIOTHERAPY_version_05_june_2006 (дата обращения: 21.01.2017).
- Лощаков И. И. Введение в дозиметрию и защита от ИИ. — СПб.: Санкт-Петербургский Государственный Политехнический Университет, 2008. — 145 с.
- Дозиметрия // VMEDE. URL:http://vmede.org/sait/?id=Medbiofizika_fedor ov_2008&menu =Medbiofizika_fedorov_2008&page=36 (дата обращения: 21.01.2017).
- Дозиметрия ионизирующих излучений // Факультет естественных и инженерных наук. URL: http://fein.unidubna.ru/document/Programme/Bio physics /Posobie-DOZIMETRIYA.pdf (дата обращения: 21.01.2017).
Ключевые слова
система планирования, лучевая терапия, клиническая дозиметрия, радиохромная плёнка, тканеэквивалентный фантом, ионизационная камера, фантомные пластиныПохожие статьи
О возможности изменения изодозного распределения в лучевой...
Ключевые слова: лучевая терапия, тканеэквивалентный фильтр, болюс, изодозное распределение.
1. Ратнер Т. Г. Клиническая дозиметрия. Теоретические основы и практическое применение / Т. Г. Ратнер, Н. А. Лютова.
Автоматизация системы расчета дозы ионизирующего излучения...
В состав автоматизированной системы «Дозиметрия» можно включить следующие подсистемы
При проведении лучевой терапии, применяемой для лечения опухолей головного мозга, шеи и
О возможности использования пластинчатого тканеэквивалентного...
Вопросы обеспечения радиационной защиты больных раком...
Для лучевой терапии молочной железы предпочтительнее технология лучевой терапии с модулированной интенсивностью пучков
О возможности использования пластинчатого тканеэквивалентного...
Система мониторинга интенсивности ионизирующего излучения...
Использование ионизирующих излучений в промышленности...
Радиология и практика.
О возможности использования пластинчатого тканеэквивалентного... В лучевой терапии окружающей средой являются либо тело пациента, либо фантом.
Влияние протонной и лучевой терапии на когнитивные функции...
При проведении лучевой терапии, применяемой для лечения опухолей головного мозга, шеи и т. д., необходима фиксация, с целью избежания
О возможности использования пластинчатого тканеэквивалентного...
Клинический случай агрессивной аденомы гипофиза...
Разработка системы рентгенозащитных ограждений
О возможности использования пластинчатого тканеэквивалентного...
Система мониторинга интенсивности ионизирующего излучения... Отзывы и защиты наших авторов.
Вопросы обеспечения радиационной защиты больных раком молочной железы при лучевой терапии.
Компьютерная томография: технические аспекты качества...
Следует также отметить, что в современных клинических центрах врачи имеют доступ к
Активность γ-источников для дистанционной лучевой терапии колеблется от 37 ГБк (1 Кu).
О возможности использования пластинчатого тканеэквивалентного...
Экспериментальное исследование парамагнитного гепатотропного...
Многочисленные лабораторные и клинические исследования показали, что гадолиний в комплексе не наносит вред здоровью пациента [7].
Подготовленные фантомы печени крыс и водных растворов контрастного соединения GDOF-Mn-DTPA помещались на штативе в камеру...
Похожие статьи
О возможности изменения изодозного распределения в лучевой...
Ключевые слова: лучевая терапия, тканеэквивалентный фильтр, болюс, изодозное распределение.
1. Ратнер Т. Г. Клиническая дозиметрия. Теоретические основы и практическое применение / Т. Г. Ратнер, Н. А. Лютова.
Автоматизация системы расчета дозы ионизирующего излучения...
В состав автоматизированной системы «Дозиметрия» можно включить следующие подсистемы
При проведении лучевой терапии, применяемой для лечения опухолей головного мозга, шеи и
О возможности использования пластинчатого тканеэквивалентного...
Вопросы обеспечения радиационной защиты больных раком...
Для лучевой терапии молочной железы предпочтительнее технология лучевой терапии с модулированной интенсивностью пучков
О возможности использования пластинчатого тканеэквивалентного...
Система мониторинга интенсивности ионизирующего излучения...
Использование ионизирующих излучений в промышленности...
Радиология и практика.
О возможности использования пластинчатого тканеэквивалентного... В лучевой терапии окружающей средой являются либо тело пациента, либо фантом.
Влияние протонной и лучевой терапии на когнитивные функции...
При проведении лучевой терапии, применяемой для лечения опухолей головного мозга, шеи и т. д., необходима фиксация, с целью избежания
О возможности использования пластинчатого тканеэквивалентного...
Клинический случай агрессивной аденомы гипофиза...
Разработка системы рентгенозащитных ограждений
О возможности использования пластинчатого тканеэквивалентного...
Система мониторинга интенсивности ионизирующего излучения... Отзывы и защиты наших авторов.
Вопросы обеспечения радиационной защиты больных раком молочной железы при лучевой терапии.
Компьютерная томография: технические аспекты качества...
Следует также отметить, что в современных клинических центрах врачи имеют доступ к
Активность γ-источников для дистанционной лучевой терапии колеблется от 37 ГБк (1 Кu).
О возможности использования пластинчатого тканеэквивалентного...
Экспериментальное исследование парамагнитного гепатотропного...
Многочисленные лабораторные и клинические исследования показали, что гадолиний в комплексе не наносит вред здоровью пациента [7].
Подготовленные фантомы печени крыс и водных растворов контрастного соединения GDOF-Mn-DTPA помещались на штативе в камеру...











