В патогенезе сердечно-сосудистых заболеваний основную роль играют нарушения обменных процессов в сердечной мышце. Кровоснабжение миокарда имеет ряд органоспецифических особенностей: каждое мышечное волокно контактирует с 3–4 капиллярами, имеется множество анастомозов, эндотелий микрососудов обладает высокой метаболической активностью, коронарный кровоток относительно замкнут и в некоторой степени автономен, за что ряд исследователей называет его третьим кругом кровообращения — «коронарным кругом». Пластичность микроциркуляторного русла (МЦР) зависит от возраста и от функциональной нагрузки на орган.
В условиях ишемии в первую очередь изменяется строение капиллярной сети. Ишемическое повреждение на первых порах сопровождается усилением транспортной функции капилляров, повышением сосудистой проницаемости как в зоне гипоксии, так и в интактных участках миокарда. Ранее было отмечено, что причиной сужения капиллярного просвета является набухание ядер эндотелиальных клеток, отёк перицитов, систолический компрессионный эффект, непосредственное разрушение сосудов МЦР, либо сочетание этих факторов. Известно, что в стенке левого желудочка на 1 мм2 площади среза приходится 3–4 тыс. капилляров, но из них функционирует не более 50 %, также насчитывается 1826±50 кардиомиоцитов (КМЦ) [1]. Кровоснабжение правого желудочка сердца отличается большим количеством анастомозов между терминальными ветвями правой и левой венечных артерий.
Целью настоящего исследования является констатация, анализ и трактовка изменений морфометрических показателей структурных компонентов функционального элемента миокарда (ФЭМ) в условиях его острой ишемии. Для реализации цели были поставлены следующие задачи:
- Определить морфометрические показатели МЦР миокарда в ишемической, геморрагической и окружающей (реактивной) зонах субэпикардиального, интрамурального и субэндокардиального слоев сердечной мышцы.
- Замерить диаметры капилляров, количество функционирующих капилляров на единицу площади, диаметры и объемы ядер КМЦ в указанных локализациях.
- Рассчитать интегративные морфометрические значения (объем капиллярного русла, радиус диффузии) в изучаемых зонах.
- Сопоставить и проанализировать полученные данные.
Материалы иметоды исследования.
Материалом исследования послужили кусочки миокарда, взятые через всю толщу стенки левого желудочка у 5 беспородных собак, на высоте эфирно-кислородного наркоза, через 2 часа после перевязки передней ветви левой коронарной артерии. Контролем послужил материал тех же собак, взятый из неизмененной зоны левого желудочка. Срезы окрашивались гематоксилином и эозином, ставилась PAS — реакция и PAS — реакция с контролем амилазой. Препараты просматривались с помощью светооптической и поляризационной микроскопии. Проводилось измерение диаметра капилляров — d (мкм), подсчитывалось количество функционирующих капилляров — N (на 1 мм2 площади среза).
В срезах, окрашенных гематоксилин — эозином, измеряли диаметр КМЦ — D (мкм), а железным гематоксилином — площадь ядер КМЦ — S (мкм2) по формуле (1):
![]() (1)
(1)
где a – малый, b – большой диаметры ядра, ![]() = 3,14.
= 3,14.
Объем капиллярного русла (V) и радиус диффузии (R) в различных зонах миокарда (субэпикардиальной, интрамуральной, субэндокардиальной) рассчитывался в условных единицах по формулам (2, 3):
V=147∙N∙d(2)
где 147 – константа, N – количество функционирующих капилляров (шт/мм2), d – диаметр капилляров (мкм).
![]() (3)
(3)
где ![]() = 3,14, N — количество функционирующих капилляров (шт/мм2).
= 3,14, N — количество функционирующих капилляров (шт/мм2).
Полученные данные были обработаны методами вариационной статистики.
Результаты.
Таблица 1
Количество функционирующих капилляров (N), их диаметр (d), диаметр КМЦ (D), площадь ядер КМЦ (S), объем капиллярного русла (V), радиус диффузии (R) вслоях миокарда: а) интактной зоны, б) ишемической зоны, в) зоны геморрагического пояса, г) зоны реактивных изменений
|
Показатель |
Субэпикард |
Интрамуральный слой |
Субэндокард |
В среднем по миокарду | |
|
а) | |||||
|
N (шт/мм2) |
7329,4±424,8 |
11203,6±556,7 |
5640,5±679,5 |
8057,3±510,0 | |
|
d (мкм) |
3,0±0,2 |
9,3±0,5 |
5,9±0,3 |
5,6±0,3 | |
|
D (мкм) |
11,8±0,5 |
12,7±0,7 |
13,0±0,7 |
12,0±0,6 | |
|
S (мкм2) |
32,01±2,6 |
33,9±0,2 |
19,7±1,6 |
28,07±1,4 | |
|
V (усл. ед.) |
3307711,8±8352513,1 |
15316441,5±1163297,1 |
4941754,8±1498901,7 |
7855302,27±7161237,3 | |
|
R (усл. ед.) |
0,0066±0,0002 |
0,0053±0,0001 |
0,0074±0,0005 |
0,00643±0,0003 | |
|
б) | |||||
|
N (шт./мм2) |
13008,0±1377,3 |
11984,2±750,9 |
3083,1±480,6 |
9358,1±869,5 | |
|
d (мкм) |
4,99±0,2 |
7,88±0,3 |
3,43±0,3 |
4,65±0,9 | |
|
D (мкм) |
8,2±0,4 |
11,2±0,5 |
9,4±0,4 |
9,3±0,4 | |
|
S (мкм2) |
26,9±2,2 |
18,2±1,0 |
16,4±1,3 |
22,3±1,5 | |
|
V (усл. ед.) |
9446149,4±1011320,4 |
13882017,9±1864021,5 |
1554544,8±479897,2 |
8294240,7±1118412,6 | |
|
R (усл. ед.) |
0,0049±0,0003 |
0,0052±0,0002 |
0,0102±0,0005 |
0,0067±0,0003 | |
|
в) | |||||
|
N (шт./мм2) |
10235,2±352,0 |
12500,0±1125,3 |
5781,2±1345,8 |
9505,3±2821,4 | |
|
d (мкм) |
5,6±0,2 |
9,6±0,5 |
5,32±0,3 |
6,3±0,3 | |
|
D (мкм) |
9,2±0,4 |
11,0±0,7 |
9,74±0,5 |
9,6±0,5 | |
|
S (мкм2) |
24,0±1,7 |
25,8±1,4 |
27,8±1,3 |
25,8±1,4 | |
|
V (усл. ед.) |
8546024,3±901241,4 |
17695125,0±2430582,4 |
4521129,6±622225,1 |
10254093,0±1318016,3 | |
|
R (усл. ед.) |
0,0056±0,0001 |
0,0050±0,0003 |
0,007±0,0009 |
0,0058±0,0004 | |
|
г) | |||||
|
N (шт./мм2) |
7812,1±656,8 |
12296,7±573,4 |
9375,8±650,1 |
9827,6±661,1 | |
|
d (мкм) |
3,3±0,1 |
5,5±0,2 |
5,2±0,2 |
4,3±0,1 | |
|
D (мкм) |
13,9±0,6 |
14,3±0,6 |
13,2±0,6 |
13,3±0,6 | |
|
S (мкм2) |
27,3±1,1 |
26,5±0,5 |
18,8±1,2 |
23,6±0,8 | |
|
V (усл. ед.) |
3812617,2±512221,0 |
10068414,8±1281164,5 |
7276562,0±928712,4 |
7052533,3±523115,6 | |
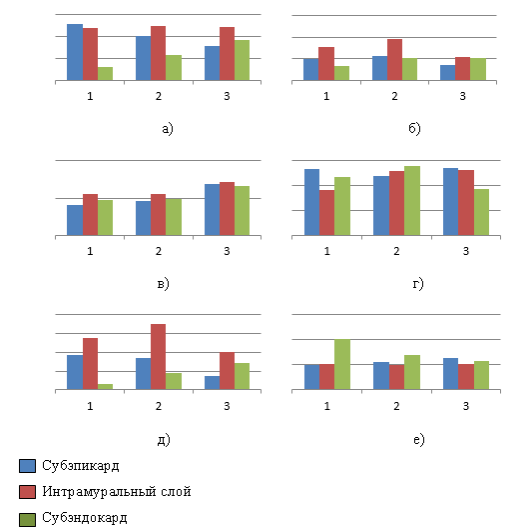
Рис. 1.а)Количество функционирующих капилляров (N), б) Диаметр капилляров (d), в) Диаметр КМЦ (D), г) Площадь ядер КМЦ (S), д) Объем капиллярного русла (V), е) Радиус диффузии (R). В трех слоях миокарда: 1 — ишемической зоны, 2 — зоны геморрагического пояса, 3 — зоны реактивных изменений
Данные морфометрического изучения капиллярной сети и КМЦ различных слоев миокарда представлены в таблице 1.
Светооптическое микроскопическое исследование миокарда показало в опыте выраженные морфологические изменения КМЦ. Отмечены явления нарушения кровообращения: мелкоточечные диапедезные экстравазаты, межуточный отек, стаз в капиллярном звене МЦР, умеренное венозное полнокровие. По результатам морфометрического анализа интактной (контрольной) группы отмечено, что диаметр КМЦ по слоям сердечной мышцы статистически не различается (таб. 1а). Наименьшая площадь ядер отмечена в субэндокарде. Капиллярная сеть более развита в среднем слое, в нем же наблюдался наибольший диаметр капилляров. В среднем слое миокарда низкий уровень диффузии и наибольший объем капиллярного русла, наименьший — в субэпикардиальном слое. Во внутреннем слое самый высокий радиус диффузии.
В центре ишемизированной области определялись спавшиеся капилляры. По периферии ишемического очага отмечались перерастянутые и заполненные кровью микрососуды. Морфометрическое исследование зоны ишемии по данным таблицы 1б свидетельствует об уменьшении диаметра и площади ядер КМЦ всех слоев миокарда по сравнению с контрольной группой. Наиболее выраженное снижение диаметра КМЦ под эпикардом и под эндокардом. Значительно уменьшилась площадь ядер в среднем слое — на 53,6 %. Исследование капиллярной сети указывает на увеличение количества функционирующих капилляров под эпикардом — на 23,5 % и в интрамуральном слое — на 6,9 %, уменьшение их в субэндокарде — на 46,6 %. Увеличение диаметра капилляров зафиксировано под эпикардом, а в интрамуральном и субэндокардиальном слоях — его уменьшение. Объем капиллярного русла увеличивался в наружном слое на 80 %, уменьшался в интрамуральном на 90 % и субэндокарде — на 30 %. Отмечалось нарастание радиуса диффузии от эпикарда к эндокарду по сравнению с контролем.
Зона образовавшегося геморрагического пояса во всех слоях выглядела полиморфно: очаги дистрофии чередовались с участками умеренного отека стромы и резко расширенными капиллярами с явлениями стаза. Диаметр КМЦ (таб. 1в) во всех слоях снижался, площадь ядер возросла в субэндокарде — на 22 % и уменьшилась в субэпикарде и интрамуральном слое на 35 %. Во всех слоях незначительно увеличилось число функционирующих капилляров и их диаметр. Объем капиллярного русла возрастал от внутреннего слоя к наружному, соответственно на 9 %, 15 %, 158 %. Радиус диффузии умеренно снижен во всех слоях.
В более удаленной реактивной зоне (таб.1г) зафиксировано умеренное уменьшение диаметра КМЦ. Площадь ядер уменьшалась в наружном и среднем слое, возрастала на 37 % во внутреннем слое. Количество функционирующих капилляров увеличилось в интрамуральном слое, диаметр микрососудов умеренно снижен во всех слоях. Объем капиллярного русла снизился в интрамуральном слое и возрос под эндокардом. Значимых различий радиуса диффузии по сравнению с контролем не отмечено.
Обсуждение.
В условиях ишемической гипоксии изменяется строение капиллярной сети и происходит нарушение транспортно — трофических процессов в миокарде. Быстрая перестройка микроциркуляторной системы, происходящая за счет расширения просвета сосудов, приводит к укорочению пути диффузии от капилляров к КМЦ. Общий механизм изменений микроциркуляции заключается в недостаточном заполнении кровью обменных сосудов, возникновении ацидоза вследствие появления недоокисленных продуктов, которые в свою очередь вызывают расширение микрососудов. На периферии ишемизированной зоны миокарда в большинстве препаратов отмечалось паралитическое расширение капилляров, особенно венул, в их просвете — агрегаты эритроцитов. Заполненные кровью капилляры способны поддерживать некоторое время жизнеспособность КМЦ. В отличии от других органов, в сердце артериолы непосредственно переходят в капилляры, чем объясняется отсутствие прекапиллярных сфинктеров. Ряд авторов отмечают наличие венуло-венулярных анастомозов в субэпикардиальном слое, множество мостиков между капиллярами во всех слоях сердечной мышцы и отсутствие артериоло-венулярных анастомозов [2]. В субэндокарде было отмечено наименьшее количество функционирующих капилляров, но имеющих широкий просвет, что связано с поддержанием метаболизма внутреннего слоя миокарда за счет диффузии субстратов из крови полостей сердца. Значительный радиус диффузии данного слоя свидетельствует о высокой проницаемости стенок капилляров, что необходимо при максимальном сдавлении субэндокарда в период систолы. Радиус диффузии также отражает процесс поступления энергетических субстратов в наиболее отдаленные зоны ФЭМ.
Ядра КМЦ внутреннего слоя миокарда наиболее мелкие, в данном участке прослеживается обратная зависимость между радиусом диффузии капилляров и площадью ядер. В более поздние сроки поврежденные КМЦ уменьшаются в диаметре из — за повышения мембранной проницаемости, нарастают явления периваскулярного отека и происходит сужение сосудов МЦР [3]. По результатам исследования возможно установить зависимость морфологических изменений от характера инфаркта миокарда. В литературе встречаются данные о прямой зависимости между величиной объемной плотности МЦР и характером инфаркта, так, трансмуральный инфаркт чаще возникает в сердце с относительно низким удельным объемом интрамурального русла, а наиболее высокие объемные показатели МЦР обнаружены в сердце людей со средним типом венечного кровоснабжения [4]. Малый объем артериального русла является предпосылкой для возникновения нарушения кровотока в пораженном миокарде. Необходимо также отметить, что для обеспечения транскапиллярного обмена большое значение имеет исходное состояние просвета сосудов, которое зависит от возраста, функциональной нагрузки на сердце, индивидуальных особенностей ангиоархитектоники.
Нечеткая граница между нормальной и ишемизированной тканями, определяется разной чувствительностью КМЦ к ишемии и особенностями капиллярного русла. Капилляры всех слоев миокарда располагаются параллельно КМЦ. Изменения миокарда отмечаются не только в участке, снабжаемым кровью из пораженного сосуда, но и в отдаленном миокарде, где было уменьшение диаметра капилляров и увеличение капиллярного русла. В дальнейшем эти участки будут компенсировать функцию сердечной мышцы и влиять на прогноз болезни. Большое количество анастомозов обеспечивает поступление крови в зону ишемии, что приводит к ее уменьшению. Резкое снижение АТФ в клетках после 30 минут ишемии приводит к необратимым изменениям, гибель КМЦ происходит постепенно от центра к периферии, и в зависимости от степени снижения кровотока может происходить и более продолжительное время [5].
Резкие изменения МЦР приводят к нарушению гемодинамики и реологических свойств крови, возникает стаз и агрегация эритроцитов, в конечном счёте приводящие к микротромбозу капилляров, возникают локальные участки ишемии. В ранее проведенных исследованиях указано, что у 26 % внезапно погибших больных тромбы локализовались в капиллярах сердца [6].
Заключение.
Изучение количественных и морфометрических показателей МЦР и КМЦ в различных зонах инфаркта позволяет судить характере и распространенности патологического процесса. Для зоны ишемии характерно уменьшение числа и диаметра капилляров, снижение радиуса диффузии (в субэндокардиальном и интрамуральном слое). Наиболее выраженное снижение диаметра ядер КМЦ характерно для субэпикарда и субэндокарда, вследствие мембранной проницаемости. Периферия ишемии и зона геморрагического венчика выглядит во всех слоях полиморфно, гибель клеток происходит постепенно, что служит предпосылкой для проведения терапии, направленной на ограничение поражения при инфаркте миокарда. Увеличение количества функционирующих капилляров, их диаметра и объема капиллярного русла в субэпикардиальном и субэндокардиальном слоях сердечной мышцы неишемизированной зоны носит компенсаторно-адаптационный характер.
Литература:
- Розенберг В. Д. Изменения сосудистого русла при дилятационной и гипертрофической кардиомиопатии // Кардиология. — 1989. — № 11. — С. 116–120.
- Богданович Н. К., Жучкова Н. И. Изучение микроциркуляторного русла миокарда человека при внезапной сердечной смерти // Арх. пат. — 1988. — № 8. — С. 33–35.
- Василенко В. Т. Возможный подход к оценке энергетической мощности митохондрий при морфологических исследованиях // Бюл. экспер. биол. и мед. — 1985. — № 9. — С. 361–363.
- Автандилов Г. Г. Гевондян Т. А. Стереометрическое исследование системы «мышечное волокно — капилляр» сердца человека в функциональном аспекте // Арх. анат. — 1980. – № 7. — С. 33–37.
- Чернышенко Н. М., Котляров В. С. Модель гемомикроциркуляторного модуля // Арх. анат. — 1986. — № 4. — С. 9–13.
- Бураковский В. И., Сапрыгин Д. Б. Биохимическая оценка повреждений миокарда человека при полной ишемии во время оперативных вмешательств на сердце / М.: медицина, 1981. — С. 336–345.

