Цитостатики на основе циансодержащих гетероциклов
Авторы: Давыдова Вера Владимировна, Данилова Мария Валерьевна, Марьясов Максим Андреевич, Шевердов Владимир Петрович, Насакин Олег Евгеньевич
Рубрика: 9. Биологическая химия
Опубликовано в
II международная научная конференция «Современная химия: Успехи и достижения» (Чита, апрель 2016)
Дата публикации: 06.04.2016
Статья просмотрена: 129 раз
Библиографическое описание:
Цитостатики на основе циансодержащих гетероциклов / В. В. Давыдова, М. В. Данилова, М. А. Марьясов [и др.]. — Текст : непосредственный // Современная химия: Успехи и достижения : материалы II Междунар. науч. конф. (г. Чита, апрель 2016 г.). — Чита : Издательство Молодой ученый, 2016. — С. 45-47. — URL: https://moluch.ru/conf/chem/archive/162/10217/ (дата обращения: 20.09.2024).
Рак остается одной из наиболее серьезных заболеваний человечества. Онкологические заболевания являются одной из основных причин смерти во всем мире. По прогнозам, число случаев смерти от онкологических заболеваний в мире будет продолжать расти и в 2030 году достигнет 12 миллионов случаев смерти. В связи с этим, синтез новых соединений и создание на их основе противоопухолевых препаратов, обладающих улучшенными фармакокинетическими свойствами, является актуальной задачей.
Несмотря на появление новых противоопухолевых лекарств, их клиническая эффективность недостаточна, а спектр онкологических заболеваний, чувствительных к химиотерапии, ограничен. В связи с этим не теряет актуальности вопрос поиска новых химических соединений с противоопухолевыми свойствами как основы для последующей разработки более эффективных лекарств. Основными критериями для отбора новых соединений являются: уникальность химической структуры, новый механизм действия, избирательная цитотоксичность, высокая противоопухолевая активность invivo, доступность для производства.
Наземные растения были использованы в качестве лекарственных средств в Египте, Китае, Индии и Греции с древнейших времен и большое количество современных препаратов, разработано с ними в наше время. Первые письменные упоминания о целебных возможностях использования растений появились примерно в 2600 г. до н. э. у шумеров и Аккадцев (Самуэльсон, 1999). В «Папирусе Эберса», самым известным египетским фармацевтическим справочнике, в котором зафиксировано более 700 препаратов, представляет собой историю египетской медицины датированный около 1500 г. до н. э.
Определенное место в этих рецептурах занимали растения, содержащие цианогенные глюкозиды. Цианогенные гликозиды — это группа нитрилсодержащих растительных вторичных соединений, которые выделяют цианид (цианогенез) после их ферментативного расщепления. Хотя есть много природных источников цианида, в том числе растения, бактерии и грибы. Цианогенные глюкозиды были зарегистрированы в более чем 2650 видах высших растений, распределенных среди 130 семейств. Самым известным цианогенным глюкозидом является амигдалин. Он был впервые выделен в 1830 году французскими химиками и использовался в качестве противоракового средства в России уже в 1845 г. Первое использование амигдалина в Соединенных Штатах для лечения рака произошло в начале 1920-х годов.
Выделение алкалоидов барвинка — винбластина и винкристина представила новую эру использования растительных материалов. Эти алкалоиды содержат гидроксильные, метоксильные, метоксикарбонильные функциональные группы. Представляются актуальными также работы по синтезу и исследованию свойств куркумина, колхицина и производных, содержащих эти фрагменты. Ранее было установлено, что синтезированные нами полицианозамещенные карбо- и гетероциклы обладают противоопухолевыми свойствами.
Обзор литературы позволяет прогнозировать высокую противоопухолевую активность соединений, содержащих гидроксильные, метоксильные, метоксикарбонильные и циано-группы. Для их синтеза мы использовали тетрацианоэтилен, малононитрил, метил 2,4-диоксобутаноаты, альдегиды.
Метил-6-амино-3-ацил-4-арил-5-циано-4Н-пиран-2-карбоксилаты I получены реакциями 2-арилиденмалононитрилов с метил 2,4-диоксобутаноатами. Синтез 9-арил-12-имино-10,11-диоксатрицикло [5.3.2.01,6]додекан-7,8,8-трикарбонитрилов IIосуществлен из тетрацианоэтилированного аддукта циклогексанона и альдегидов по известной методике. Реакциями тетрацианоэтилированных аддуктов циклогексанона и циклогептанона с гидробензамидами получены 1,2-дигидропиридин-3,3,4,4-тетракарбонитрилы III.
2,5-Бис-(3,4,5-триметоксифенил)пирролидин-3,3,4,4-тетракарбонитрил IVполучен путем взаимодействия 1,1,2,2-тетрацианоэтана с N,N′-бис(4-метоксибензилиден)-1-(4-метоксифенил)метандиамином.


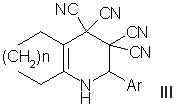

I: Ar = 3,4,5-(MeO)3C6H2 (a, b, c), 4-MeOOCC6H4 (d), 2-F-6-ClC6H3 (e); R = Me (a), 2-Fu (b), 3,4-(MeO)2C6H3 (c), 4-BrC6H4 (d), 3,4-(MeO)2C6H3 (e).
II: Ar = 3,4,5-(MeO)3C6H2 (a), 3-MeO-4-HOC6H3 (b), 4-MeOOCC6H4 (c), 4-(CH3)2NC6H4 (d).
III: n = 2 (a, b), 3 (c); Ar = 4-MeOC6H4 (a), 2-Thienyl (b, c).
Антипролиферативная активность цианозамещенных соединений I-IVисследована в Национальном институте рака (США). Для исследований использовали модель invitro, позволяющую стандартизовать условия эксперимента для повторяющихся серий. Исследования проведены на 60 клеточных линиях, полученных из опухолей легких, толстой кишки, мозга, яичников, почек, предстательной железы, молочной железы, а также лейкемии и меланомы человека. Обнаружено, что из исследованных на противоопухолевую активность веществ 2-(4-метоксифенил)-1,2,5,6,7,8-тетрагидрохинолин-3,3,4,4-тетракарбонитрилы IIIа,b является наиболее перспективным для дальнейших исследований (таблица 1). При концентрации 10–5 М это соединение оказывает значительное ингибирование роста опухолевых клеток. Получены следующие результаты:
Таблица 1
Результаты исследования антипролиферативной активности соединений при концентрации 10–5M*
|
Соединение |
Культура клеток / ингибирование,% |
||||||||
|
лейкоза |
рака легких |
рака толстой кишки |
рака мозга |
Меланомы |
рака яичников |
рака почек |
рака простаты |
рака молочной железы |
|
|
Ia |
- |
NCI-H522/ 14.19 |
- |
SNB-75/ 14.9 |
SK-MEL-2/ 11.36 |
- |
- |
- |
- |
|
Ib |
- |
- |
- |
SNB-75/ 19.3 |
- |
- |
CAKI-1/ 13.0 UO-31/ 11.3 |
- |
- |
|
Ic |
- |
A549/ATCC/ 12.65 HOP-92/ 11.8 NCI-H522/ 19.07 |
- |
- |
- |
- |
UO-31/ 11.2 |
- |
- |
|
Id |
- |
A549/ATCC/ 14.74 NCI-H522/ 17.93 |
- |
- |
UACC-257/ 12.06 |
- |
TK-10/ 15.9 UO-31/ 14.4 |
- |
- |
|
Ie |
- |
NCI-H23/ 12.23 NCI-H522/ 16.33 |
- |
SNB-75/ 11.0 |
- |
- |
A49/ 14.4 |
- |
- |
|
IIa |
SR/ 37.09 |
NCI-226/ 13.24 |
- |
SNB-75/ 18.6 |
UACC-62/ 15.50 |
- |
UO-31/ 14.8 |
- |
MDA-MB-231/ATCC/ 11.24 MDA-MB-468/ 22.50 |
|
IIb |
SR/ 25.02 |
NCI-H226/ 13.54 NCI-H522 / 12.05 |
- |
SNB-75/ 11.3 |
- |
- |
UO-31/ 18.3 |
- |
MDA-MB-468/ 18.21 |
|
IIc |
SR/ 13.45 |
NCI-H522/ 13.91 |
- |
- |
LOX IMVI/ 13.74 UACC-257/ 11.36 UACC-62/ 12.21 |
- |
- |
- |
MCF7/ 15.43 MDA-MB-468/ 15.38 |
|
IId |
SR/ 13.12 |
A549/ATCC/ 10.02 NCI-H522/ 13.76 |
- |
- |
UACC-257/ 17.73 |
- |
- |
- |
MCF7/ 10.93 |
|
IIIa |
CCRF-CEM/ 92.62 HL-60(TB)/ 58.67 K-562/ 87.50 MOLT-4/ 90.71 RPMI-8226 / 20.10 SR/ 98.88 |
EKVX/ 11.77 NCI-H522 / 76.19 |
COLO 205/ 88.21 HCT-116/ 21.25 HCT-15/ 34.07 HT29 / 20.07 SW-620/ 51.84 |
SNB-19/ 11.5 SNB-75/ 11.4 |
MALME-3M / 28.35 UACC-62/ 24.58 |
OVCAR-3/ 57.04 |
786–0/ 11.9 ACHN/ 62.87 CAKI-1/ 21.97 SN1C/ 11.30 TK-10 / 20.31 UO-31/ 24.25 |
- |
MCF7/ 50.13 MDA-MB-231/ ATCC/ 29.88 T47D / 50.80 MDA-MB-468 / 42.05 |
|
IIIb |
CCRF-CEM / 53.73 HL-60(TB) / 39.35 K-562 / 34.90 MOLT-4 / 54.37 SR/ 86.42 |
A549/ATCC / 11.53 EKVX / 11.70 NCI-H522 / 64.27 |
COLO 205 / 35.53 HCT-116 / 15.04 HCT-15 / 25.11 SW-620 / 48.60 |
- |
LOX IMVI / 12.54 UACC-257 / 15.26 UACC-62/ 12.12 |
OVCAR-3 / 40.54 |
ACHN / 62.25 CAKI-1/ 10.78 TK-10 / 15.32 UO-31 / 37.90 |
- |
MCF7/ 21.74 T47D/ 31.00 MDA-MB-468/ 17.79 |
|
IIIc |
- |
NCI-H522/ 10.63 |
HCT-116/ 11.45 |
SNB-75/ 44.6 |
- |
- |
UO-31 / 19.09 |
PC-3/ 10.58 |
MCF7 / 15.19 HS 578T/ 10.05 MDA-MB-468/ 19.84 |
|
IV |
HL-60(TB)/ 10.61 |
- |
- |
SNB-76/ 19.3 |
SK-MEL-5/ 10.47 |
- |
UO-31 / 16.25 |
- |
HS 578T/ 10.84 |
|
бусульфан |
- |
- |
- |
- |
M14/ 18.80 |
- |
- |
- |
- |
|
цисплатин |
- |
HOP-92/ 35.80 NCI-H522/ 28.40 |
- |
SNB-75/ 13.90 |
MALME-3M/ 15.80 SK-MEL-2/ 12.60 |
IGROV1/ 26.90 |
CAKI-1/ 17.40 UO-31 / 18.80 |
DU-145/ 19.90 |
BT-549 / 10.90 |
*указаны результаты при ингибировании роста >10 %
Результаты исследований показывают, что 2-R-1,2,5.6,7,8-тетрагидрохинолин-3,3,4,4-тетракарбонитрилы IIIa,b наиболее активены по отношению к лейкемии, они ингибирует рост всех известных клеточных линий. Таким образом, 2-(4-метоксифенил)-1,2,5.6,7,8-тетрагидрохинолин-3,3,4,4-тетракарбонитрил при концентрации 10–5М намного более активен по сравнению с известными противоопухолевыми препаратами, такими как бусульфан и цисплатин. Среднее значение ингибирования клеточных линий лейкемии составляет 59.31 %, а максимальное 98.88 %.
Полученные результаты подтверждают нашу гипотезу о том, что этил-1,1,2,2-тетракарбонитрильный фрагмент в циклических соединениях является фармакофором.
Работа выполнена при поддержке гранта РНФ № 15–13–10029.
Похожие статьи
Современные возможности диагностики фиброзно-кистозной...
Поводом для обращения послужили симптомы, вызвавшие у женщин подозрение на болезни молочных желез для установления диагноза.
Достоинство маммографии: высокая информативность (чувствительность до 95 %, специфичность до 97 %), возможность...
Мамоклам в лечении мастопатии, как профилактика рака...
Доброкачественные заболевания молочных желез (МЖ) — самая распространенная женская патология.
- Факторы внешней среды: высокий социально-экономический статус; воздействие ионизирующей радиации и химических канцерогенов; избыток алкоголя, жиров, калорий...
Психологические особенности отношения к жизни онкологических...
Женщины с диагнозом рака молочной железы III ст. в возрасте от 27 до 35 лет. Выборка являлась однородной, все участницы в процессе лечения пережили предоперационное лечение, далее операцию по удалению молочной железы...
Актуальные проблемы диагностики и лечения...
Актуальные проблемы диагностики и лечения инфильтративно-отечной формы рака молочной железы с метастазами в кости.
Для сцинтиграфии скелета использовался РФП — технефор-99м Tc, обладающий высокой тропностью к костной ткани.
Роль акушерки смотрового кабинета в раннем выявлении...
III международная научная конференция «Новые задачи современной медицины» (Санкт-Петербург, декабрь 2014).
Согласно мировой статистике первое место среди онкологических заболеваний у женщин занимает рак молочной железы — 16 % всех случаев рака.
Использование способности железа вызывать угнетение...
Гемосидерин является нерастворимым агрегатом железа с высоким отношением железа к белку».
Ясно видно, что железо, воздействуя на клетки, вызывает угнетение их жизнедеятельности, путем угнетения метаболизма и митотической активности.
Онкологическая ситуация в Оренбургской области
Оренбургская область, молочная железа, I-II, показатель, заболевание, своевременность взятия, высокая смертность, онкологический процесс, предстательная железа, этап развития.
Онтогенетические перестройки синтеза и секреции...
В то же время в тех же пробах выявляются высокая активность протеаз- трипсина и химотрипсин, т. е. существует «не параллелизм»
Основные термины (генерируются автоматически): поджелудочная железа, рождение, дефинитивное питание, молочное...
Оценка качества жизни и частоты встречаемости побочных...
Наиболее высокий средний уровень АЛТ был зарегистрирован при режимах СMF (2,96±0,16 ммоль/л), EFC (2,78±0,10 ммоль/л) и СС (2,40±0,13 ммоль/л).
Качество жизни больных раком молочной железы и раком яичников (EORTC - QLQ - C 30).
Похожие статьи
Современные возможности диагностики фиброзно-кистозной...
Поводом для обращения послужили симптомы, вызвавшие у женщин подозрение на болезни молочных желез для установления диагноза.
Достоинство маммографии: высокая информативность (чувствительность до 95 %, специфичность до 97 %), возможность...
Мамоклам в лечении мастопатии, как профилактика рака...
Доброкачественные заболевания молочных желез (МЖ) — самая распространенная женская патология.
- Факторы внешней среды: высокий социально-экономический статус; воздействие ионизирующей радиации и химических канцерогенов; избыток алкоголя, жиров, калорий...
Психологические особенности отношения к жизни онкологических...
Женщины с диагнозом рака молочной железы III ст. в возрасте от 27 до 35 лет. Выборка являлась однородной, все участницы в процессе лечения пережили предоперационное лечение, далее операцию по удалению молочной железы...
Актуальные проблемы диагностики и лечения...
Актуальные проблемы диагностики и лечения инфильтративно-отечной формы рака молочной железы с метастазами в кости.
Для сцинтиграфии скелета использовался РФП — технефор-99м Tc, обладающий высокой тропностью к костной ткани.
Роль акушерки смотрового кабинета в раннем выявлении...
III международная научная конференция «Новые задачи современной медицины» (Санкт-Петербург, декабрь 2014).
Согласно мировой статистике первое место среди онкологических заболеваний у женщин занимает рак молочной железы — 16 % всех случаев рака.
Использование способности железа вызывать угнетение...
Гемосидерин является нерастворимым агрегатом железа с высоким отношением железа к белку».
Ясно видно, что железо, воздействуя на клетки, вызывает угнетение их жизнедеятельности, путем угнетения метаболизма и митотической активности.
Онкологическая ситуация в Оренбургской области
Оренбургская область, молочная железа, I-II, показатель, заболевание, своевременность взятия, высокая смертность, онкологический процесс, предстательная железа, этап развития.
Онтогенетические перестройки синтеза и секреции...
В то же время в тех же пробах выявляются высокая активность протеаз- трипсина и химотрипсин, т. е. существует «не параллелизм»
Основные термины (генерируются автоматически): поджелудочная железа, рождение, дефинитивное питание, молочное...
Оценка качества жизни и частоты встречаемости побочных...
Наиболее высокий средний уровень АЛТ был зарегистрирован при режимах СMF (2,96±0,16 ммоль/л), EFC (2,78±0,10 ммоль/л) и СС (2,40±0,13 ммоль/л).
Качество жизни больных раком молочной железы и раком яичников (EORTC - QLQ - C 30).











