Актуальность: быстрый темп развития компьютерных технологий в медицине и новейших методов обследования пациентов позволяет нам в кратчайшие сроки установить диагноз послеоперационных осложнений. Одним из таких осложнений является послеоперационный панкреатит.
В большинстве случаев послеоперационный панкреатит развивается в первые 3–4 суток после операции. Частота данного осложнения после лапаротомий составляет 0,7–25,6 %, а при операциях на поджелудочной железе возрастает до 32,7–50 % (Б. И. Альперович 1991 г., Р. В. Вашетко с соавт.) [1].
Клиника послеоперационного панкреатита вариабельна, каких-либо патогномоничных симптомов не имеет. Этим объясняется постоянный поиск новых, информативных методов распознавания его [2].
Выявление гомеостазиологических нарушений, их коррекция, своевременная релапаротомия предопределяют исход заболевания больных послеоперационным панкреатитом и являются актуальными проблемами [3].
Летальность при послеоперационном панкреатите остается высокой — 24,5 %, а при деструктивных формах достигает 50–60 % и не имеет тенденции к снижению (Р. В. Вашетко).
Цель исследования: оптимизировать алгоритм диагностики, лечения послеоперационного панкреатита и определить оптимальные сроки релапаротомии для снижения летальности.
Задачи:
- изучить частоту развития панкреатита после операции на органах брюшной полости,
- выявить частоту клинико-лабораторных проявлений послеоперационного панкреатита,
- определить значимость неинвазивных и малоинвазивных методов диагностики послеоперационного панкреатита,
- определить необходимость и оптимальные сроки релапаротомии,
- разработать эффективные способы санации брюшной полости.
Материалы и методы. Мы проанализировали результаты лечения 6689 больных оперированных в военном госпитале г. Алматы с 1982 по 2012 гг. по поводу заболеваний и травм органов брюшной полости.
Операции были проведены на следующих органах: поджелудочной железе — 253(10 случаев послеоперационного панкреатита — 4 %), желудке и двенадцатиперстной кишке — 1268 (24 случая — 1,9 %), билиарном дереве — 3152 (28 случаев — 0,9 %), печени — 1231 (3 случая — 0,2 %), селезенке и прочих органах — 785 (6 случаев — 0,8 %) (см. Диаграмма 1).
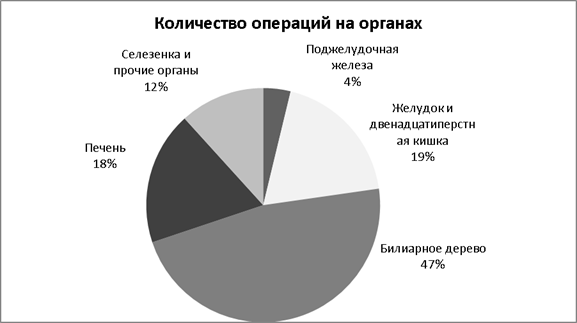
Рис. 1.
Послеоперационный панкреатит развился у 71 больного (1,1 %). Мужчин — 59 (83 %), женщин — 12 (17 %). Возраст больных колеблется в пределах от 25 до 74 лет.
Клинически, лабораторно и УЗИ-подтвержденный послеоперационный панкреатит возник на 3–4 сутки, только у 8 человек на 7–8 сутки. Клиническая картина его характеризовалась скудностью и непостоянством симптоматики.
Частыми клиническими проявлениями были: боль в верхних отделах живота — 68 (95,8 %); тахикардия — 64 (90 %); парез кишечника, не поддающийся лечению — 52 (73,2 %); рвота — 47 (66,2 %); гипертермия — 38 (53,5 %); напряженный мышечный дефанс в эпигастрии — 33 (46,5 %); иктеричность кожи — 28 (39,4 %); положительный симптом Щеткина-Блюмберга — 25 (35,2 %); коллапс — 12 (16,9 %); психоз — 12 (16,9 %); икота — 10 (14 %) (см. Диаграмма 2).
В общем анализе крови отмечался выраженный лейкоцитоз в 62 (81,3 %) случаях, сдвиг лейкоцитарной формулы влево в 30 (42,3 %) случаях, токсическая зернистость лейкоцитов в 22 (31 %) случаях. Биохимический анализ крови показал гипербилирубинемию за счет прямой фракции у 25 (35 %) пациентов, повышение уровня АЛТ и АСТ у 21 (30 %), гипергликемию у 15 (21 %) и повышение амилазы у 32 (45 %) пациентов. Диастазурия имелась в 35 (49 %) случаях, но только у 23 (32 %) больных достигла значительных цифр.
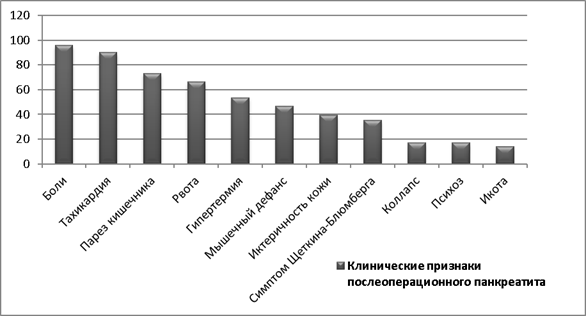
Рис. 2.
Вышеперечисленный симптомокомплекс показывает глубину гомеостатических нарушений и не является патогномоничным для данного осложнения. Для облегчения постановки диагноза, мы выделили основные симптомы, такие как: боли в верхних отделах живота, выраженный парез кишечника, тахикардия, гипертермия. Значительную роль в диагностике сыграла диастазурия и использование специальных методов исследования. При рентгенологическом обследовании у 32 (45 %) больных выявлены косвенные признаки панкреатита: вздутие поперечно-ободочной кишки, левосторонний реактивный плеврит, симптом «дежурной кишки», симптом «вырезанной кишки», симптом «отсеченной ободочной кишки». Ультразвуковое исследование позволяет выявить увеличение размеров, размытость контуров поджелудочной железы, наличие выпота в сальниковой сумке. После операции на органах верхнего отдела брюшной полости не всегда удается визуализировать поджелудочную железу: из 68 обследованных больных ценная информация получена у 41. Наиболее информативными являются компьютерная томография и диагностическая видеолапароскопия.
В клинике мы начинаем лечение с функционального покоя поджелудочной железы: декомпрессии желудка, локальной гипотермии, парентерального, а в последние годы и энтерального питание. Проводим коррекцию нарушений гемостаза, детоксикацию, улучшение реологии крови, купирование проявлений синдрома системного воспалительного ответа. Широко используем управляемую гемодилюцию с форсированным диурезом [4].
Особое значение мы придаем мероприятиям по блокированию повреждающего воздействия ферментативного токсического экссудата, играющего важную роль на ранних стадиях тяжелого послеоперационного панкреатита и применению различных методик выведения токсических компонентов из тканевых депо.
При проведении курса интенсивной консервативной терапии у 49 (69 %) из 71 больных отмечалось субъективное и объективное улучшение состояния через 36–48 часов от начала лечения: купировались признаки интоксикации, нормализовались показатели крови и диастазы.
В 22 (31 %) случаях консервативное лечение не имело эффекта. Прогрессивное ухудшение состояния пациентов, нарастание симптомов ферментной токсемии, появление признаков перитонита явились показанием к релапаротомии. 16 пациентов взяты на операцию с диагнозом послеоперационный панкреатит. У 6 больных был выставлен диагноз: высокая тонкокишечная непроходимость (4), недостаточность швов анастомоза (2).
Релапаротомии произведены в следующие сроки с момента появления симптомов осложнения: через 6–24 часов — у 9 больных, на 2–4 сутки — у 12, на 5 сутки — у 1 (см. Диаграмма 3). При релапаротомии диагностированы жировой панкреонекроз у 14, геморрагический панкреонекроз у 8 больных. Перитонит диагностирован в 19 случаях (86,4 %).
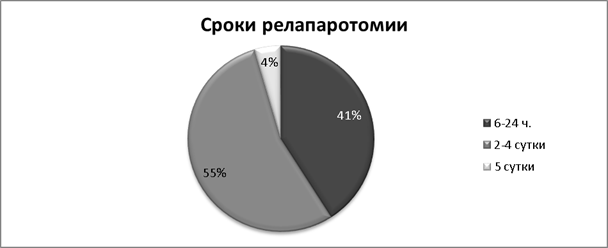
Рис. 3.
Во время операции по поводу тяжелого послеоперационного панкреатита хирург должен решить несколько проблем. Наиболее сложной и ответственной является выбор рациональной хирургической тактики.
У 12 больных после релапаротомии проводилась программированная видеолапароскопическая санация брюшной полости по нашей методике с использованием специального лапаропорта (патент № 19772 от 28.05.2008г.). Лапаропорт устанавливали и фиксировали на передней брюшной стенке. Через него выполнялась ревизия и санация брюшной полости эндохирургической стойкой фирмы «Карл Шторц». После окончания лечения лапаропорт удаляли, а фиксирующие его нити завязывали, закрывая дефект передней брюшной стенки [5].
Больные получали внутриаортальную инфузию лекарственных средств, антибиотикотерапию, управляемую гемодилюцию с форсированным диурезом. На фоне послеоперационного тяжелого течения с явлениями интоксикации, пареза кишечника у 10 (45,4 %) больных развились осложнения: у 5 (22,7 %) пневмония, у 3 (13,6 %) плеврит, у 2 (9,1 %) флегмона брюшной стенки. Двое (9,1 %) повторно 2 раза оперированы по поводу спаечной кишечной непроходимости и абсцессов брюшной полости. Проводилась иммунокоррегирующая и иммунозаместительная терапия. При анемии переливали свежецитратную кровь. Применяли анаболические гормоны и пиримидиновые производные, антистафилококковую плазму, антистафилококковый гамма-глобулин.
Умерло 6 больных, что составило 8,4 % от всех случаев послеоперационного панкреатита и 27,2 % после релапаротомий. У 5 на вскрытии геморрагический панкреонекроз, у 1 — жировой с распространением некротического процесса на забрюшинную клетчатку. Причиной летального исхода явилось у 5 больных прогрессирование панкреонекроза, у 1 профузное кровотечение из магистральных артериальных сосудов.
Выводы:
1. Доминирующими клиническими проявлениями послеоперационного панкреатита явились болевой синдром, выраженный парез кишечника, тахикардия, гипертермия;
2. Для ранней диагностики и коррекции лечения информативными оказались неинвазивные методы мониторирования — рентгенологическое, ультразвуковое исследования, компьютерная томография, клинико-лабораторные данные;
3. Неэффективность консервативной терапии в течении суток должна явиться показанием для релапаротомии;
4. Операция должна быть минимальной по объему;
5. Применение лапароскопического мониторирования позволило своевременно санировать и купировать прогрессирование послеоперационного панкреатита.
Литература:
1. Басенов Л. Н. Неотложная хирургия груди и живота. Руководство для врачей. СПб, Гиппократ, 2002 г.
2. Макаренко Г. П. Ведение больных общехирургического профиля в послеоперационном периоде, 1989 г.
3. Клиническая хирургия: Национальное руководство, 3 т. (редакция Савельев В. С., Карпенко А. И., Гальперин Э. И., Милонов О. Б.) — Медиа, 2002г., том — 2.
4. Неотложная хирургия органов брюшной полости (клиническое руководство) под редакцией Кондратенко П. Г., Русина В. И. Донецк, 2013 г.
5. Ибадильдин А. С.. Хирургические болезни. Алматы, 2010.

