В статье приведены результаты количественного изменения доли В-лимфоцитов в общей популяции лимфоцитов, уровня иммуноглобулинов A (IgA), IgE, IgG, IgM в периферической крови 4 групп исследуемых групп: 21 некурящий пациент с ХОБЛ, 20 курящих пациентов с ХОБЛ, 20 некурящих здоровых людей и 21 здоровый курильщик. Полученные данные свидетельствуют о патогенетическом значении IgA, IgE и IgG при ХОБЛ.
Ключевые слова: хроническая обструктивная болезнь легких, иммуноглобулины, индекс курения, IgA, IgE.
Хроническая обструктивная болезнь легких (ХОБЛ) представляет серьезную проблему как социального, так и экономического характера. Сегодня ХОБЛ занимает четвертое место среди причин смерти в мире, причём к 2030 году прогнозируется перемещение ХОБЛ как причины смерти на третье место. В мире насчитывается порядка 3 млн больных ХОБЛ, в Беларуси данная цифра — до 60 тыс. человек. В Европейском союзе общие прямые затраты на лечение ХОБЛ достигают 38,6 млрд. евро.
К факторам риска развития ХОБЛ:
- Тяжёлые респираторные инфекции в детском возрасте или же частые инфекции дыхательных путей в зрелом возрасте;
- Курение (однако, результаты обследований населения в разных странах мира показали, что до 68.6 % пациентов, страдающих ХОБЛ, никогда не курили [1, с. 22; 3, с. 735]). Известно, что 53.5 % ХОБЛ-пациентов в Беларуси не являются курильщиками.
- Вдыхание дыма биоорганического топлива;
- Производственная пыль и химикаты;
- Перенесенный туберкулёз;
- Бронхиальная астма.
ХОБЛ — болезнь, трудно поддающейся лечению, что делает актуальным изучение патогенеза этого заболевания. Несмотря на тот факт, что в изучении Т-клеточного иммунного ответа при ХОБЛ достигнуты значительные успехи, по сей день мало изученным является состояние гуморального иммунитета у некурящих пациентов при ХОБЛ.
Как уже известно, в реализации гуморального ответа участвуют АПК, Т-хелперы, В-лимфоциты, В-клетки памяти, плазмоциты, система комплемента, цитокины и иммуноглобулины. АПК поглощают АГ и презентируют их на своей поверхности в составе молекулы ГКГ II класса. Посредством связывания с этими молекулами активируются Т-хелперы, и те начинают активно секретировать воспалительные цитокины (ИЛ-1,2,6,8,12,ФНО,g-интерферон). В результате происходит последовательная активация, пролиферация и бласттрансформация В-клеток в плазматические клетки. Данные клетки выделяют антитела, способные специфически связаться с исходным АГ. Образовавшийся комплекс АТ-АГ фагоцитируется и элиминируется макрофагами.Кроме антител, плазматические клетки выделяют иммуноглобулины — иммунные белки, различающиеся по строению и аминокислотному составу тяжёлых цепей и по выполняемым эффекторным функциям.
Для выделения В-клеток используется определение В-клеточного рецепторного комплекса (BCR), в состав которого входит CD20 — интегральный негликозилированный белок, участвующий в активации и пролиферации данных клеток. Данный белок присутствует на всех В-клетках, но отсутствует на плазматических клетках [2, с. 108].
Целью данного исследования явилось определение патогенетической значимости показателей гуморального иммунитета в прогрессировании хронической обструктивной болезни лёгких. Для этого были предложены следующие задачи:
- Сформировать группы исследуемых людей (курящие/некурящие здоровые/пациенты с ХОБЛ),
- Определить доли В-лимфоцитов в общей популяции лимфоцитов крови у испытуемых,
- Оценить концентрации иммуноглобулинов А, Е, G, M в плазме крови у изучаемых выборок,
- Выполнить статистическую обработку и оценить различия результатов между исследуемыми группами.
Материал и методы
Обследованы 21 некурящий пациент с ХОБЛ, 20 курящих пациентов с ХОБЛ, 20 некурящих здоровых людей и 21 здоровый курильщик. Необходимо отметить, что к некурящим мы относили людей, которые выкурили менее 100 сигарет за жизнь.
Критерием включения в исследование были следующие тезисы: возраст старше 40 лет, соответствие критериям GOLD 2011, отсутствие симптомов обострения ХОБЛ в течение последних 2 месяцев до взятия крови. Из данного исследования исключались пациенты с наличием в анамнезе бронхиальной астмы, атопии, аллергического ринита, принимавшие системные глюкокортикостероиды как минимум за 2 месяца до настоящего исследования, пациенты, неспособные правильно выполнить дыхательный маневр при тестировании функции внешнего дыхания.
Анализ популяций лимфоцитов проводили на 5-канальном проточномцитометреCytomicsFC500 с использованием программного обеспечения CXP («BeckmanCoulter», США). Для каждой пробы учитывали не менее 50 000 клеток.
По показателям прямого (FSC) и бокового (SSC) светорассеивания выделяли регион лимфоцитов. В пределах этого региона по маркеру СD20 рассчитывали процент В-клеток в общей популяции лимфоцитов.
У всех пациентов также определяли уровень IgA, IgE, IgG, IgM («Вектор-Бест», Российская Федерация) в плазме крови методом иммуноферментного анализа на иммуноферментом анализаторе «StatFax 3200» («AwarenessTechnology», США).
Статистическую обработку проводили с помощью пакета прикладных программ Statistica 8.0. Для всех имеющихся выборок данных проверяли гипотезу нормальности распределения по критерию Колмогорова-Смирнова. Поскольку полученные нами данные не подчинялись нормальному распределению, анализ проводили методами непараметрической статистики. Рассчитывались медиана и интерквартильный размах. Для сравнения данных между группами использовался U-критерий Манна-Уитни. Оценка взаимосвязи двух исследуемых групп проводилась вычислением коэффициента корреляции по Спирмену (SpearmanR). Достоверными считались различия при уровне значимости p менее 0,05.
Результаты и обсуждение
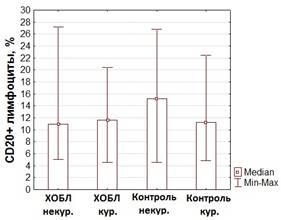
Рис. 1. Доля CD20+ лимфоцитов периферической крови у пациентов с ХОБЛ
В результате проведенного исследования не удалось зафиксировать статистически значимых отличий процента В-клеток среди всех исследуемых групп.
Концентрация IgA повышалась в плазме крови курящих пациентов с ХОБЛ по сравнению со здоровыми курящими людьми. Уровень IgA также повышался у некурящих пациентов с ХОБЛ по сравнению с некурящими людьми без ХОБЛ.
Исследование общего IgЕ в плазме крови выявило достоверное увеличение концентрации этого показателя в группе курящих пациентов с ХОБЛ по сравнению с курящими здоровыми людьми.
При проведении корреляционного анализа у курящих пациентов с ХОБЛ обнаружена положительная корреляционная связь средней силы между уровнем общего IgЕ в плазме крови и индексом курения. Напомним, что индекс курящего человека (ИКЧ) — основной показатель, используемый для расчёта частоты табакокурения, и рассчитываемый как стаж курения (годы)*количество выкуренных сигарет в день/20.
Наличие обнаруженной взаимосвязи предполагает, что у курящих пациентов с ХОБЛ с увеличением стажа и интенсивности курения происходит нарастание в крови уровня общего IgE. Это косвенно указывает на то, что у пациентов с ХОБЛ курение усиливает секрецию IgE плазматическими клетками [4, с. 383].
По данным нашей работы, уровень IgG был выше у курящих пациентов с ХОБЛ, чем у здоровых курящих людей. У некурящих пациентов подобные изменения этого иммуноглобулина отсутствовали.
Как показали полученные нами результаты, различия уровня IgM отсутствовали как в группе курящих, так и в группе некурящих пациентов с ХОБЛ по сравнению с соответствующими группами здоровых людей.
Таблица 1
Концентрация иммуноглобулинов в плазме крови курящих и некурящих пациентов с ХОБЛ
|
Некурящие |
Курящие | |||
|
Цитокин |
ХОБЛ |
Контроль |
ХОБЛ |
Контроль |
|
IgA, мг/мл |
2,3 (1,7–3,8)* |
1,6 (1,3–2,2) |
2,4 (1,7–2,8)# |
1,8 (1,6–2,0) |
|
IgE, ME/мл |
560,0 (285,0–740,0)* |
257,5 (175,0–535,0) |
490,0 (285,0–940,0)# |
285,0 (245,0–420,0) |
|
IgG, мг/мл |
16,3 (14,5–19,5) |
15,8 (13,1–18,3) |
16,9 (13,8 –20,6)# |
12,5 (10,5–16,0) |
|
IgM, мг/мл |
1,5(1,3–1,9) |
1,4 (0,8–2,1) |
1,3 (0,9–2,2) |
1,0 (1,0–1,6) |
Примечание: данные представлены как медиана (25 % — 75 %); * — p< 0,05 по сравнению со здоровыми некурящими людьми; # — p< 0,05 по сравнению со здоровыми курящими людьми.
Заключение
Проведенное исследование позволило выявить неоднозначный характер изменения показателей гуморального иммунитета в периферической крови пациентов с ХОБЛ:
- независимо от фактора курения повышена концентрация IgA и IgE;
- только у курящих больных имеет место более высокий уровень IgG;
- ни ХОБЛ, ни курение не сопровождаются каким-либо сдвигом уровня IgM и доли В-лимфоцитов;
- у курящих пациентов с ХОБЛ установлена положительная корреляционная связь средней силы между уровнем общего IgЕ в плазме крови и индексом курения, что косвенно указывает на то, что у пациентов с ХОБЛ курение усиливает секрецию IgE плазматическими клетками.
Литература:
1. Кадушкин, А. Г. Эпидемиологические особенности хронической обструктивной болезни легких у городских жителей Республики Беларусь / А. Г. Кадушкин, А. Д. Таганович, И. М. Лаптева // Здравоохранение. — 2013. –№ 7. — С. 21–25.
2. Хайдуков, С. В. Цитометрический анализ в клинической иммунологии / С. В. Хайдуков, А. В. Зурочка, В. А. Черешев– Екатеринбург: УрО РАН, 2011. –220 с.
3. Salvi, S. S.Chronic obstructive pulmonary disease in non-smokers / S. S. Salvi, P. J. Barnes // –Lancet–2009. –№ 374. — P. 733–743.
4. Inflammatory cells and mediators in bronchial lavage of patients with chronic obstructive pulmonary disease / A. Pesci [et al.] // Eur. Respir. J. — 1998. — Vol. 12. — P. 380–386.

