Введение. Болезнь Паркинсона (БП) — это прогрессирующее нейродегенеративное нарушение, характеризующееся потерей дофаминергических нейронов в черной субстанции и приводящее к моторным и немоторным симптомам. Патофизиология БП включает сложное взаимодействие генетических, экологических и биохимических факторов, включая накопление агрегатов альфа-синуклеина, митохондриальную дисфункцию, окислительный стресс и нейровоспаление.Современное фармакологическое лечение в первую очередь направлено на облегчение симптомов, при этом леводопа (LD) является «золотым стандартом» в контроле моторных симптомов. Кроме того, для модуляции и улучшения допаминергической и холинергической передачи применяются ингибиторы фермента ДОПА-декарбоксилазы (DDC), дофаминовые агонисты (DA), ингибиторы моноаминоксидазы В (MAO-B), ингибиторы катехол-О-метилтрансферазы (COMT) и центрально действующие антихолинергические средства. Несмотря на эти достижения, эффективность существующей терапии снижается со временем, сопровождаясь тяжелыми побочными эффектами, что подчеркивает необходимость разработки новых терапевтических подходов [1].
Причина болезни Паркинсона чаще всего идиопатическая (с неизвестной точной причиной), однако доказано, что генетические факторы увеличивают риск развития заболевания у некоторых пациентов. Генетические исследования вносят важный вклад в понимание патогенеза БП [2].
В период с 1990 по 2021 годы нагрузка от болезни Паркинсона (БП) значительно возросла: в 2021 году количество новых случаев заболевания (incidence) во всем мире достигло примерно 13,35 миллионов, что существенно выше показателей 1990 года. Кроме того, число смертей, связанных с БП, превысило 388 тысяч, а показатель DALYs (утраченные годы жизни с поправкой на инвалидность) оставался на высоком уровне [3].
Интенсивный рост глобальной заболеваемости БП наблюдался в 1990–2021 годах: incidence увеличился на 220 %, смертность — на 77 %, а показатель DALYs также существенно возрос. Эта тенденция связана с ростом стареющего населения и демографическими изменениями [3].
Нагрузка БП различается по полу: число заболевших мужчин выше, чем женщин (males > females), что является фактором значительного увеличения тяжести заболевания [3].
В Азии наблюдаются высокие показатели распространенности болезни Паркинсона (БП): в период с 1990 по 2021 годы incidence БП в Азии увеличился на 198 %, prevalence — на 284 %, смертность (mortality) — на 111 %, а показатель DALYs — на 144 %. Эти данные указывают на высокий темп роста БП в странах Азии.
Нагрузка значительно различается, при этом количество случаев среди мужчин всегда выше, а основными причинами этого являются старение населения и демографические изменения [4].
Недавние исследования показывают тенденцию к росту нагрузки БП в странах Центральной Азии. В этом регионе повседневные экологические факторы и социально-экономические различия рассматриваются как важные аспекты, влияющие на динамику развития заболевания [5].
Цель исследования: Проанализировать особенности лекарственной терапии болезни Паркинсона в разных странах, используемые препараты и их клиническую эффективность.
Материалы и методы: Внастоящем исследовании проведён систематический анализ научной литературы, посвящённой фармакотерапии болезни Паркинсона. Поиск публикаций осуществлялся в международных базах данных PubMed, MEDLINE и EMBASE, а также в ведущих рецензируемых клинических журналах.
В анализ включались исследования, посвящённые современным подходам к лечению болезни Паркинсона, с акцентом на основные фармакологические стратегии, включая применение леводопы, дофаминовых агонистов и ингибиторов моноаминоксидазы типа B (MAO-B).
Критериями включения являлись:
— оригинальные исследования, систематические обзоры и метаанализы;
— публикации на английском языке;
— доступность полного текста;
— соответствие тематике фармакотерапии болезни Паркинсона.
Критерии исключения включали:
— дублирующие публикации;
— статьи с недостаточной методологической обоснованностью;
— исследования, не относящиеся к фармакологическому лечению.
Поисковая стратегия включала использование следующих ключевых слов и их комбинаций: Parkinson’s disease , treatment , pharmacotherapy , levodopa , dopamine agonists , MAO-B inhibitors .
Всего было проанализировано 45 научных публикаций, из которых 19 индексированы в базе данных PubMed и опубликованы в авторитетных журналах по неврологии и клинической фармакологии.
Для систематизации данных статьи были распределены по следующим тематическим группам:
— терапия леводопой — 8 публикаций;
— лечение дофаминовыми агонистами — 6 публикаций;
— применение ингибиторов MAO-B — 3 публикаций;
— сравнительные клинические исследования (леводопа vs другие методы терапии) — 2 публикаций.
Результаты: Во многих клинических исследованиях оценивались моторные и немоторные симптомы БП с использованием шкал UPDRS (Unified Parkinson’s Disease Rating Scale), времени «on/off», частоты дискинезий, а также переносимости терапии в общей популяции пациентов. Результаты продемонстрировали, что хотя леводопа остаётся наименее спорным и наиболее эффективным средством для контроля моторных симптомов, другие классы препаратов играют важную роль в комплексной терапии, особенно на ранних стадиях заболевания или для уменьшения побочных эффектов лечения [6].
L-DOPA (L-дигидроксифенилаланин) является наиболее эффективным антипаркинсоническим средством для облегчения симптомов болезнь Паркинсона. Однако её нейротоксический потенциал и механизмы образования дофамина (DA) остаются недостаточно изученными, особенно с учётом того, что целевые структуры базальных ганглиев могут быть лишены дофаминергической иннервации.В данном обзоре обобщаются ключевые аспекты и современные достижения в этой области. На основании данных терапии L-DOPA показано, что в экспериментальных моделях болезни Паркинсона у животных L-DOPA проявляет нейропротективные, а не нейротоксические свойства. В частности, установлено, что применение L-DOPA не увеличивает уровень реактивных форм кислорода, в стриатальной ткани, а также не изменяет его внеклеточную концентрацию, измеренную методом in vivo микродиализа. Кроме того, антипаркинсонический эффект L-DOPA, вероятно, усиливается в условиях выраженной дофаминергической денервации базальных ганглиев. Данные in vivo микродиализных исследований демонстрируют, что внеклеточные уровни дофамина в денервированном стриатуме значительно выше, чем в интактной ткани. Это объясняется отсутствием дофаминовых транспортеров в дегенерировавших нервных окончаниях, что приводит к снижению обратного захвата дофамина. Соответственно, количество механизмов, обеспечивающих удаление дофамина из внеклеточного пространства, существенно уменьшается. Клинические исследования также подтверждают, что терапия леводопой обеспечивает значительное улучшение моторной функции пациентов с БП по шкале UPDRS (Unified Parkinson’s Disease Rating Scale), особенно в первые годы лечения, и позитивно влияет на качество жизни пациентов. Кроме того, комбинации леводопы с периферическими ингибиторами ДОПА‑декарбоксилазы (например, карбидопа или бенсеразид) повышают эффективность терапии и уменьшают побочные эффекты, связанные с периферическим метаболизмом леводопы. Одним из значимых побочных эффектов длительной терапии L-DOPA являются моторные дискинезии. Предполагается, что их развитие связано с повышенной чувствительностью дофаминовых рецепторов (D1–D5). Данный эффект может быть воспроизведён в экспериментальных условиях при многократном введении агонистов дофамина, особенно агонистов D2-класса, даже при отсутствии денервации дофаминергической системы. Современные исследования также указывают на то, что L-DOPA стимулирует высвобождение нейротрофического фактора мозга (BDNF) из кортикостриарных проекций, что, в свою очередь, приводит к усилению экспрессии D3-рецепторов. Этот механизм, вероятно, играет важную роль в развитии L-DOPA-индуцированных дискинезий. При этом антагонисты D3-рецепторов способны подавлять данный эффект. Таким образом, новые данные о механизмах действия L-DOPA углубляют понимание её фармакологических эффектов и открывают перспективы для оптимизации терапии, направленной на усиление её клинической эффективности и снижение выраженности побочных эффектов [7].
Леводопа остаётся наиболее эффективным средством симптоматического лечения болезнь Паркинсона, обеспечивая выраженное улучшение моторных функций. Тем не менее, длительное применение леводопы ассоциировано с развитием моторных осложнений, включая дискинезии и флуктуации эффекта, что обусловливает необходимость использования дополнительных фармакологических стратегий. В этом контексте Агонисты дофамина занимают важное место в современной терапии. В отличие от леводопы, они непосредственно стимулируют дофаминовые рецепторы, минуя этап метаболического превращения в дофамин. Данный механизм обеспечивает более стабильную стимуляцию дофаминергических структур и снижает зависимость эффекта от сохранности пресинаптических нейронов. Агонисты дофамина применяются как в виде монотерапии на ранних стадиях заболевания, так и в составе комбинированной терапии с леводопой. Назначение этих препаратов на ранних этапах позволяет отсрочить развитие леводопа-индуцированных осложнений, хотя их эффективность в режиме монотерапии ограничена и уступает леводопе по степени выраженности клинического ответа. Согласно данным современных сетевых мета-анализов, агонисты дофамина достоверно превосходят плацебо как при монотерапии, так и при комбинированном применении с леводопой, обеспечивая улучшение моторных симптомов и снижение частоты моторных осложнений. Среди препаратов данной группы высокую клиническую эффективность продемонстрировали Прамипексол, Ропинирол и Ротиготин. Сравнительные исследования показывают, что применение агонистов дофамина, особенно на ранних стадиях заболевания, связано с более низким риском развития дискинезий и моторных флуктуаций по сравнению с монотерапией леводопой. Однако леводопа сохраняет статус «золотого стандарта» лечения благодаря более выраженному и устойчивому влиянию на моторные проявления заболевания. Комбинированная терапия леводопой и агонистами дофамина имеет особое значение у пациентов с феноменом «изнашивания дозы» (wearing-off), характеризующимся сокращением продолжительности действия леводопы. Добавление агонистов дофамина в таких случаях способствует снижению выраженности моторных флуктуаций, удлинению периода «on» и улучшению качества жизни пациентов. Несмотря на различия в фармакокинетических и фармакодинамических характеристиках, производные эргота, такие как Бромокриптин, Лизурид и Перголид, демонстрируют сопоставимую клиническую эффективность. Парентеральное применение Апоморфин позволяет реализовать непрерывную дофаминергическую стимуляцию и эффективно контролировать выраженные моторные флуктуации на поздних стадиях заболевания. Дополнительно обсуждается потенциальная способность агонистов дофамина снижать оксидативный стресс, связанный с метаболизмом дофамина, что теоретически может замедлять прогрессирование заболевания. Однако на сегодняшний день убедительные клинические доказательства их нейропротективного эффекта отсутствуют. Таким образом, агонисты дофамина являются важным компонентом фармакотерапии болезни Паркинсона, позволяя оптимизировать лечение, уменьшить выраженность моторных осложнений и повысить качество жизни пациентов, особенно при рациональном использовании в составе комбинированной терапии. Болезнь Паркинсона представляет собой прогрессирующее нейродегенеративное заболевание, характеризующееся дефицитом дофамина в центральной нервной системе. Основные терапевтические стратегии направлены на восполнение дофаминергической активности и включают применение Леводопа, ингибиторов метаболизма дофамина (ингибиторы моноаминоксидазы B и катехол-O-метилтрансферазы), а также агонистов дофаминовых рецепторов. Ингибиторы МАО‑B реализуют свой эффект путём селективного подавления фермента моноаминоксидазы типа B, ответственного за деградацию дофамина в центральной нервной системе, что приводит к увеличению его биодоступности и уменьшению выраженности симптомов заболевания [8].
К числу наиболее изученных представителей данного класса относятся Селегилин, Разагилин и Сафинамид. Особый интерес представляет разагилин — селективный и необратимый ингибитор МАО-B из группы пропаргиламинов. В отличие от селегилина, он не метаболизируется с образованием потенциально токсичных амфетаминоподобных метаболитов, что определяет его более благоприятный профиль безопасности. Фармакокинетические характеристики разагилина включают пероральную биодоступность около 35 %, достижение максимальной концентрации в плазме крови через 0,5–1 час и период полувыведения в пределах 1,5–3,5 часов. Препарат подвергается интенсивному печёночному метаболизму с участием изофермента CYP1A2. Разагилин применяется в дозе 1 мг один раз в сутки в качестве монотерапии на ранних стадиях заболевания и в дозе 0,5–1 мг в сутки — в составе комбинированной терапии с леводопой у пациентов с более продвинутыми стадиями болезни. Важно отметить, что терапия разагилином не ассоциируется с развитием так называемого «сырного эффекта» (тираминового синдрома), а дозы до 20 мг в сутки демонстрируют хорошую переносимость. Однако у пациентов с нарушением функции печени требуется коррекция дозы. Разагилин противопоказан к применению в сочетании с другими ингибиторами МАО, а также требует осторожности при совместном назначении с рядом антидепрессантов и опиоидных препаратов. Согласно данным клинических обзоров, ингибиторы МАО-B обладают благоприятным профилем безопасности и умеренной клинической эффективностью. При применении в качестве монотерапии на ранних стадиях заболевания они обеспечивают статистически значимое, хотя и умеренное улучшение моторных функций, а также способны отсрочить необходимость назначения леводопы. В составе комбинированной терапии с леводопой ингибиторы МАО-B способствуют значительному сокращению продолжительности «off»-периодов и улучшению моторной стабильности, что делает их важным компонентом лечения пациентов с прогрессирующим течением заболевания и моторными флуктуациями. Дополнительно обсуждается потенциальная нейропротективная роль ингибиторов МАО-B, обусловленная снижением оксидативного стресса, связанного с метаболизмом дофамина. Тем не менее, несмотря на обнадеживающие экспериментальные данные, убедительные клинические доказательства данного эффекта на сегодняшний день остаются ограниченными и требуют дальнейших исследований. Таким образом, ингибиторы МАО-B представляют собой важный класс препаратов в терапии болезни Паркинсона, обеспечивая как симптоматическое улучшение, так и возможность оптимизации комбинированного лечения, направленного на повышение качества жизни пациентов. Болезнь Паркинсона остаётся прогрессирующим нейродегенеративным заболеванием, при котором Леводопа сохраняет статус наиболее эффективного симптоматического средства [9].
Одним из подходов к повышению её эффективности является ингибирование периферического и центрального метаболизма дофамина, в частности за счёт подавления фермента катехол-O-метилтрансферазы (КОМТ). Ингибиторы КОМТ увеличивают биодоступность леводопы, пролонгируют её действие и способствуют более стабильной дофаминергической стимуляции. Среди препаратов данной группы особое место занимает Толкапон — мощный и селективный ингибитор КОМТ. Применение толкапона в клинической практике длительное время было ограничено из-за риска гепатотоксичности. Однако современные данные свидетельствуют о том, что при условии регулярного мониторинга функции печени его переносимость сопоставима с другими доступными методами терапии. При этом использование толкапона ассоциируется с выраженным клиническим улучшением, включая не только моторные, но и немоторные симптомы заболевания. Фармакологическое обоснование применения толкапона заключается в его способности ингибировать КОМТ как в периферических тканях, так и в центральной нервной системе, в отличие от некоторых других представителей класса. Это обеспечивает более значительное увеличение концентрации леводопы в плазме и головном мозге, а также уменьшение вариабельности её фармакокинетического профиля. Клинические исследования показывают, что добавление толкапона к терапии леводопой приводит к значительному сокращению продолжительности «off»-периодов и увеличению времени «on», сопровождающегося адекватным контролем симптомов. В сравнении с другими стратегиями коррекции моторных флуктуаций (включая применение Энтакапон и ингибиторов МАО-B), толкапон демонстрирует более выраженный и стабильный эффект у части пациентов. Особое значение толкапон может иметь у пациентов, сохраняющих выраженные моторные флуктуации несмотря на комбинированную терапию с использованием энтакапона и/или ингибиторов МАО-B. В таких случаях предлагается рассматривать пробное назначение толкапона как следующий этап фармакологической оптимизации лечения. Кроме того, в современных подходах к ведению пациентов с болезнью Паркинсона подчёркивается целесообразность рассмотрения толкапона до перехода к более инвазивным методам лечения, таким как хирургические вмешательства или инфузионные терапии, направленные на обеспечение непрерывной дофаминергической стимуляции. Таким образом, несмотря на ранее существовавшие ограничения, толкапон представляет собой эффективный компонент комбинированной терапии болезни Паркинсона. При надлежащем контроле безопасности он может значительно улучшать клиническое состояние пациентов, снижать выраженность моторных флуктуаций и расширять возможности индивидуализированного подхода к лечению [10].
Установлено что комбинированная фармакотерапия является одним из наиболее эффективных подходов к лечению болезни Паркинсона на различных стадиях заболевания. Результаты крупного рандомизированного исследования PD-MED показали, что монотерапия леводопой обеспечивает выраженный контроль моторных симптомов, однако в долгосрочной перспективе её комбинация с другими лекарственными средствами способствует повышению стабильности клинического эффекта и улучшению качества жизни пациентов. Кроме того, комбинированная терапия позволяет снизить выраженность моторных флуктуаций Согласно данным мета-анализов, добавление дофаминовых агонистов к леводопе приводит к значительному сокращению периода «off-time» и улучшению моторных функций. При этом уменьшается потребность в высоких дозах леводопы, что способствует снижению риска развития леводопа-индуцированных дискинезий. Комбинированное применение ингибиторов моноаминоксидазы B (MAO-B), таких как селегилин, разагилин и сафинамид, с леводопой также продемонстрировало высокую эффективность. Данные препараты замедляют метаболизм дофамина, способствуя увеличению продолжительности «on-time» и улучшению моторной стабильности. При этом они характеризуются благоприятным профилем переносимости и относительно низкой частотой побочных эффектов. Использование ингибиторов катехол-О-метилтрансферазы (КОМТ) в сочетании с леводопой направлено на продление её фармакологического действия. Исследования показывают, что данная комбинация снижает выраженность феномена «wearing-off» и обеспечивает более стабильную дофаминергическую стимуляцию, что приводит к улучшению двигательной активности пациентов. В целом, основным преимуществом комбинированной терапии является её способность оказывать комплексное воздействие на дофаминергическую систему за счёт различных механизмов действия препаратов. Это позволяет эффективно контролировать моторные симптомы, уменьшать выраженность феномена «on/off» и повышать эффективность длительного лечения. Вместе с тем, применение нескольких лекарственных средств одновременно может сопровождаться увеличением риска развития побочных эффектов, включая ортостатическую гипотензию, психические расстройства и нарушения сна. В связи с этим выбор комбинированной терапии должен осуществляться индивидуально с учётом клинических особенностей пациента. Таким образом, результаты анализа литературы свидетельствуют о том, что комбинированные схемы терапии обладают более высокой эффективностью по сравнению с монотерапией, особенно на поздних стадиях заболевания, и являются одной из ключевых стратегий лечения болезни Паркинсона [11]. Леводопа подтверждена как фундаментальный препарат в контроле моторных симптомов болезни Паркинсона и улучшении качества жизни пациентов на всех стадиях заболевания; её эффективность подтверждена в крупных клинических исследованиях. Дофаминовые агонисты являются эффективной терапевтической опцией, особенно на ранних стадиях БП, с более низким риском моторных осложнений, однако уступают леводопе по силе действия при выраженных симптомах. MAO‑B ингибиторы обеспечивают умеренное улучшение моторных функций и эффективны как добавочная терапия к леводопе, снижая период «off»‑времени и улучшая стабильность двигательных характеристик. Комбинированные схемы терапии демонстрируют лучшие клинические результаты, чем монотерапия, что делает их предпочтительными для длительного поддерживающего лечения пациентов с прогрессирующим течением БП [11].
Общие принципы фармакотерапии: Основное направление медикаментозного лечения при болезни Паркинсона (БП) — коррекция дефицита дофамина и облегчение моторных симптомов. Для достижения этой цели применяются: Леводопа (L-DOPA) —Леводопа является предшественником дофамина и способна проникать через гематоэнцефалический барьер, где под действием фермента ароматической L‑аминокислотной декарбоксилазы превращается в дофамин. Повышение уровня дофамина в стриатуме способствует уменьшению гипокинезии, ригидности мышц и тремора у пациентов с Болезнь Паркинсона Леводопа обычно откладывается до более поздних стадий или до выраженного проявления симптомов, что может отсрочить появление моторных флуктуаций [12].
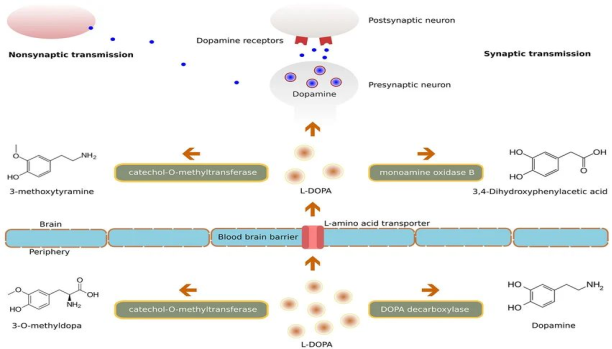
Рис. 1. Схема демонстрирует ключевые этапы фармакокинетики и фармакодинамики леводопы, а также основные ферментативные пути её метаболизма в периферии и центральной нервной системе
Агонисты допаминовых рецепторов (DA) — Агонисты дофаминовых рецепторов — это препараты, которые напрямую стимулируют дофаминовые рецепторы (преимущественно D2). Они компенсируют дефицит дофамина при Болезнь Паркинсона и улучшают двигательные функции (уменьшают брадикинезию и ригидность). Основные представители: Прамипексол, Ропинирол, Бромокриптин.Побочные эффекты: тошнота, гипотензия, сонливость, галлюцинации. Часто применяются вместе с Леводопа [13].
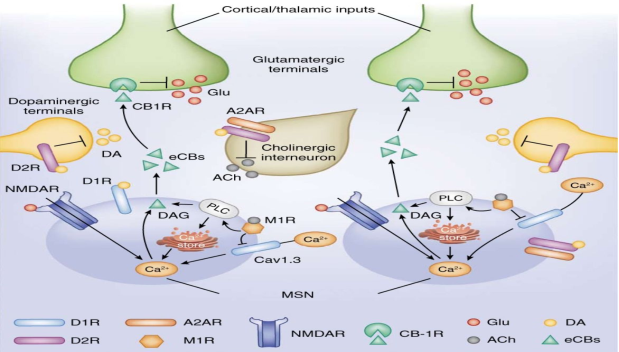
Рис. 2. Схема иллюстрирует интегративную синаптическую регуляцию активности средних шипиковых нейронов (MSN) полосатого тела за счёт взаимодействия кортикоталамических глутаматергических, дофаминергических и холинергических входов с участием рецепторов D1/D2, NMDA, M1 и A2A, эндоканнабиноидной системы (CB1R) и внутриклеточных каскадов PLC–DAG–Ca²⁺ (включая Cav1.3), определяющих возбудимость нейрона
Ингибиторы MAO-B (селегилин, разагилин) —Ингибиторы MAO‑B, такие как Селегилин и Разагилин, предотвращают распад дофамина в мозге, повышая его концентрацию и облегчая моторные симптомы при Болезнь Паркинсона. Препараты принимаются внутрь, хорошо всасываются и чаще всего применяются на ранних стадиях монотерапией или в комбинации с Леводопа. Побочные эффекты: тошнота, сонливость, головокружение; взаимодействие с тирамином из пищи минимальное [13].
Ингибиторы КOMT (энтакапон, толкапон) —Ингибиторы КОМТ, такие как Энтакапон и Толкапон, подавляют периферический метаболизм L‑DOPA, повышая концентрацию дофамина в мозге. Они дополняют терапию L‑DOPA при Болезнь Паркинсона, сокращают «off»-фазы и облегчают моторные симптомы. Энтакапон эффективен только в комбинации с L‑DOPA, тогда как толкапон метаболизируется в печени и требует контроля функции печени. Побочные эффекты: тошнота, диарея, изменения артериального давления [14].
Американские клинические руководства при лечении БП придают особое значение фармакотерапии: На ранних стадиях заболевания рекомендуется начинать лечение с DA или ингибиторов MAO-B, а затем добавлять леводопу, особенно у молодых пациентов, чтобы уменьшить моторную токсичность. Согласно рекомендациям Американской академии неврологии (AAN), имеются подробные указания по применению селегилина и других дофаминергических препаратов в зависимости от клинических проявлений БП [8]. В США решение о терапии выбирается на основе возраста пациента, сопутствующих заболеваний и тяжести моторных симптомов [9]. В европейской практике лечение болезни Паркинсона (БП) в основном опирается на международные рекомендации и индивидуализированные фармакологические стратегии, где: Леводопа играет ведущую роль, особенно при средних и тяжелых симптомах. Агонисты допаминовых рецепторов и ингибиторы MAO-B часто применяются на ранних стадиях, особенно у пожилых пациентов, с целью снижения моторной токсичности. Дополнительные препараты (ингибиторы COMT) играют вспомогательную роль в контроле моторных флуктуаций. В Европе стратегии медикаментозного лечения динамически адаптируются под конкретного пациента с учетом возраста, характера симптомов и возможных побочных эффектов [9]. Например, в Великобритании экспертные руководства NICE рассматривают леводопу как стартовую и основную терапию, тогда как в Германии и Франции часто практикуется начальное применение дофаминовых агонистов (DA). В Китае существуют национальные рекомендации по лечению болезни Паркинсона (БП), которые широко применяются китайскими клиницистами: Исследование, проведённое в Пекине, показало, что леводопа и её комбинации (например, леводопа + бензеразид или леводопа + карбидопа) являются наиболее назначаемыми препаратами для терапии БП. Кроме того, агонисты допаминовых рецепторов (DA), такие как прамипексол и пирифедил, также широко применяются, особенно у молодых пациентов в качестве стартовой терапии. В Китае использование DA в начальной терапии более популярно, тогда как леводопа обычно рекомендуется как препарат первой линии для пациентов старше 65 лет. Эти подходы также связаны с политикой общественного здравоохранения и системой медицинского страхования [15]. Глобальные фармакоэпидемиологические данные свидетельствуют о высокой доступности леводопа для лечения болезнь Паркинсона (до 99 % стран), в то время как доступ к другим противопаркинсоническим препаратам существенно варьирует в зависимости от уровня экономического развития стран. Как показано в табл. 1, подходы к лечению болезни Паркинсона варьируют: в США применяется индивидуализированная терапия, в Европе — поэтапная с отсрочкой леводопы у молодых пациентов, в Азии — комбинированная стратегия, тогда как в странах с низким и средним доходом основным препаратом остаётся леводопа из-за её доступности.
В странах с высоким уровнем дохода, помимо леводопы, широко представлены дофаминовые агонисты, ингибиторы катехол-O-метилтрансферазы (КОМТ) и ингибиторы моноаминоксидазы типа B (MAO-B), что обеспечивает возможность проведения комплексной и индивидуализированной терапии. Напротив, в странах с низким и средним уровнем дохода доступность альтернативных лекарственных средств остается ограниченной, что сужает терапевтические возможности и может негативно влиять на качество лечения и исходы заболевания [16].
Как представлено в табл. 2, рекомендации по началу лечения болезни Паркинсона основываются на возрасте пациента и предполагают более щадящие стратегии с использованием ингибиторов MAO-B и дофаминовых агонистов у молодых пациентов, тогда как с увеличением возраста приоритет смещается в сторону раннего назначения леводопы с последующей коррекцией терапии в зависимости от клинического ответа.
Таблица 1
Сравнительные особенности лечения по странам
|
Страна/Регион |
Основной препарат |
Дополнительные препараты |
Особенности |
|
США |
Леводопа, DA, ингибиторы MAO-B |
Ингибиторы COMT |
Используются руководства AAN, терапия часто индивидуализируется под конкретного пациента |
|
Европа |
На ранних стадиях предпочтение отдается ингибиторам МАО-В и DA; леводопа применяется при нарастании симптомов |
Ингибиторы КОМТ, амантадин, DA |
Подход основан на поэтапной стратегии лечения в соответствии с NICE EFNS/MDS, с возможной отсрочкой назначения леводопы у молодых пациентов |
|
Китай/Азия |
Комбинированная терапия с использованием леводопы; у молодых пациентов часто инициируют лечение с DA |
Прамипексол, ропинирол, ингибиторы МАО-В |
Региональные рекомендации ориентированы на раннее применение DA и адаптацию терапии к возрасту пациента |
|
Страны с низким/средним доходом |
Леводопа как основной препарат первой линии |
Иногда доступны MAO-B/DA |
Терапевтическая стратегия определяется доступностью лекарственных средств; леводопа остаётся наиболее широко применяемым препаратом |
Таблица 2
Рекомендации по началу лечения болезни Паркинсона в зависимости от возраста
|
Возраст пациента |
Начало лечения |
Коррекция при недостаточной эффективности |
Последующая коррекция |
|
До 50 лет |
Ингибитор MAO-B (при лёгких двигательных нарушениях), агонист допаминового рецептора (при умеренных двигательных нарушениях) |
Переход на комбинацию ингибитора MAO-B и АДР. Добавление амантадина. Замена АДР. При треморе в покое — добавление антихолинергических препаратов |
Добавьте малые дозы леводопы (100–200 мг в сутки) |
|
50–70 лет |
Леводопа как наиболее эффективная терапия; при лёгких симптомах — ингибиторы МАО-В или агонисты дофаминовых рецепторов |
Добавление агонистов дофаминовых рецепторов или переход на комбинированную терапию; при прогрессировании добавление леводопы |
Увеличение дозы леводопы, (300–400 мг в сутки), добавление ингибиторов МАО-В или других препаратов для усиления эффекта |
|
Старше 70 лет |
Леводопа — препарат выбора из-за высокой эффективности и лучшей переносимости |
Ограниченное добавление других препаратов (с осторожностью из-за побочных эффектов) |
Титрация дозы леводопы, добавление ингибиторов МАО-В или КОМТ, комбинированная терапия при необходимости |
Исследование Гох З с авторами (n=1620) показало, что начальная терапия леводопа при болезнь Паркинсона обеспечивает статистически значимое преимущество по подвижности (PDQ-39: +1,8 балла) и качеству жизни (EQ-5D: +0,03) по сравнению с дофаминовыми агонистами и ингибиторами МАО-В. Частота прекращения лечения была существенно ниже в группе леводопы (2 % против 28 % и 23 % соответственно). При длительном наблюдении (до 7 лет) различий по когнитивным нарушениям, госпитализациям и смертности не выявлено, что подтверждает её эффективность и безопасность в качестве стартовой терапии [17].
Выводы : В заключение, фармакотерапия занимает ведущую роль в лечении болезни Паркинсона и на сегодняшний день является одним из наиболее эффективных и научно обоснованных методов лечения. Поскольку ключевым патогенетическим фактором является дефицит дофамина, основной целью терапии является восполнение этого дефицита и восстановление нейромедиаторного баланса. В этом контексте препараты леводопы занимают особое место, а их сочетание с ингибиторами декарбоксилазы обеспечивает высокую клиническую эффективность и выраженное снижение моторных симптомов. Кроме того, дофаминовые агонисты, ингибиторы моноаминоксидазы-B (MAO-B) и ингибиторы катехол-O-метилтрансферазы (COMT) широко применяются на разных стадиях лечения. Эти препараты позволяют продлить действие леводопы, снизить её суточную дозу и повысить эффективность терапии. Однако при длительной фармакотерапии существует риск развития моторных флуктуаций, дискинезий и других побочных эффектов, поэтому процесс лечения требует постоянного мониторинга и корректировки. Принцип индивидуализации терапии особенно важен, поскольку необходимо учитывать клинические особенности каждого пациента, возраст, стадию заболевания и сопутствующую патологию. Правильно подобранная фармакотерапия не только замедляет прогрессирование болезни, но и улучшает качество жизни пациентов, сохраняя их социальную активность.
Литература:
- Li A, Cha A, Huang M, Dhami S, Pemminati S. A Review of the Recent Advances in the Pharmacological Management of Parkinson's Disease. Cureus. 2025 Sep 24;17(9):e93123. doi: 10.7759/cureus.93123. PMID: 41141087; PMCID: PMC12551797.
- Балестрино, Р., и Шапира, А. Х. В. (2020). Болезнь Паркинсона. Европейский журнал неврологии, 27(1), 27–42.
- Li, Y., Lv, Z., Dai, Y., Yu, L., Zhang, L., Wang, K., & Hu, P. (2025). The global, regional, and National burden of parkinson's disease in 204 countries and territories, 1990–2021: a systematic analysis for the global burden of disease study 2021. BMC public health, 25(1), 3047.
- Yang, Q., Chang, X., Li, S., Li, X., Kang, C., Yuan, W., & Lv, G. (2025). Disease Burden of Parkinson's Disease in Asia and Its 34 Countries and Territories from 1990 to 2021: Findings from the Global Burden of Disease Study 2021. Neuroepidemiology, 59(5), 525–557.
- Akhmedullin, R., Supiyev, A., Kaiyrzhanov, R., Issanov, A., Gaipov, A., Sarria-Santamera, A., Tautanova, R., & Crape, B. (2024). Burden of Parkinson's disease in Central Asia from 1990 to 2021: findings from the Global Burden of Disease study. BMC neurology, 24(1), 444.
- LeWitt P. A. (2015). Levodopa therapy for Parkinson's disease: Pharmacokinetics and pharmacodynamics. Movement disorders: official journal of the Movement Disorder Society, 30(1), 64–72.
- Lange K. W. (1998). Clinical pharmacology of dopamine agonists in Parkinson's disease. Drugs & aging, 13(5), 381–389.
- Lecht, S., Haroutiunian, S., Hoffman, A., & Lazarovici, P. (2007). Rasagiline — a novel MAO B inhibitor in Parkinson's disease therapy. Therapeutics and clinical risk management, 3(3), 467–474.
- Ruottinen, H. M., & Rinne, U. K. (1998). COMT inhibition in the treatment of Parkinson's disease. Journal of neurology, 245(11 Suppl 3), P25–P34.
- Kano, O., Tsuda, H., Hayashi, A., & Arai, M. (2022). Rasagiline as Adjunct to Levodopa for Treatment of Parkinson's Disease: A Systematic Review and Meta-Analysis. Parkinson's disease, 2022, 4216452.
- Tang, R., Zhang, S., Sun, R., Xu, J., Hu, Y., Tan, H., & Chen, L. (2025). Continuous Dopaminergic Stimulation-Based Levodopa Treatment in Patients with Early to Mid-Stage Parkinson's Disease: A Systematic Review and Meta-Analysis. Neurology and therapy, 14(4), 1197–1208.
- Salat, D., & Tolosa, E. (2013). Levodopa in the treatment of Parkinson's disease: current status and new developments. Journal of Parkinson's disease, 3(3), 255–269.
- Saba, R. A., Maia, D. P., Cardoso, F. E. C., Borges, V., F Andrade, L. A., Ferraz, H. B., Barbosa, E. R., Rieder, C. R. M., da Silva, D. J., Chien, H. F., Capato, T., Rosso, A. L., Souza Lima, C. F., Bezerra, J. M. F., Nicaretta, D., Povoas Barsottini, O. G., Godeiro-Júnior, C., Broseghini Barcelos, L., Cury, R. G., Spitz, M., Della Colletta, M. V. (2022). Guidelines for Parkinson's disease treatment: consensus from the Movement Disorders Scientific Department of the Brazilian Academy of Neurology — motor symptoms. Arquivos de neuro-psiquiatria, 80(3), 316–329.
- Höglinger, G., German Parkinson’s Guidelines Committee, & Trenkwalder, C. (2024). Diagnosis and treatment of Parkinson´s disease (guideline of the German Society for Neurology). Neurological research and practice, 6(1), 30.
- Jiang, D. Q., Wang, H. K., Wang, Y., Li, M. X., Jiang, L. L., & Wang, Y. (2020). Rasagiline combined with levodopa therapy versus levodopa monotherapy for patients with Parkinson's disease: a systematic review. Neurological sciences: official journal of the Italian Neurological Society and of the Italian Society of Clinical Neurophysiology, 41(1), 101–109.
- Chen, S., Chan, P., Sun, S., Chen, H., Zhang, B., Le, W., Liu, C., Peng, G., Tang, B., Wang, L., Cheng, Y., Shao, M., Liu, Z., Wang, Z., Chen, X., Wang, M., Wan, X., Shang, H., Liu, Y., Xu, P., … Xiao, Q. (2016). The recommendations of Chinese Parkinson's disease and movement disorder society consensus on therapeutic management of Parkinson's disease. Translational neurodegeneration, 5, 12.
- Goh, Z. H. K., Cheong, J. L. Y., Marras, C., Tanner, C. M., Kasten, M., Korczyn, A. D., Chahine, L., Lo, R., Noyce, A. J., & Movement Disorders Society Epidemiology Study Group (2022). Surveying Global Availability of Parkinson's Disease Treatment. Journal of Parkinson's disease, 12(3), 1023–1034.
- Левин О. С., Артемьев Д. В., Бриль Е. В., & Кулуа Т. К. (2017). Болезнь Паркинсона: современные подходы к диагностике и лечению. Практическая медицина, 1 (1 (102)), 45–51.
- PD Med Collaborative Group, Gray, R., Ives, N., Rick, C., Patel, S., Gray, A., Jenkinson, C., McIntosh, E., Wheatley, K., Williams, A., & Clarke, C. E. (2014). Long-term effectiveness of dopamine agonists and monoamine oxidase B inhibitors compared with levodopa as initial treatment for Parkinson's disease (PD MED): a large, open-label, pragmatic randomised trial. Lancet (London, England), 384(9949), 1196–1205.

