Хронические окклюзии коронарных артерий (ХОКА) встречаются в 20–30 % случаев при проведении коронарографии у пациентов с ишемической болезнью сердца. На сегодняшний день лечение пациентов с ХОКА путем ЧКВ является одной из наиболее сложных проблем в интервенционной кардиологии. В последние годы благодаря появлению ряда специализированных устройств, микрокатетеров, проводников, инновационных технологий, также не маловажную роль играет отличные характеристики стентов с лекарственным покрытием, значительно повысили уровень успеха и безопасность ЧКВ для лечения ХОКА. В дополнении ко всему все больше появляется научных и клинических данных в пользу реканализации ХОКА. Общеизвестно, что миокард в области окклюзированной артерии находится в состоянии ишемии. Наличие развитой системы коллатерального кровообращения позволяет обеспечить достаточный кровоток в миокарде лишь в покое, но при нагрузке коллатерального кровоснабжения недостаточно. Реканализация ХОКА позволяет уменьшить ишемию миокарда, также положительно влияет на систолическую функцию и ремоделирование миокарда левого желудочка, увеличивает толерантность к физическим нагрузкам и улучшить качество жизни пациентов.
Ключевые слова : чрескожное коронарное вмешательство, хронические окклюзии коронарных артерий, ишемическая болезнь сердца.
ПКА — правая коронарная артерия, ПМЖВ — передняя межжелудочковая ветвь, ХОКА — хроническая окклюзия коронарной артерии, ЭКГ — электрокардиография, ЭхоКГ — эхокардиография.
Введение
Ишемическая болезнь сердца (ИБС) в течение десятилетий занимает ведущую роль в структуре смертности от сердечно-сосудистых заболеваний во всем мире и остается одной из самых трудных проблем современной кардиологии. Основной причиной (~95 % больных) развития этого заболевания является атеросклеротическое поражение коронарных артерий, который часто на ранних стадиях протекает бессимптомно. Хроническая окклюзия коронарных артерий (ХОКА) характеризуется полной закупоркой просвета артерии атеросклеротическими массами в течение 3 мес. Как правило, этот процесс протекает медленно, и пациент ничего не ощущает. Согласно статистическим данным ХОКА имеются почти у 30 % пациентов с гемодинамически значимыми поражениями коронарных сосудов. Стентирование и ангиопластика коронарных артерий при хронических тотальных окклюзиях — наиболее сложная процедура в интервенционной кардиологии, частота попыток выполнения которой составляет около 8–14 % от всех чрескожных коронарных вмешательств. Однако в последние годы все больше появляется научных и клинических данных в пользу реканализации ХОКА. Современные исследования показывают, что после успешной реканализации ХОКА уменьшается функциональный класс (ФК) стенокардии, нормализуются результаты нагрузочных тестов, улучшается функция левого желудочка (ЛЖ) и снижается потребность в коронарном шунтировании.
Клинический пример
Пациент А., 63 года, находился на стационарном лечении в НАО Центр Сердца Шымкент в августе 2022г с диагнозом: Ишемическая болезнь сердца. Инфаркт миокарда c зубцом Q передней стенки левого желудочка. Острая стадия от 18.08.2022г. Сердечная недостаточность по Killip (I). Артериальная гипертензия III степени. Очень высокий риск. Сахарный диабет 2 тип, ИПФ, тяжелого течения в стадии декомпенсации. Двухсторонний коксартроз.
Жалобы при поступлении: на дискомфорт за грудиной жгучего характера, с иррадиацией в межлопаточную область, продолжительностью более 30 минут, возникший в покое, купируемый наркотическими анальгетиками, сопровождается одышкой, чувством нехватки воздуха, слабостью, холодным потом.
Анамнез заболевания: и з анамнеза известно, что с октября 2020 года пациент отметил появление одышки и снижение толерантности к физической нагрузке. Тогда же за медицинской помощью не обращался, обследование не проходил. В течении 1-й недели до госпитализации отмечает резкое снижение толерантности к физической нагрузке, малейшие физические нагрузки провоцировали приступы стенокардии, которые купировались в покое. По поводу чего обратился в Центральную районную больница по месту жительства, где пациент был осмотрен и даны рекомендации. 18.08.2022 г ранним утром 05.00 ч проснулся от жгучей боли за грудиной, сопровождалось холодным потом, чувством нехватки воздуха, после вызова СМП пациент по маршруту ОКС доставлен в НАО Центр Сердца Шымкент, где был экстренно госпитализирован в отделение реанимации и интенсивной терапии.
Анамнез жизни: сахарный диабет 2 тип выявлен в 2019 году, состоит на «Д» учете у эндокринолога, амбулаторно принимает: таб. глюконил 1000 мг/сут, тражента 5 мг/сут. Пациент страдает двусторонним коксоартрозом в течении 5 лет, по поводу чего периодически получает курс НПВП. Аллергоанамнез спокоен. Наследственность отягощена: у отца ИМ в 52 года, у братьев ИБС. Стаж табакокурения свыше 30 лет, по 1 пачке в день. Другие хронические патологии отрицает.
При объективном обследовании : при поступлении общее состояние пациента тяжелой степени тяжести. В сознании. Кожные покровы бледноватой окраски. Пастозность стоп. Аускультативно в легких ослабленное везикулярное, хрипов нет. Тоны сердца приглушены, ритмичные. Акцент 2 тона на аорте. Живот мягкий, при пальпации безболезненный. Стул и диурез в норме.
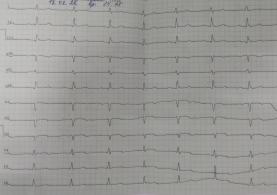
В инструментальных данных: На электрокардиограмме (рис. ЭКГ) при поступлении: синусовый ритм с частотой сердечных сокращений 74 уд./мин. Горизонтальное положение электрической оси сердца. Признаки очагово-рубцовых изменений миокарда передне-перегородочной, стенки левого желудочка.

По данным эхокардиографии (ЭхоКГ) — Уплотнение стенок корня и восходящей аорты. Краевой фиброз створок аортального клапана, митрального клапана. Аортальная регургитация 0-I ст, Митральная регургитация I степени. Трикуспидальная регугитация I степени. Легочная регургитация I степени. Зоны гипокинеза: средних передних, передне-боковых, перегородочных, верхушечных сегментов ЛЖ. Диастолическая дисфункция ЛЖ первого типа. Фракция выброса по методу Simpson — 48 %.
В лабораторных данных . В общем и биохимическом анализах крови — без значимых отклонений. В липидном спектре: холестерин общий 5,26 ммоль/л, холестерин липопротеинов низкой плотности 3,47 ммоль/л, холестерин липопротеинов высокой плотности 0,86 ммоль/л, триглицериды 2,11 ммоль/л, индекс атерогенности 5,1. Гликозилированный гемоглобин — 8,77 %. Высокочувствительный тропонин I — 0.351 нг/мл.
Учитывая острый инфаркт миокарда пациент экстренно взят на ЧКВ. Под местной анестезией пунктирована правая лучевая артерия, установлен интрадьюсер Balton 6F. Произведена селективная ангиография коронарного русла, данные которой представлены на рисунке. На КАГ выявлено: ПМЖВ — в дистальной трети стеноз 85 %, кровток TIMI-III. ДВ — в проксимальной трети стеноз 95 %, диаметр артерии 1,5 мм, кровток TIMI-III. ОВ — в проксимальной трети стеноз 45 %, кровоток TIMI-III. ВТК — стеноз у устья 60 %, кровоток TIMI-III. ПКА — в проксимальной трети хроническая окклюзия, кровоток TIMI-0. За счет межсистемной коллатерали заполняется ПКА.
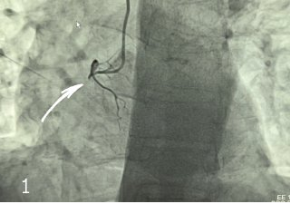
Рис. 1. Хроническая окклюзия в проксимальной трети ПКА
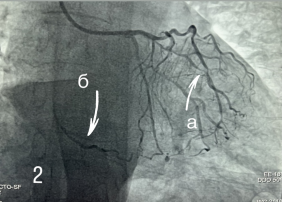
Рис. 2 а) ПМЖВ — в дистальной трети стеноз 85 %, б) Через межсистемные коллатерали заполняется ПКА
По результатам КАГ пациенту показано оперативное лечение — аорто-коронарное шунтирование. Интраоперационно проведен мультидисциплинарный консилиум с участием интервенционных кардиологов, кардиохирургов, лечащего кардиолога, учитывая многососудистое поражение коронарного русла, наличие у пациента сопутствующей патологии костно-суставной системы — двухсторонний коксоартроз, выраженное ограничение двигательной функции, передвижение только с помощью трости — у пациента высокий риск развития нестабильности грудины после АКШ, а также отказ пациента от АКШ — принято решено выполнить попытку реканализации ПКА с последующим стентированием ПНА и ОВ в плановом порядке.
Через правую лучевую артерию проведен гайд катетер Climber JR 3,5 6F, и произведена канюляция ПКА, неоднократные попытки провести реканализацию ПКА коронарным проводником Pilot 50–100 были безуспешны. Учитывая безуспешность антеградной реканализации, решено провести попытку реканализации ретроградным путем. В левую лучевую артерию установлен интрадьюсер Balton 6F. Канюляция ЛКА проведена через левую лучевую артерию гайд катетером Climber EBU 3,5 6F. Коронарный проводник Аsahi Sion blue проведен через огибающую артерию по межсистемным коллатералям в ПКА до окклюзии. Для устойчивости проводника взят баллонный катетер Powerline 1,5х15 мм. После нескольких попыток проведена реканализация ПКА ретроградно. Тем же баллоном Powerline проведена предилатация 10 атм. После баллонной ангиопластики второй коронарный проводник Аsahi Sion blue без препядственно проведен антеградно в дистальной треть ПКА. Проведена повторная ангиопластика баллонными катетерами Powerline 2,0х20 мм 10 атм. Далее позиционирован и установлен стент в проксимальный треть ПКА BioMatrix neoflex 2,75 x 28 mm 10 atm. Выполнена постдилатация стента баллонным катетором Mozec NC 3,0 x 15 mm. 12 atm. На контрольной коронарографии кровоток в ПКА восстановлен, остаточных стенозов нет.
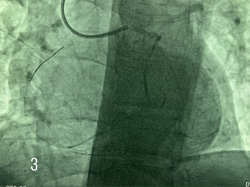
Рис. 3 Коронарный проводник проведен через огибающую артерию по межсистемным коллатералям в ПКА до окклюзии
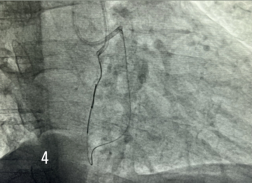
Рис. 4 Проведена реканализация ПКА ретроградным путем, после баллонной ангиопластики второй коронарный проводник проведен антеградно в дистальной треть ПКА
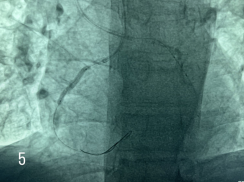
Рис. 5. Позиционирован и установлен стент в проксимальный треть ПКА
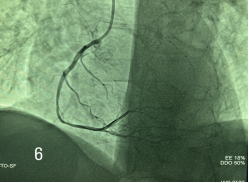
Рис. 6. На контрольной коронарографии кровоток в ПКА восстановлен, остаточных стенозов нет
Послеоперационный период протекал без осложнений. Пациент был выписан в удовлетворительном стабильном состоянии под наблюдение кардиолога по месту жительства. Через месяц планируется второй этап стентирование ПМЖВ.
Заключение
Хорошо развитые коллатерали в зоне окклюзии может быть достаточным для предотвращения ишемии, однако многие исследования доказали, что коллатерали могут хорошо обеспечивать миокард только в покое, но никогда не могут обеспечивать перфузию миокарда в окклюзированной зоне при физической нагрузке.
Приведенный выше клинический случай ЧКВ при ХОКА т. ч. ретроградным методом, является высокотехнологичной, безопасной и эффективной процедурой, в противовес открытому хирургическому лечению, который следует рассматривать методом выбора в пользу пациента.
Таким образом наш случай подтверждает, клинические преимущества у пациентов с коморбидной патологией и которым по определенным причинам не могут провести оперативное лечение традиционным способом. Конечно же, реканализация хронической окклюзии коронарных артерий ретроградным методом требует большого опыта и навыка оперирующего врача, однако наш кейс демонстрирует что успешная реканализация ХОКА значительно уменьшает зону ишемии, а также положительно влияет на функцию и ремоделирование левого желудочка, более того приводит к снижению потребности АКШ в будущем и улучшает отдаленную выживаемость.
Литература:
- Percutaneous Coronary Intervention for Chronic Total Occlusion Giovanni Maria Vescovo, Carlo Zivelonghi, Benjamin Scott. https://doi.org/10.15420/usc.2020.10
- https://www.escardio.org/Guidelines/Clinical-Practice-Guidelines/ESC-EACTS-Guidelines-in-Myocardial-Revascularisation-Guidelines-for
- Int J Angiol. 2021 Mar; 30(1): 48–52. Published online 2020 Dec 3. Management of Chronic Total Occlusion of Coronary Artery
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4774632/
- Zivelonghi C, van Kuijk JP, Poletti E, et al. A “minimalistic hybrid algorithm” in coronary chronic total occlusion revascularization: procedural and clinical outcomes. Catheter Cardiovasc Interv 2020;95:97–104.
- Nombela-Franco L., Werner G. S. Retrograde recanalization of a chronic total occlusion of the left anterior descending artery. J. Invasive Cardiol. 2010; 22 :E7–E12.
- Hsu JT, Tamai H, Kyo E, Tsuji T, Watanabe S. Traditional antegrade approach versus combined antegrade and retrograde approach in the percutaneous treatment of coronary chronic total occlusions. Catheter Cardiovasc Interv, 74 (2009), pp. 555–63. http://dx.doi.org/10.1002/ccd.22035

