It was studied the process of receiving the butenedyole -1,4 from acythelene and formaldegid under the atmospheric pressure. It was established the influence o different factors for this process.
The butane — 2 dyole -1,4, butanedyole — 1,4 technology was improved/ The shape — technical documents will be prepared and adopted.
Ключевые слова: синтез, ацетон, формальдегид, катализатор, температурa, реактор, скорость, пропаргиловый спирт, концентрация.
Изучен синтез бутин-2-диола-1,4 из ацетона и формальдегида по методике [1] в присутствии промышленного медь-цинк-алюминиевого катализатора низкотемпературного синтеза метанола марки СНМ-1 состава: % масс: CuO ‒ 53 ± 3,0; ZnO ‒ 26 ± 2 и Al2O3 ‒ 5,5 ± 0,5.
Реакцию ацетилена с формальдегидом изучали в реакторе с мешалкой или в реакторе типа барбатера. Перед проведением синтеза проводили активацию катализатора формальдегидом при температуре 60–75ºС в течение 6–8 часов. При этом расход формальдегида составлял 2,0- 2,5 моль на 1 г — атом меди на катализаторе. После активации катализатора раствор, содержащий муравьиную кислоту, сливали и загружали новую партию формальдегида [2].
Были проведены опыты по синтезу бутин-2-диола-1,4 в реакторе колонного типа с интенсивным перемешиванием реакционной смеси. При этом происходило идеальное перемешивание исходных компонентов.
Результаты показали, что при интенсивном перемешивании реакционной смеси, скорость образования бутин-2-диола-1,4 прямо пропорциональна количеству катализатора (табл. 1), а также уменьшается внутри диффузионное торможение процесса формальдегида и процесс протекает во внешней кинетической области что не зависит от количества формальдегида. Катализатор при этом образует активные комплексы с ацетиленом и формальдегидом. При соприкосновении вышеуказанных активных комплексов между собой образуются пропаргиловый спирт и бутин-2-диол-1,4.

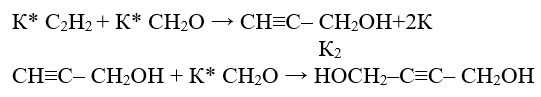
Установлено, что К1‹‹К2; так как из пропаргилового спирта и формальдегида мгновенно образуется бутин-2-диола-1,4. Протекание побочных процессов при бутин-2-диола-1,4, по-видимому, зависит от времени контакта ацетилена с абсорбированной молекулой формальдегида. Чем меньше время контакта ацетилена c формальдегидом, тем меньше образование побочных продуктов.
В качестве побочных продуктов, помимо пропаргилового спирта, образуются диацетил, винилпропаргиловый спирт и смола. Количество побочных продуктов колеблется от 4,5 до 18 % вес (в сумме).
На основании экспериментальных данных нами предложена математическая зависимость скорости реакции образования бутин-2- диола-1.4.
где: K-константа скорости;
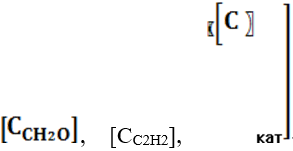 -концентрация формальдегида, ацетилена и катализатора соответственно:
-концентрация формальдегида, ацетилена и катализатора соответственно:
n — скорость перемещения
D* — коэффициенты диффузии,
К', К« — коэффициенты внутри диффузионного торможения формальдегида и бутин-2-диола-1,4;
a, b, c коэффициенты, определяемые экспериментальным путём, для каждого случая реакции.
Установлено, что в условиях интенсивного перемешивания начальная скорость образования бутин-2-диола-14 прямо пропорциональна количеству катализатора.
Таблица 1
Зависимость скорости реакции образования бутин-2-диола-1,4 от количества катализатора. (Т=90ºС, Vсн2o 1,0 л; Сcн2o 40,0%)
|
№ |
Количество катализатора, кг |
Скорость реакции, моль/час |
|
1 |
0,1 |
2,0 |
|
2 |
0,2 |
4,0 |
|
3 |
0,3 |
6,0 |
|
4 |
0,4 |
8,0 |
|
5 |
0,5 |
8,2 |
|
6 |
0,6 |
7,4 |
При этом скорость реакции определяли по изменению концентрации во времени.
Исследование процесса синтеза бутин-2-диола-1,4 в присутствии медь-висмутного (медь-никелевого) катализатора показало, что катализаторы, приготовленные методом многократной пропитки, также нестабильны во времени. С истечением времени наблюдается выделение ацетиленида меди как самостоятельной фазы что приводит к постепенному снижению активности катализатора и выходу целевого продукта [3].
Катализаторы с использованием в качестве носителя керамзита (приготовленного методом горячей пропитки) и оксида алюминия (приготовленного методом мокрого смешения активных компонент с носителем-гидратом оксида алюминия) также не проявили достаточную стабильность.
Среди исследованных образцов катализаторов наибольшую активность и селективность проявил промышленный катализатор низкотемпературного синтеза метанола марки CHM-1. На этом катализаторе нами изучены влияния температуры, времени реакции, pH среды, количества катализатора и др. на выход бутин-2-диола-14.
Температурный режим реакции исследовали в интервале температур от 60 до 110 С (Табл. 2). Установлено, что оптимальной температурой является 90º-95º С.
Таблица 2
Влияние температуры на выход бутин-2-диола-1,4
|
№ |
Температура, ºС |
Выход на катализаторах,% |
CuO— 53.0 ZnO— 26.0 Al2O3 –остальное |
|
CuO— 40.0; Bi2O3–10.0; Al2O3–50.0 |
|||
|
1 |
60 |
44,0 |
52,0 |
|
2 |
70 |
48,0 |
63,0 |
|
3 |
80 |
55,0 |
70,0 |
|
4 |
90 |
73,0 |
86,0 |
|
5 |
100 |
86,0 |
91,0 |
|
6 |
110 |
79,0 |
80,0 |
Как видно из данных таблицы, оптимальной температурой процесса является 90º-100ºС. Относительно низких температурах выход бутин- при 2-диола-1,4 средний, а при более высокой температуре наблюдается образование значительного количества смолистых веществ. Рассчитали тепловой эффект брутто-процесса образования бутин-2-диола-1,4 по известному методу
При этом найдено, что ∆Н298 =55 Ккал/Моль. С целью выяснения что влияния времени реакции на выход бутин-2-диола-14 были проведены опыты, где продолжительность реакции менялась от 4 до 20 часов.
При этом установлено, что оптимальным является время реакции — 14 часов. Использование катализатора состава СuО- 40,0 %, Bi20- 10,0 %, Al2O3 -50,0 % и медь-цинк-алюминиевого катализатора (CHM-1) дало возможность получить бутиндиoл-14 с достаточно высоким выходом за более короткое время (8–14 часов).
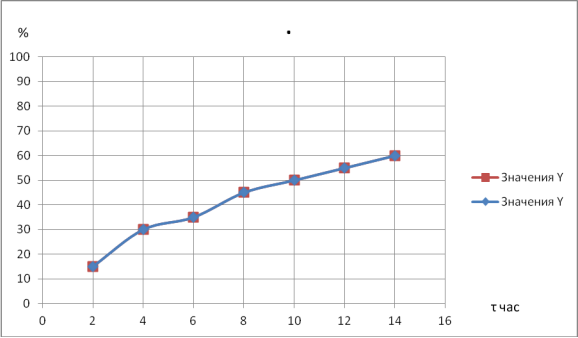
Рис. 1. Влияние времени реакции на выход бутин-2-диола-1,4: а) реакция с катализатором состава; СuО — 40,0 %, Bi2О3- 10,0 %, SiO2–50,0 %; б) реакция с катализатором CHM-1.
Установлены следующие технологические параметры и показатели процесса:
Катализатор CHM-1: CuO-53±3,0 %; ZnO-26±2,0 %;
Al2O3- 5,5–6,0 %
Количество катализатора — 200 г
Количество формальдегида — 500 мл
Температура — 90–95ºС
Продолжительность процесса — 8–10 часов
Начальная концентрация формальдегида — 13,4 моль (40 %).
Балансовый режим ацетилена — 800–1000 мл/мин
pH-реакционной массы — 4–6
Выход бутиндиола -1,4 по формальдегиду — 90–92 %
Конверсия ацетилена — 85–95 %
Изучен процесс гидрирования бутиндиола-1,4 до бутандиола -1,4 в присутствии селективного алюмо-никелевого катализатора Ренея. При гидрировании спиртового раствора бутиндиола-1,4 при 20–40º С и атмосферном давлении получен бутандиол-1,4 95–98 %-ным выходом.
Литература:
- Шаповалова А. Н. Синтез бутин-2-диола-1,4 из формалина и ацетилена при атмосферном давлении ЖПХ, 1969, Т. 36, с. 904–909
- Сергеев Г. П., Любомилова В. И., Богатырова А. И. Синтез бутин- 2-диола-1,4 из ацетилена и формальдегида при атмосферном давлении Хим. наук и пром. 1957, № 2, с. 272.
- Каримов А. У. Исследование технологических процессов синтеза бутин-диола-1.4 и бутандиола-1,4 из ацетилена и формальдегида при атмосферном давлении. Дисс. канд. техн. наук Т., 1997, с. 118
- Кадирова Н. Т. Совершенствование технологии производства бутин-2 диола -1,4, бутандиола-1,4 и продуктов их переработки. Дисс. канд. техн. Наук. Т., 2000, с. 96.







