Введение
Фенол и его производные являются высокостабильными органическими соединениями и очень токсичными для окружающей среды. Каждый год страны мира производят тысячи тонн этих нитрофенолов. Они очень токсичны для водных организмов, что может вызвать прямую нейротоксичность. Было изучено много методов для их разложения, таких как фотохимическая деградация, адсорбция активированного угля, фильтрация твердой мембраны, биодеградация, каталитическая деградация и т. д.
С другой стороны, 4-нитрофенол является важным посредником в производстве обезболивающих и препаратов, которые снижают температуру, такие как парацетамол. Однако, процесс восстановления 4-нитрофенола в р-аминофенол необходимы катализаторы для снижения энергии активации реакции [1].
Использование наночастиц серебра в качестве катализатора представляет большой интерес из-за их каталитической активности для многих органических реакций [2,3]. Существует много разных способов получения наночастиц серебра, но метод зеленого синтеза, используемого растительный экстракт в качестве восстановителя, является самым дешевым и наименее рискованным. Авторы [4] успешно синтезировали серебряные наночастицы из экстракта куркумы и изучили антимикробную способность материала.
Цель настоящей работы — синтез наночастиц серебра из экстракта куркумы и раствора AgNO3 для катализирования восстановления 4-нитрофенола.
Экспериментальная часть
Экстракт получили при нагревании m(g) порошок куркумы в 200 мл дистиллированной воды при температуре 99°C в течение определенного периода времени.
Добавили V мл экстракта в треугольник, содержащий 20 мл раствора AgNO3 xМ, помешали смесь магнитной мешалкой во следующих условиях: Время смешения: 9 ч; Температура: 250C; Объем экстракта: 1 ÷ 7 мл. После того центрифугировали в течение 15 минут и получили наночастицы серебра [4].
Процесс восстановления 4-нитрофенола проводили в стакане, содержащем 100 мл раствора 4-нитрофенол 1,5.10–3М и 0,15М NaBH4. Добавили сюда 10 мл раствора наночастиц серебра и осторожно перемешали. Время реакции варьируется от 1 до 60 мин. В каждый указанный промежуток времени отбирали 1мл смеси в 9 мл холодной воды и измерили молекулярные спектры на ультрафиолетовом свете Lambda PerkinElmer UV-VIS. Концентрация 4-нитрофенола определяется на основе оптической плотности при 401нм. Эффективность реакции рассчитывается по формуле:
где C0, Ct — начальная и оставляющая концентрация 4-нитрофенола в момент времени t.
Результаты иобсуждение
1. Каталитическая активность наночастиц серебра для реакции восстановления 4-нитрофенола
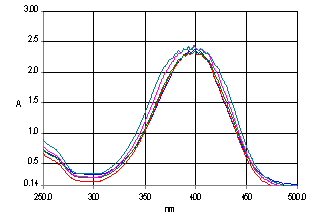
Молекулярные спектры UV-Vis реакционного раствора без катализатора в разное время приведены на рис. 1.
|
|
|
|
Рис. 1. Молекулярные спектры UV-Vis раствора 4-нитрофенола 1,5.10–4M + NaBH4 0,015M при T = 250C во время t = 1мин, 5 мин, 10 мин, 20 мин, 30 мин и 60мин |
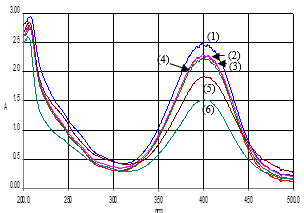
Рис. 2. Молекулярные спектры UV-Vis раствора 4-нитрофенола 1,5.10–4M + NaBH4 0,015M в присутствии наночастиц серебра при T = 250C во время t = 1мин (1), 5мин (2), 10мин (3), 20мин (4), 30мин (5) и 60мин (6) |
Результаты показали, что при 25°C молекулярные спектры смешанного раствора 4-нитрофенолаиNaBH4 были почти постоянными. Это значит, что в нормальных условиях процесс восстановления 4-нитрофенола боргидридом натрия без катализатора не происходит. На самом деле, реакция переноса 4-нитрофенола на 4-аминофенол происходит в условиях высокой температуры и давления или в присутствии катализаторов, которые уменьшают энергию активации, тем самым увеличивая скорость реакции.
Экспериментальные данные показали, что присутствие наночастиц серебра в реакционный раствор приводит к заметному увеличению скорости реакции (рис.2). Из оптической плотности при λ = 401нм получены данные по концентрации 4-нитрофенола подстановкой в стандартное калибровочное уравнение. Зависимость lnC от времени показывает, что реакция восстановления 4-нитрофенола боргидридом натрия в присутствии наночастиц серебра в качестве катализатора обладает кинетическим уравнением реакции первого порядка с константой скорости k = 0,0448 мин-1 (рис.3).
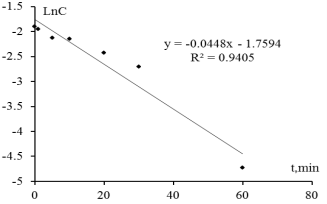
Рис. 3. Зависимость lnC от времени
2. Влияние экстракции куркумы на каталитическую активность наночастиц серебра
Для исследования влияния факторов на каталитическую активность нано-серебра, время реакции поддерживалось постоянным t = 60мин. На основе данных максимальной оптической плотности, измеренных при λmax = 401нм, подставляя в стандартное уравнение получается концентрация 4-нитрофенола и эффективность реакции (Н) рассчитается по формуле (1).
Зависимость эффективности реакции восстановления 4-нитрофенола от количества порошка куркумы приведена на рис.4.
|
|
|
|
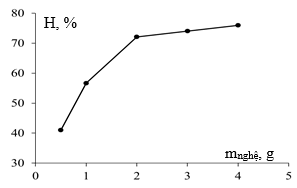
Рис. 4. Зависимость эффективности реакции 4-нитрофенол/NaBH4 с катализатором, полученным из экстракта куркумы и раствора AgNO3, от количества куркумы |
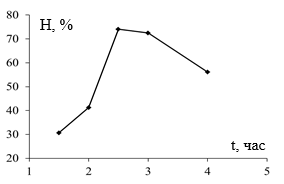
Рис. 5. Зависимость эффективности реакции 4-нитрофенол/NaBH4 с катализатором, полученным из экстракта куркумы и раствора AgNO3, от времени экстракции |
Видно, что с ростом количества порошка куркумы с 0,5г до 2г на 200мл воды, время экстракции: 2часа 30мин, каталитический эффект наночастиц серебра резко возрастает. Это можно объяснить тем, что при увеличении массы порошка количество восстановителей, входящих в растворитель, и следовательно, количество наночастиц серебра увеличивается. При продолжении увеличения массы куркумы эффективность восстановления почти не меняется. Это может быть связано с возрастанием размера частиц из-за повышения скорости формования.
Влияние времени экстракции куркумы на эффективность нанокатализатора для реакции восстановления 4-нитрофенола показано на рис. 5. Результаты показывают, что при увеличении времени экстракции эффективность восстановления сначала резко повышается, достигается максимум в области с 2часа 30мин до 3часа, потом уменьшается.
Известно, что время экстракции является одним из важных факторов, влияющих на количество восстановителей в экстракте, что определяет количество полученных наночастиц серебра. С другой стороны, если время экстракции было длинно, то возможно, что некоторые из восстановителей были разложены, испарены или в экстрактах могут появляться дополнительные окислители, способные реагировать с новыми наночастицами серебра. Это является причиной снижения активности катализатора.
3. Влияние процесса синтеза наночастиц на их каталитическую активность
Данные по зависимости эффективности реакции восстановления 4-нитрофенол от объема экстракта куркумы приведены на рис. 6.
|
|
|
|
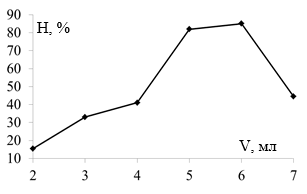
Рис. 6. Зависимость эффективности реакции 4-нитрофенол/NaBH4 с катализатором, полученным из экстракта куркумы и раствора AgNO3, от объема экстракта |
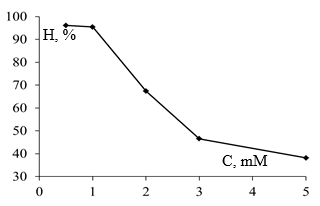
Рис. 7. Зависимость эффективности реакции 4-нитрофенол/NaBH4 с катализатором, полученным из экстракта куркумы и раствора AgNO3, от концентрации AgNO3 |
Из рис. 6 видно, что эффективность реакции восстановления быстро возрастает по мере увеличения объема экстракта от 2 до 5 мл. При объеме экстракции 6–7 мл она резко снижается. Это можно объясниться увеличением концентрации наночастиц из-за увеличения объема экстракции. Однако, при этом большие частицы могут быть легко агглютинированы, что приводит к снижению их каталитической активности.
Влияние концентрации раствора AgNO3 на эффективность наночастиц серебра показано на рис. 7. Экспериментальные результаты показывают, что увеличение концентрации AgNO3 от 0,5 до 5 mМ приводит к заметному понижению эффективности реакции восстановления 4-нитрофенола. Полученные результаты могут быть связаны с возрастанием размера образованных наночастиц при увеличении концентрации AgNO3.
Заключение
Таким образом, наночастицы серебра, синтезированные из экстракта куркумы и раствора AgNO3, способны катализировать восстановление 4-нитрофенола боргидридом натрия. Каталитическая активность материала зависит от условий процесса, включая экстракцию и синтез наночастиц.
Установлено, наночастицы серебра, синтезированные в условиях: 3g порошка на 200мл воды; время экстракции: 2 часа 30 мин; соотношение 6мл экстракта на 20 мл раствора AgNO3 10–3 M, обладает наилучшей каталитической активностью для восстановления 4-нитрофенола, эффективность реакции достигла примерно 95 % во время 60 мин.
Литература:
- Maolin Li and Guofang Chen. Revisiting catalytic model reaction p-nitrophenol/NaBH4 using metallic nanoparticles coated on polymeric spheres // Nanoscale. 2013, 5, P.11919–11927.
- Nguyen Thi Duyen. Синтез дисперсии наночастиц серебра на среднем капиллярном материале (SBA), используемом для обезуглероживания п-нитрофенола в сточных водах: Магистерская диссертация. Ханойский национальный университет. 2014.
- Nguyen Van Huong. Изучение обрабатывания нитрофенольной взрывчатой сточной воды с помощью оптического процесса Фентона: Магистерская диссертация. Ханойский национальный университет. 2013.
- Vo Thanh Hung. Cинтез наночастиц серебра из раствора AgNO3 с использованием экстракта куркумы и применение в качестве противомикробного материала: Магистерская диссертация, педагогический университет Данага. 2014.