В повседневную практику лечебно-диагностических учреждений все более активно входят гемоанализаторы. Гемоанализаторы в отличие от рутинных исследований крови дают, среди прочих, точные сведения о среднем объеме эритроцита (MCV), среднем содержании гемоглобина в отдельном эритроците (МСН), средней концентрации гемоглобина в эритроците (МСНС), показателе анизоцитоза эритроцитов (RDW), гемоглобине (HGB) и гематокрите (HCT). Перечисленные характеристики «красной» крови, несмотря на чрезвычайно высокую информативность, еще не достаточно широко используются в клинической практике. Тем не менее, показано, что многие из них высокоинформативны при динамическом наблюдении за результатами лечения пациентов с анемиями, больных онкологическими заболеваниями, болезнями почек [16]. Кроме того, гемоанализаторы существенно расширили возможности гематологов в изучении функциональной активности клеток крови и в том числе эритроцитов. Стало почти рутинным исследованием определение содержания и концентрации гемоглобина в эритроцитах, измерения среднего объема клеток как «красной» так и «белой» крови, тромбоцитов. Тем не менее, остается малоизученным вопрос о спонтанных или индуцированных какими-либо препаратами изменениях основных параметров крови при длительной инкубации invitro.
Можжевельник (Juniperus) — издревле используется в народной и официальной меди-цине. Ископаемая древесина JuniperixylonKalickii известна из палеоцена полуострова Челекен [23]. Из 60 видов можжевельника умеренного пояса северного полушария в бывшем СССР произрастало 20 видов, из которых 12 встречаются на территории Средней Азии. В европейской медицинской практике наиболее известны и используемы — JuniperuscommunisL.(верес) [17], можжевельник даурский — Junip-rusdavurica, можжевельник сибирский — JuniperussibiricaBurgsd., JuniperusnanaWilldPallasиможжевельник казацкий — JuniperussabinaLВ[23].
JuniperusturcomanicaB.Fedtsch. — такое название дано можжевельнику туркмен-скому (арче) в Средней Азии. Можжевельник туркменский (МТ) произрастает в Турк-менистане в виде редколесья от нижнего до верхнего пояса гор в Юго-Западном и Центральном Копетдаге. Плоды его, так же как и других представителей можжевельников, шишкоягоды черно-синего цвета, покрытые сизоватым восковым налетом [14,15]. В народной медицине шишкоягоды МТ используют в качестве мочегонного, дезинфицирующего, отхаркивающего и улучшающего пищеварение средства [1, 5, 7, 8, 10,14, 22].
МТ давно привлекает внимание туркменских ученых. Именно их исследованиями было установлено, что растение накапливает достаточно большое количество эфирных масел в плодах (1,29 %) и хвое (3,64 %). В состав эфирных масел МТ входят альфапинен, лимонен, кадинен, цедрол. Обнаружены, также, смолистые вещества — в хвое до 8,09 % и плодах — 4,8 %. В смоле хвои МТ идентифицированы гентриканотан, нонакозантол, ситостерин, оксидитер-пеновая кислота, названная туркомановой. Плоды и хвоя можжевельника туркменского богаты сахаристыми веществами (от 28 до 11 %) гликозидами (0,1–0.12 %), кумаринами (0.18–0,44 %), дубильными веществами (2,8–5,8 %), органическими кислотами (1,8–2.2 %), флавоноидами (0,8–1,5 %), витамином С (8 %) [15]. В целом химический состав МТ позволяет допустить его высокую биологическую активность на уровне организма вообще и конкретных органов и тканей в частности. Исследованиями туркменских ученых выявлены иммуномодулирующие свойства отвара МТ. В частности, показана его способность модулировать функциональную активность лимфоидных клеток условно здоровых лиц invitroиinvivo. А именно, как стимулировать, так и тормозить спонтанную и индуцированную тканевыми и паразитарными антигенами миграцию лейкоцитов из стеклянного капилляра [20,21]. 5 % отвар МТinvitro модулирует (чаще стимулирует) миграцию лейкоцитов периферической крови больных гипотиреозом в присутствии растворимого тканевого антигена щитовидной железы как invitro, так и invivo[7]; лейкоцитов крови больных хроническим тонзиллитом в присутствии тканевого антигена миндалин [6]. На основании чего препарат был рекомендован к применению и эффективно используется при лечении больных гипотиреозом и хроническим тонзиллитом.
Выраженное влияние отвара МТ на функции клеток крови послужило основным толчком к проведению настоящей работы, целью которой являлось изучение характера влияния 5 % отвара МТ in vitro на основные параметры автоматически полученной эритрограммы венозной крови условно здоровых лиц (УЗЛ).
Материалы и методы. Нами исследовано 200 гемограмм УЗЛ в возрасте 19–25 лет (средний возраст обследованных составил 22,7±0,9 лет). В работе использован гемо-анализатор ABXPentra 60 С+ (Франция). Для проведения исследования 5,0 мл венозной крови забирали преимущественно из локтевой вены УЗЛ при помощи вакутейнеров в специально предназначенные для гемоанализаторов данного класса одноразовые про-бирки (BD VACUTAINER K2E (EDTA) 5.0 ml). После первичного определения пара-метров крови на гемоанализаторе в пробирки вносили по 0,01 мл 5 % отвара МТ, тщательно перемешивали на шейкере при 150 колебаниях в минуту в течение 5 и 60 минут при комнатной температуре (+25ºС). В указанные сроки (5 и 60 минут) повторно определяли показатели красной крови.
МТ для исследования получали от Государственного института лекарственных растений АН Туркменистана в виде высушенной рубленой хвои, расфасованной в бумажные пакеты по 50 гр. 5 % отвар МТ (infusumex 10:200) готовили в соответствии с требованиями Фармакопеи (1991) [24] по прописи для Juniperus communis L. [18]. В частности, 10,0 г сухой измельченной хвои можжевельника туркменского (Juniperus turcomanica) заливали водой комнатной температуры, нагревали на кипящей водяной бане в течение 15 минут, затем настаивали 45 минут, процеживали и доливали первоначальный объем кипяченой водой. Препарат готовили непосредственно перед проведением эксперимента.
Полученные данные математически обработаны при помощи компьютерной программы SPSS.
Результаты исследования. Было установлено, что показатели эритрограммы крови УЗЛ существенно не изменяются в течение всего времени инкубации пробы (60 минут) при комнатной температуре (табл.1).
Таблица 1
Показатели эритрограммы крови условно здоровых лиц в зависимости от длительности инкубации (контроль)
|
Показатель/единицы измерения |
Исходные значения |
Через 5 минут |
Через 60 минут |
|
RBC (106/mm3) |
4,76+0,15 |
4,7+017 |
4,64+0,13 |
|
HGB (g/dl) |
13,2+0,55 |
13,1+0,3 |
12,9+0,6 |
|
HCT (%) |
39,1+1,5 |
38,6+1,9 |
37,6+1,5 |
|
MCV (μm3) |
82,5+0,21 |
82+0,13 |
80,6+1,0* |
|
MCH (pg) |
27,9+0,5 |
27,8+0,86 |
27,6+0,6 |
|
MCHC (g/dl) |
33,9+0,35 |
33,8+0,4 |
34,2+0,3 |
|
RDW (%) |
9,7+0,12 |
9,8+0,16 |
10,1+0,36 |
Примечание: * — p<0,05
Ни в один из сроков наблюдения математически достоверно не изменились численность эритроцитов (RBC), концентрация гемоглобина (HGB), гематокрит (HCT), среднее содержание гемоглобина в эритроците (MCH) и средняя концентрация гемоглобина в эритроците (MCHC). Однако некоторая тенденция к их снижению имелась (p>0,05) (рис.1).
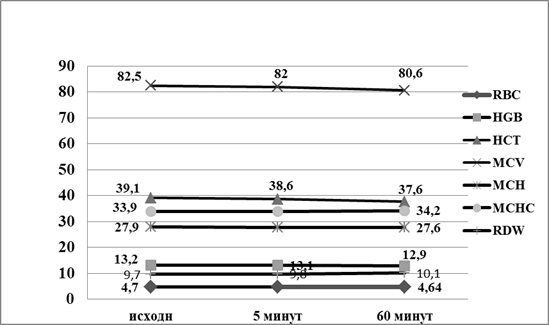
Рис. 1. Динамика параметров эритрограммы условно здоровых лиц в зависимости от времени инкубации без препарата (контроль)
На наш взгляд важно отметить, что при инкубации крови без препарата величина MCV– одна из важнейших характеристик эритроцитов первоначально так же имеет толь-ко тенденцию к снижению (p>0.05), но через 60 минут различие становися достоверным по отношению к исходному уровню (p<0,05) (рис.2).

Рис. 2. Сравнительня величина MCV в зависимости от времени и условий инкубации
Одновременно с увеличением MCV появляется тенденция к увеличению RDW — степени анизоцитоза эритроцитов, но различие на протяжении всего времени инкуба-ции остается стати-стически не достоверным (p>0,05) (рис.3).

Рис. 3. Сравнительня величина RDW в зависимости от времени и условий инкубации
При введении в пробирку с кровью 0,01 мл отвара МТ уже через 5 минут инкубации математически достоверно снизились величина гематокрита — HCT (p<0,01), средний объем эритроцита — MCV, содержание гемоглобина в эритроците -MCH (p<0,05), увеличился показатель анизоцитоза эритроцитов — RDW (p<0,05) (таблица 2, рис. 4). Однако общая численность эритроцитов — RBC иконцентрация гемоглобина — HGB, как и в контроле при этом не изменились (таб.2)
Таблица 2
Влияние отвара МТ (Juniperus turcomanica) на показатели эритрограммы крови условно здоровых лиц в зависимости от длительности инкубации
|
Показатель/единицы измерения |
Исходные значения |
Через 5 минут |
Через 60 минут |
|
RBC (106/mm3) |
4,7+0,1 |
4,5+0,2 |
4,5+0,25 |
|
HGB (g/dl) |
13,5+0,3 |
11,8+1,8 |
11,9+1,9 |
|
HCT (%) |
40+1,5 |
35,5+0,2** |
36,0+1,5* |
|
MCV (μm3) |
84+1,3 |
77+3,0* |
76,5+3,0* |
|
MCH (pg) |
28+1,2 |
25,5+0,5* |
22+0,5** |
|
MCHC (g/dl) |
33,9+1,0 |
33,5+0,6 |
34+0,15 |
|
RDW (%) |
9,5+0,9 |
10,6+0,8* |
10,8+0,6* |
Примечание: * — p<0,05; **- p<0,01
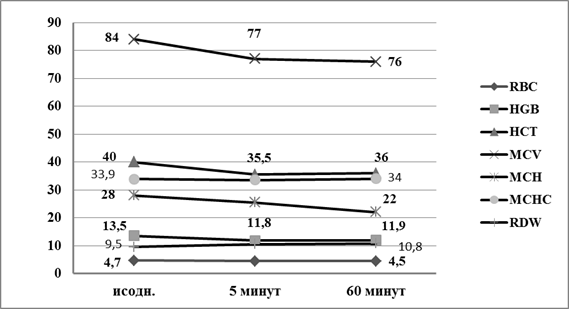
Рис. 4. Динамика параметров эритрограммы условно здоровых лиц в зависимости от времени инкубации в присутствии отвара МТ
Через 60 минут инкубации общая численность эритроцитов — RBC иконцентрация гемоглобина — HGB так и остались без изменения. Вместе с тем несколько увеличились по отношению к 5 минуте инкубации величины гематокрита — HCT, среднее содержание гемоглобина в эритроците –MCH, средняя концентрация гемоглобина в эритроците — МСНС и анизоцитоз эритроцитов- RDW; незначительно снизилась величина среднего объема эритроцита — MCV (p>0,05) (рис.4,5).

Рис. 5. Сравнительня величина MCH в зависимости от времени и условий инкубации
Все эти изменения носили математически недостоверный характер по отношению к 5-ой минуте инкубации (p>0,05), но оставались достоверными по отношению к исходным показателям (p<0,05) (рис.6).
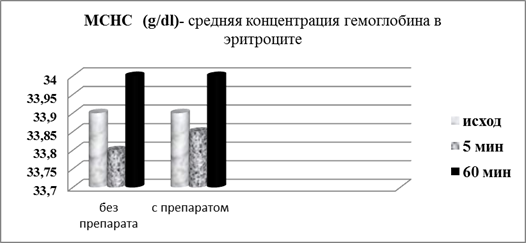
Рис. 6. Сравнительня величина MCHС в зависимости от времени и условий инкубации
Другими словами, основные изменения эритрограммы происходят уже на 5-ой минуте инкубации крови в присутствии МТ.
Обсуждение результатов исследования. Различные характеристики крови — это чрезвычайно важная информация не только о выраженности патологического процесса, если таковой имеется, но и состояния здоровья человека вообще. Гемоанализаторы резко сокращают вариабельность результатов и число субъективных ошибок лаборанта при исследовании крови больных, делают доступными для практического здраво-охранения довольно трудоемкие специальные исследования клеток крови. Они позволяют, так же, рассматривать известные показатели «белой» и «красной» крови в новом свете. Так величина RDW в настоящее время рассматривается в качестве важного дополнительного критерия диагностики и динамического наблюдения за результатами лечения пациентов с анемиями. По данным некоторых зарубежных авторов в целом ряде случаев железодефицитной анемии RDW становится выше нормы раньше, чем изменяются остальные параметры крови — MCV и HGB. Кроме того, изолированное повышение RDW предлагается расценивать в качестве раннего прогностического признака развития дефицита железа в организме [16]. Этот показатель полезен при дифференциальной диагностике микроцитарных анемий. Так, у пациентов с малой b-талассемией отмечаются низкие значения MCV, при нормальных показателях RDW, тогда как при дефиците железа MCV — снижен, а RDW- повышен. Установлено, что по мере нарушения гемоглобинообразования наблюдается прогрессивное снижение MCV, МСН, МСНС на фоне увеличения RDW. Эритроцитарная гистограмма существенно уширяется и значительно сдвигается влево [16].
Величина МСНС рассматривается в качестве генетически детерминированной, наиболее стабильной характеристики эритроцитов крови человека. Снижение величины МСНС наблюдается, в основном, при заболеваниях, связанных с нарушением синтеза гемоглобина [3]. Однако, корреляционной зависимости между скоростью синтеза глобина и уровнем гемоглобина крови не выявлено (r= +0,25; р>0,05) [9]. Снижение значений МСНС in vitro вприсутствии микроколичества отвара МТ, на наш взгляд, косвенно указывает на использование гемоглобина эритроцитов другими клетками крови, присутствующими в пробирке и «отвечающие» на присутствие МТ. Во всяком случае, установлено, что Гемофилус инфлюенса (Haemophilus influenzae) in vitro может использовать различные связанные с белком формы гема для роста на искусственной питательной среде, содержащей кровь. При чем, у некоторых «нетипичных» штаммов- мутантов значительно ослаблена способность к использованию гемоглобина для синтетических процессов [2]. Гем in vitro используется не только бактериями [12], но и паразитами, например шистосомами [4]. Известно, что в молекуле гема железо связано с потопорфирином. Кроме того, гем входит в состав цитохромов [13]. Вполне возможно, что используется не сам гемоглобин, а железо гема, так как известно, что не все железо, поглощенное клеткой, используется для синтеза гемоглобина, часть его депонируется в виде глыбок ферритина [3, 9]. Кроме того, в простетическую группу большинства фер-ментов антиоксидантной защиты — например, СДГ, МПО, каталазы, NADР.H-оксидазы входит атом железа [11,19].
Химический состав отвара МТ представлен определенным количеством биоло-гически активных молекул и в том числе эфирными маслами. Противовоспалительное действие отваров можжевельника — например, Juniperuscommunis среди прочих связывают именно с наличием в хвое и ягодах растения эфирных масел [15], которые, как известно, обладают антиоксидантными свойствами. Возможно, что антиоксидантный эффект препарата реализуется за счет способности определенных компонентов отвара данного лекарственного растения стимулировать синтез ферментов антиоксидантной защиты и не толькоinvivo, но и invitro. Непонятно, куда в системе in vitro в присутствии микроколичества отвара можжевельника туркменского может «уходить» гемоглобин эритроцитов. Во всяком случае, полученные результаты в известной степени могут свидетельствовать о способности компонентов отвара МТ модулировать обмен железа в эритроцитах крови практически здоровых лиц или использовать его для синтетическх процессов, осуществляемых invitro другими клетками крови, находящимися в пробе.
Кроме того, на наш взгляд, снижение среднего объема эритроцитов (MCV) при одновременно нарастающем анизоцитозе (RDW), наблюдаемое в присутствии отвара МТ, может быть обусловлено необходимостью поддержания стационарной концентра-ции гемоглобина в эритроцитах — МСНС, то есть сохранения гомеостаза всей системы эритрона.
Исследования в этом направлении на наш взгляд перспективны, так как позволяют уточнить не только свойства, отвара лекарственного растения (в данном случае можжевельника туркменского — Juniperusturcomanica), но и разработать научные осно-вы целенаправленного использования фитопрепаратов, глубже понять механизм их воз-действия на организм человека и, частности, клетки кр). МТ (Juniperusturcomanica) по ботаническим признакам и химическому составу схож с составом плодов и хвои офи-цинального вида Juniperuscommunisэто позволяет поддержать точку зрения [15] о возможности его использования в официальной медицинe наряду с последним.
Выводы:
1. Эритрограмма крови условно здоровых лиц при длительной (в течение часа) инкубации без добавления какого-либо препарата характеризуется значимым снижением среднего объема эритроцита (MCV) и появлением тенденции к увеличению анизоцитоза (RDW). Данное обстоятельство, на наш взгляд, необходимо учитывать при проведении исследования крови больных на автоматических гемоанализаторах.
2. Инкубация крови в присутствии 5 % отвар МТ in vitro сопровождается достоверным и прогрессивным снижением гематокрита (HCT), среднего объема эритроцита (MCV), содержания гемоглобина в эритроците (MCH), концентрации гемоглобина в эритроците (MCHC) при одновременном нарастании анизоцитоза (RDW).
Литература:
1. Adams R. P. 2004. Juniperus deltoidеs, a new species and nomenclatural notes on Juniperus policarpos and Juniperus turcomanica (Cupressaceae). Phytologia 86:49–53.
2. Barcak G. J., Chandler M. S., Redfield R. J., Tomb J.-F. (1991) Genetic systems in Haemophilus influenzae. Methods Enzymol. 204:321–342.
3. Deepika Darbari, Mark Loyevsky, Victor Gordeuk, John A. Kark, Oswaldo Castro, Sohail Rana, Victor Apprey, and Joseph Kurantsin-Mills (2003) Fluorescence measurements of the labile iron pool of sickle erythrocytes.Blood.102:357–364.
4. Lewis A Foster and Burton J. Bogitsh (1986) Utilization of the Heme Moiety of Hemoglobin by Schistosoma mansoni Schistosomules In vitro The Journal of Parasitology 72,5:669–676 Published by: The American Society of Parasitologists Article Stable URL: http://www.jstor.org/stable/3281454
5. Munir Ozturk, Salih Gucel et all. (2012) An overview of the medicinal plants of Turkey In. Genetic resources, chromosome engineering, and crop improvement (Medical plants), Ed. Ram J. Singh, CRC Press, Taylor&Francis Group, Bocf Raton-London-New York, 2012, Vol.6, chapter 7, p.181–207.
6. Pleskanovskaya S. A., Gurbandurdiyev A. et all (2003) On the possibility of Juniperus turcomanica decoction in the chronic tonsillitis patients’ treatment using, Turkmen health care J. 4:18–20.
7. Pleskanovskaya S. A., Mamedova G., Munir Ozturk, Salih Gucel, Ashyraliyeva M. (2012) Аn Overviev of the Ethnobotany of Turkmenistan and Use of Juniperus turcomanica in Phytotherapy In. Genetic resources, chromosome engineering, and crop improvement (Medical plants), Ed. Ram J. Singh, CRC Press, Taylor&Francis Group, Bocf Raton-London-New York, 2012, Vol.6, chapter 8, p.207–220
8. Ram J. Singh (2012) Landmark Research in medical plants Phytotherapy In. Genetic resources, chromosome engineering, and crop improvement (Medical plants), Ed. Ram J. Singh, CRC Press, Taylor&Francis Group, Bocf Raton-London-New York, 2012, Vol.6, chapter 1, p.1–13.
9. Regulation of cellular iron metabolism, Biochem J. 2011 March 15; 434(Pt 3): 365–381. http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3048577/
10. Shahina A. Ghazanfar (2012) Medical plants of the Middle East Phytotherapy In. Genetic resources, chromosome engineering, and crop improvement (Medical plants), Ed. Ram J. Singh, CRC Press, Taylor&Francis Group, Bocf Raton-London-New York, 2012, Vol.6, chapter 2, p.163–181.
11. Stryer L, Berg JM, Tymoczko JL (2002). Biochemistry. San Francisco: W. H. Freeman. ISBN 0–7167–4684–0.
12. Wandersman C., Stojiljkovic I. (2000) Bacterial heme sources: the role of heme, hemoprotein receptors and hemophores. Curr. Opin. Microbiol. 3:215–220. CrossRef
13. Идельсон Л. И. Гипохромные анемии. М., Медицина, 1981, 89 стр..
14. Каррыев М. О.,АртемьеваМ.В., Баева Р. Т., Киселева В. В., Наби-заде Л. И., Оразмухамедова Н. О. Фармакохимия лекарственных растений Туркменистана (Под ред. проф.Прокопенко А. П.), Ашхабад:Ылым,1991, 203 с.
15. Каррыев М. О. Арча — лекарственное растение, Ылым, Ашхабад, 1971.
16. Куриляк О. А. Клиническая интерпретация некоторых показателей гематологических анализаторов 26.05.2009. http://unimedao.ru/articles/-6826/9671-/item/90.
17. Лагерь А. А. Фитотерапия. Изд-во Красноярского университета: Красноярск, 1988, 300 с.
18. Машковский М. Д. Лекарственные средства, том 1, Медицина: Москва, 1973, Стр.398;
19. Николаев А. Я. Биологическая химия М: Высшая школа, 1989, 487 с.
20. Плескановская С. А.(2005) Фитоиммуномодуляции — возможности и перспективы. Аллергология и иммунология 6,3:323.
21. Плескановская С. А., Акыев А., и др. (2007) Модуляция иммунного ответа на антиген эхинокковой кисты отварами можжевельника туркменского. Аллергология и иммунология 8,1:104.
22. Справочник лекарственных растений Туркменистана (под ред. Каррыева М. О.), Ашгабат-1992, изд. АНТ «Энциклопедия», 88 с.
23. Телятьев В. В. Целебные клады (растения, продукты животного и минерального происхождения Центральной Сибири и их лечебные свойства) Восточносибирское книжное издательство, 1991, 400 с.
24. Фармакопея СССР, изд. 11, вып.2, М, Медицина, 1990, 398 с.







