Введение
В настоящее время значительная часть болезней человека связана с ухудшением экологической обстановки. Ионы многих металлов, содержащихся в окружающей среде, способны накапливаться в организме человека, оказывая отрицательное воздействие. Известно, что повышенное содержание алюминия ведет к нарушению обмена веществ, расстройству нервной системы, способствует увеличению распространенности анемий.
Суммарное содержание всех форм алюминия в питьевой воде не должно превышать 0.5 мг/л (в Европе — 0.2 мг/л, в США — 0.05 мг/л).
Из-за широкого распространения алюминиевых изделий и негативного влияния соединений алюминия на здоровье человека представляется актуальным контролировать содержание алюминия в объектах окружающей среды [1].
В настоящее время применяют различные способы определения алюминия в зависимости от состава анализируемого объекта. Среди аналитических методов особый интерес представляет экстракционно-фотометрический, благодаря его довольно высокой чувствительности, селективности, точности и простоте выполнения.
Цель нашей работы — экстракционно-фотометрическое определение ионов алюминия в водных растворах с применением спиртов в качестве добавок к основному экстрагенту — толуолу. Подобные исследования применительно к определению алюминия в литературе отсутствуют.
На нашей кафедре разработана экстракционно-фотометрическая методика определения содержания алюминия (III), основанная на образовании экстрагируемого бензолом ионного ассоциата фторидного комплекса алюминия с основными красителями. [2] Бензол, являясь хорошим экстрагентом, весьма ядовит и практически не выводится из организма, поэтому перед нами стояла задача — заменить бензол на менее вредный экстрагент толуол. Толуол, в отличие от бензола, не накапливается, а выводится из организма.
Плотность заряда на ионе фтора высока, вследствие его малого размера, в результате чего фторидный комплекс алюминия (III) несет на себе достаточно большой отрицательный заряд, что является причиной незначительного перехода его ионного ассоциата с бриллиантовым зеленым в малополярный растворитель толуол.
Мы предположили, что добавление некоторых более полярных растворителей, например, некоторых спиртов к толуолу должно увеличивать экстракцию ассоциата за счет частичной компенсации заряда комплекса, что приведет к увеличению степени извлечения ионного ассоциата.
В качестве полярных растворителей использовали амиловый, гексиловый, октиловый, нониловый, ундециловый спирты.
В качестве основного красителя в нашей работе был использован краситель трифенилметанового ряда — бриллиантовый зеленый.
Определение основано на измерении оптической плотности экстракта ионного ассоциата фторидного комплекса алюминия (III) с бриллиантовым зеленым.
Экспериментальная часть
В работе использован кристаллогидрат нитрата алюминия Al(NO3)3·9H2O «х. ч»., толуол«х. ч»., спирты «х. ч».. Исходный раствор соли (0.1 моль/л) готовят растворением соответствующей навески в дистиллированной воде, подкисленной азотной кислотой. Концентрацию ионов алюминия в полученном растворе определяют обратным комплексонометрическим титрованием раствором сульфата цинка с индикатором ксиленоловым оранжевым [3].
Растворы меньшей концентрации готовят соответствующим разбавлением непосредственно перед использованием. Растворы соли алюминия подкисляют азотной кислотой (до pH = 3) для предотвращения их гидролиза. Измерение оптической плотности экстракта ионного ассоциата проводят на спектрофотометре СФ-26. Все органические растворители перед экстракцией насыщают водой, а воду — соответствующим экстрагентом.
Методика определения
В делительные воронки помещают 5 мл 10–5 М раствора нитрата алюминия, приливают 1 мл 0.01М раствора фторида калия. Затем добавляют 10 мл ацетатно-аммиачного буферного раствора с pH = 3.0 и 3 мл 0.01М раствора бриллиантового зеленого, объем жидкой фазы доводят дистиллированной водой до 30 мл, приливают 3.5 мл толуола, держащего различные объемы используемых спиртов.
Содержимое делительных воронок перемешивают на механической мешалке в течение 5 минут. Предварительно было установлено, что пятиминутного перемешивания достаточно для установления равновесия в системе.
После разделения органической и водной фаз экстракт помещают в фотометрическую кювету с толщиной поглощающего слоя 1 см и измеряют оптическую плотность на фоне раствора сравнения. Раствор сравнения готовят по аналогичной методике с той разницей, что вместо исследуемого раствора, содержащего ионы алюминия, помещают 5 мл дистиллированной воды.
Для нахождения оптимальной длины волны снята кривая поглощения ионного ассоциата в толуоле в интервале длин волн от 500 до 700 нм. Спектры поглощения сняты в присутствии всех исследованных спиртов. (Рис. 1)
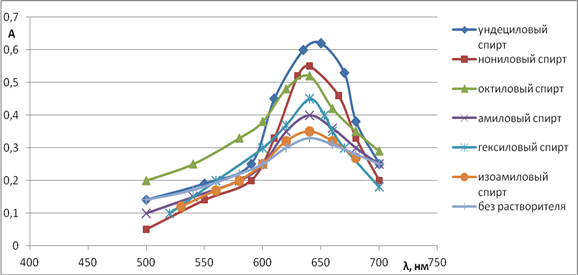
Рис. 1. Спектры поглощения ионного ассоциата фторидного комплекса алюминия с бриллиантовым зеленым на фоне раствора сравнения при добавлении различных спиртов
Из Рис. 1 видно, что максимальное поглощение комплекса приходится на длину волны, равную 640 нм и при использовании в качестве добавки ундецилового спирта. Поэтому дальнейшие измерения проводили при 640 нм.
В дальнейшем исследовано: влияние избытков реагентов — бриллиантового зеленого, фторида калия. Найдена оптимальная кислотность водной фазы (рН = 3). Определены объемные доли исследуемых спиртов, при добавлении которых к толуолу получено максимальное увеличение оптической плотности экстракта.
Для нахождения оптимальных значений вышеперечисленных факторов использована вышеописанная методика. При этом исходная концентрация Al (III) оставалась постоянной, менялась концентрация того вещества, влияние которого исследовалось.
Проведенные исследования позволили окончательно сформулировать методику определения: в делительные воронки помещают 5 мл 10–5 М раствора нитрата алюминия, приливают 1 мл 0.01М раствора фторида калия. Затем добавляют 10 мл ацетатно-аммиачного буферного раствора с pH = 3.0 и 3 мл 0.01М раствора бриллиантового зеленого, объем жидкой фазы доводят дистиллированной водой до 30 мл, приливают 3.5 мл толуола, содержащего 1,13 % ундецилового спирта.
С использованием разработанной методики проведено определение концентрации Al(III) в водных растворах по методу градуировочного графика. Для сравнения построены градуировочные графики с использованием в качестве экстрагента чистого толуола и толуола с добавкой ундецилового спирта. (Рис.2)
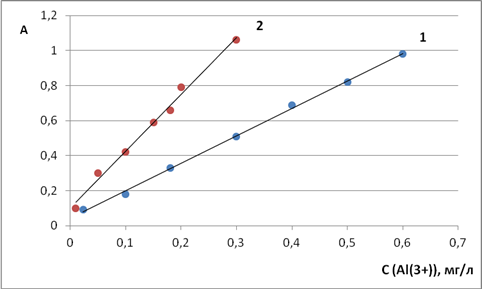
Рис. 2. Градуировочные графики для определения алюминия (III) в водных растворах: 1- экстрагент — толуол; 2 — экстрагент толуол + ундециловый спирт
Уравнение градуировочного графика 1 (экстрагент — толуол): y = 1,579x+0,067, коэффициент корреляции 0,992. Рабочая область градуировочной зависимости находится в интервале концентраций 0,023–0,61 мг/л. Предел обнаружения равен: Cmin=6 мкг/л. Рассчитан молярный коэффициент светопоглощения ионного ассоциата в органической фазе: ε = (6,3 ± 0,1).104 л/(моль.см).
Уравнение градуировочного графика 2 (экстрагент толуол + ундециловый спирт):
y = 3,386x+0,092, коэффициент корреляции 0,992. Рабочая область градуировочной зависимости находится в интервале концентраций 0,009–0,44 мг/л. Предел обнаружения равен: Cmin= 1,2 мкг/л. Молярный коэффициент светопоглощения ионного ассоциата в смешанном органическом растворителе имеет значение ε = (2,5 ± 0,1).105 л/(моль.см), что в 4 раза выше коэффициента чувствительности в случае использования в качестве экстрагента чистого толуола.
При использовании смешанного экстрагента возрастает чувствительность определения ионного ассоциата алюминия (тангенс угла наклона графика).
Проверка воспроизводимости результатов определения алюминия методом «введено — определено»
Градуировочные графики применены для определения Al(III) в водных растворах (Таблицы 1 и 2).
Таблица 1
Результаты определения алюминия (III) методом «введено — определено» (n=3, P=0,95; экстрагент — толуол)
|
Введено, мг/л |
Определено, мг/л |
Sr |
|
0,14 |
0,138±0,004 |
0,06 |
|
0,45 |
0,449±0,002 |
0,01 |
|
0,67 |
0,667±0,003 |
0,02 |
Таблица 2
Результаты определения алюминия (III) методом «введено — определено» (n=3, P=0,95; экстрагент — толуол с добавкой ундецилового спирта)
|
Введено, мг/л |
Определено, мг/л |
Sr |
|
0,090 |
0,091±0,018 |
0,05 |
|
0,150 |
0,147±0,016 |
0,03 |
|
0,220 |
0,218±0,016 |
0,02 |
Из таблиц 1 и 2 видно, что определение с использованием экстрагента толуола и экстрагента толуола с добавкой ундецилового спирта позволяет получать хорошо воспроизводимые достаточно точные результаты с относительной погрешностью не более 6 %.
Заключение
Разработана методика экстракционно-фотометрического определения ионов алюминия в водных растворах, основанная на образовании экстрагируемого ассоциата фторидного комплекса алюминия с бриллиантовым зеленым с использованием смешанного экстрагента.
Коэффициент чувствительности определения ассоциата возрастает в 4 раза по сравнению с использованием в качестве экстрагента чистого толуола.
Методика характеризуется хорошей воспроизводимостью и точностью результатов анализа, что подтверждается методом «введено — определено».
Литература:
1. Давыдова С. Л. О токсичности ионов металлов. М.: Наука, 1991. 31 с.
2. Кутырева И. А., Калугин А. А., Зорин А. Д., Занозина В. Ф. Вестник Нижегородского университета им. Н. И. Лобачевского, 1 (1), 2012, 318 с.
3. Умланд Ф. и др. Комплексные соединения в аналитической химии: теория м практика применения. М.: Мир, 1975, 536 с.

