О возможности получения металлического кальция различными восстановителями
Автор: Фалин Владимир Викторович
Рубрика: 6. Металлургия
Опубликовано в
Дата публикации: 04.10.2013
Статья просмотрена: 1983 раза
Библиографическое описание:
Фалин, В. В. О возможности получения металлического кальция различными восстановителями / В. В. Фалин. — Текст : непосредственный // Технические науки: традиции и инновации : материалы II Междунар. науч. конф. (г. Челябинск, октябрь 2013 г.). — Т. 0. — Челябинск : Два комсомольца, 2013. — С. 48-53. — URL: https://moluch.ru/conf/tech/archive/87/4269/ (дата обращения: 27.04.2024).
Исследована возможность получения металлического кальция различными термическими методами, а именно — методом диссоциации карбида кальция в вакууме, с помощью газовых восстановителей и металлотермическим восстановлением оксида кальция. Показано, что применение газовых восстановителей или диссоциация карбида кальция при температурах ниже 1750 0С не позволяет получить металлический кальций. Алюминотермическое восстановление сопровождается хорошей смачиваемостью алюминием поверхности оксида, однако не является оптимальным по себестоимости восстановителя. Критерий смачиваемости положен в основу выбора металла восстановителя.
Ключевые слова:кальций; восстановление оксида кальция; диссоциация карбида кальция; вакуумная печь; алюминотермическое и металлотермическое восстановление.
В мире и, прежде всего, в КНР как главном поставщике кальция, его получение основано на процессе восстановления оксида кальция алюминием [1]. В Российской Федерации этот способ пока не нашел своего промышленного воплощения. Поскольку для нужд металлургической промышленности на первый план выходит не чистота получаемого кальция, а его стоимость, нами исследовалась возможность получения кальция металлотермическим, в том числе, алюминотермическим, а также альтернативными методами, связанными с проведением нагрева в вакууме.
Процессы получения кальция проводились на вакуумной дистилляционной электропечи ВОж-16–22 (рис.1) в состав электропечи помимо основных компонентов входили:
- нагревательный блок из углерод-углеродного композиционного материала (УУКМ) различной плотности;
- охлаждаемый водой конденсатор паров кальция;
- в вакуумной системе предусмотрен мембранный насос, позволяющий проводить откачку паров воды при относительно низких температурах.

Рис. 1. Вакуумная дистилляционная печь ВОж-16–22
Используемая в работе измерительная аппаратура:
- рентгеновская съемка (РФА) проведена на дифрактометре ДРОН-3 в CuKα;
- растровая электронная микроскопия (РЭМ) проведена на электронном микроскопе FEI Quanta 600 FEG с приставкой энергодисперсионного рентгеновского микроанализа EDAX;
- массу образцов измеряли на лабораторных электронных весах AJH-620CE.
Используемые в работе материалы: оксид и карбид кальция, алюминий марки АПВ, кремний технический КР00, ферросилиций ФС75, ацетилен марки Б, аргон газообразный высшего сорта и диоксид углерода газообразный.
Возможность получения металлического кальция как продукта диссоциации карбида кальция была проверена при проведении нагревов в вакууме 1 Па. На рис.2 показана зависимость выхода кальция от температуры при постоянной выдержке — 3 час.
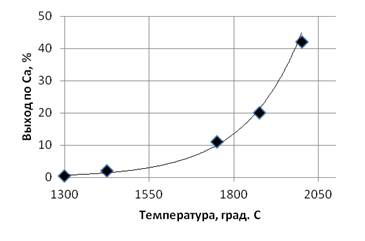
Рис. 2. Выход кальция при дистилляции карбида кальция в зависимости от температуры при постоянном давлении 1 Па и времени выдержки 3 час.
Как видно из представленных данных, заметный выход кальция соответствует температуре 1750 0С. Это не совпадает с расчетными данными работы [2], в которой приведены результаты термодинамических оценок реакции диссоциации карбида кальция с поправкой на изотерму Ван-Гоффа.
В соответствие с этими оценками температура начала диссоциации при давлении 100 Па должна составлять 1526 0С, а при давлении 10 Па — 1286 0С. Причиной такого несоответствия, видимо, является то обстоятельство, что при выводе уравнения изотермы Ван-Гоффа предполагается гомогенность системы, в которой происходит химическая реакция (наличие пара кальция и твердых углерода и карбида кальция делает систему гетерогенной), а также, то, что каждый участник реакции есть идеальный газ (очевидно, в рассматриваемой системе — это не так). Также вызывает большие сомнения принципиальная возможность применения стандартных термодинамических расчетов, например, по алгоритму Темкина — Шварцмана, для реальных необратимых термических процессов, сопровождаемых испарением, образованием и растворением промежуточных соединений, изменением межфазных границ.
Образующийся при диссоциации CaC2 углерод обладает низкой эрозионной стойкостью и требует применения специальных мер, предотвращающих распыление и последующее осаждение продуктов износа в местах электрических вводов в герметичный объем, а также исключающих попадание частиц углерода в откачную систему. Как показали прямые эксперименты, при скорости откачки (скорости напуска воздуха) более 50 Па/с в диапазоне давлений > 30 кПа происходит «разброс» углерода по рабочему пространству печи, а, следовательно, возникает опасность его попадания в систему откачки и на диэлектрические вводы.
Следовательно, применение прямой диссоциации карбида кальция требует проведение процесса в области высоких температур (выше 1750 0С); время откачки и напуска воздуха при этом будет составлять до 1 часа. При стоимости карбида кальция 60–65 руб./кг [3] получение кальция из такого сырья при существующих ценах на кальций вряд ли рентабельно.
Эксперименты с газообразными восстановителями (C2H2–10 кПа + Ar — 24 кПа с диссоциацией ацетилена) или CO2 (наличие в печи нагревательного блока из УУКМ приводит к образованию CO по реакции Будуара) показали отсутствие восстановления оксида кальция, как при постоянной атмосфере газа-восстановителя, так и при проведении циклического режима.
Наличие в составе оксида кальция заметного количества карбоната кальция (в отечественном сырье доля карбоната кальция в оксиде достигает 15–20 масс. %), а тем более применение двуокиси углерода в печи с нагревателями из углеродного материала приводит к выходу из строя нагревателя. На рис.3 показано разрушение электрического контакта нагревателя печи после проведения экспериментов с CO2. Между секцией нагревателя и токоподводом образовалась магистральная трещина.

Рис. 3. Разрушение углеродного нагревателя печи ВОж-16–22 после проведения экспериментов с CO2.
В настоящее время единственным методом металлотермического получения кальция, применяемым в промышленности, является способ алюминотермического восстановления оксида кальция. Для гетерогенной системы CaO — Al (расплав) — Ca (газ) при прочих равных параметрах кинетика восстановления определяется размерами межфазной границы раздела.
При алюминотермическом (АПВ) восстановлении в составе шихты были идентифицированы следующие фазы: 3CaO*Al2O3, 12CaO*7Al2O3 и Al2Ca. На рис.4 показана микроструктура шихты после проведения алюминотермического восстановления (температура 1350 ОС, выдержка в течение 3 час. при остаточном давлении 1 Па). Обращает на себя внимание наличие ярко выраженных линейных структурных элементов толщиной 102–103 нм (рис.4, а,б — съемка с поверхности).
Состав этих структурных элементов, точнее, соотношение содержания кальция к алюминию (рис.5.) не позволяет «приписать» линейные структурные элементы ни к одной из идентифицированных фаз: в них «завышено» количество алюминия.

Рис. 4. Микроструктура брикета после алюминотермического восстановления во вторичных и обратно рассеянных электронах (а) и во вторичных электронах (б,в): а,б — съемка с внешней поверхности образца; в –съемка с поверхности излома.

Рис. 5. Элементный состав линейной структуры брикета после проведения алюминотермического восстановления.
Если предположить, что измеренная величина состава связана с раствором Al2Ca — Al4Ca, имеющим область гомогенности более 10 % Ca (раствор на базе Al2Ca в приблизительном соотношении интерметаллидов 75:25), то это устраняет «противоречие» между результатами РФА и РЭМ.
Линейные размеры составляют 200–500 мкм, что близко к размеру фракций CaO. В то же время съемка с поверхности излома образца не выявила наличие подобных структурных элементов (рис.4, в). Поверхности съемки отличаются условиями смачиваемости.
Вблизи светлой границы (рис.6.) — смесь алюминатов кальция 3CaO*Al2O3, 12CaO*7Al2O3.

Рис. 6. Элементный состав вблизи светлой границы после проведения алюминотермического восстановления.
Проведенные эксперименты дают основание полагать, что смачиваемость восстановителем межфазной границы играет значительную роль в металлотермическом восстановлении оксида кальция. Поскольку одной из основных статей расхода при проведении алюминотермического восстановления является стоимость алюминия, были проведены эксперименты по изучению возможности замены алюминия более дешевым восстановителем.
В качестве восстановителей применяли технический кремний Кр00, ферросилиций ФС 75 в различных отношениях с порошком вторичного алюминия АПВ. При применении железа в его составе присутствовали 1,2–2,0 % Si и 0,4–0,7 % Mn.
Порошки смешивали с оксидом кальция в массовом соотношении 80 % оксида и 20 % металла-восстановителя с последующим прессованием в брикеты. В табл. 1 показаны составы восстановителей (ат. %) и величина выхода по кальцию. При выбранном режиме (температура 1350 ОС, выдержка в течение 3 час. при остаточном давлении 1 Па) восстановитель находится в жидком состоянии; в табл.1 также указана температура ликвидуса восстановителя [4].
Таблица 1
Состав исследованных восстановителей оксида кальция и выход кальция
|
№ смеси |
Восстановитель, ат. % |
Выход по Ca, % |
Т ликвидуса, ОС [4] |
||
|
Al |
Si |
Fe |
|||
|
1 |
100 |
- |
- |
57 |
660 |
|
2 |
76 |
24 |
- |
43 |
760 |
|
3 |
51 |
49 |
- |
39 |
1020 |
|
4 |
26 |
74 |
- |
27 |
1250 |
|
5 |
89,3 |
9,2 |
1,5 |
51 |
735 |
|
6 |
72,8 |
23,3 |
3,9 |
47 |
880 |
|
7 |
50,8 |
42,2 |
7 |
38 |
1040 |
|
8 |
- |
85,7 |
14,3 |
17 |
1320 |
Таблица 2
Состав кальция
|
№ смеси |
Примеси, масс. % |
||||||
|
Mg |
Al |
Si |
Fe |
Mn |
K |
Na |
|
|
1 |
0,44 |
0,50 |
0,05 |
0,003 |
0,049 |
0,002 |
0,001 |
|
3 |
0,41 |
0,05 |
0,03 |
0,002 |
0,02 |
0,015 |
0,015 |
|
4 |
0,35 |
0,04 |
0,06 |
0,002 |
0,02 |
0,003 |
0,006 |
|
8 |
0,40 |
0,04 |
0,04 |
0,005 |
0,02 |
0,009 |
0,012 |
|
Электролиз «ЧМЗ» |
0,0005 |
0,012 |
0,016 |
0,0036 |
0,0026 |
0,003 |
0,01 |
Анализ представленных результатов свидетельствует о сложном влиянии состава и температуры ликвидуса восстановителя на выход кальция. Так, выход кальция (табл.1), полученный при восстановлении смесью 76 % Al — 24 % Si (№ 2), меньше выхода кальция при восстановлении смесью 72,8 % Al — 23,3 % Si — 3,9 % Fe (№ 6).
Обычный подход к интерпретации результатов, полученных при восстановлении CaO, предусматривает, что скорость образования кальция на конденсаторе на начальных стадиях определяется испарением, а затем — встречной диффузией кальция в оксиде и металла восстановителя к поверхности раздела. Однако это не позволяет объяснить того факта, что рассчитанная, например, по данным [5,6] энергия активации процесса (соответственно 47 кДж/моль и 42 кДж/моль) в 3–4 раза отличаются и от значений теплоты испарения кальция, и от значений энергии активации диффузии кальция в структурах, близких к алюмосиликатам кальция [7].
Исходя из того, что устойчивое равновесие системы с постоянной температурой и объемом соответствует минимуму свободной энергии Гельмгольца, а также — исходя из модели, в которой при наличии смачиваемости на физическом рельефе поверхности раздела, происходит перемещение расплава металла-восстановителя, можно получить зависимость выхода Y от температуры Т процесса в виде соотношения:
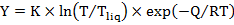 ,
,
где: 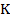 — постоянный для данного восстановителя коэффициент пропорциональности,
— постоянный для данного восстановителя коэффициент пропорциональности, 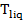 — температура плавления для однокомпонентного восстановителя или температура ликвидуса многокомпонентного восстановителя,
— температура плавления для однокомпонентного восстановителя или температура ликвидуса многокомпонентного восстановителя, 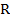 — газовая постоянная,
— газовая постоянная, 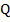 — теплота испарения кальция.
— теплота испарения кальция.
Приведенное выше соотношение вполне удовлетворительно согласуется с известными нам данными по металлотермическому восстановлению оксида кальция.
Переход от алюминия к иному восстановителю приведет к изменению Тliq. Повышение температуры восстановления сопровождается повышением расхода электроэнергии вакуумной электропечи. Таким образом, одновременный учет стоимости металла-восстановителя и стоимость электроэнергии на единицу массы кальция позволит выйти на оптимальный режим восстановления.
Выводы:
1. Применение газовых восстановителей водорода и оксида углерода не приводит к восстановлению оксида кальция.
2. Получение металлического кальция диссоциацией карбида кальция протекает в вакууме 1 Па при температурах не ниже 17500С. Образующаяся при этом сажа требует применения специальных мер при откачке и напуске воздуха.
3. При металлотермическом восстановлении выход кальция зависит от превышения температуры восстановления над температурой плавления (температурой ликвидуса) восстановителя и его индивидуальных свойств. Стоимость восстановителя может быть снижена, например, за счет введения в алюминий железного порошка.
Литература:
1. Обзор рынка кальция металлического в России и мире. http://www.infomine.ru. август 2011 г. — 102 с.
2. Кулифеев В. К., Кропачев А. Н., Божко Г. Г., Елсукова М. А. Термодинамический анализ системы CaCO3 — CaO — C при карботермическом восстановлении кальция в вакууме. Сб научн. трудов SWorld «Перспективные инновации в науке, образовании и транспорте» Одесса, 2012, вып.2, т.8, с.66–72.
3. http://www.chemservice.ru/materials/karbid_kalcija/ (дата обращения 19.08.13)
4. Пакет программ FACT-Win/F*A*C*T and ChemSage/SOLGASMIX — http://www.crct.polymtl.ca/fact/documentation/
5. Ватулин И. И., Минков О. Б., Сухарев А. В. и др. Высокотемпературное алюминотермическое восстановление оксида кальция.// Материаловедение, 2009, № 3, с.46–50.
6. Кулифеев В. К., Кропачев А. Н., Миклушевский В. В., Ватулин И. И. Технология алюминотермического получения кальция и аппаратное оформление процесса// Цветные металлы, 2004, № 10, с. 58–61.
7. Schwandt C. S., Cygan R. T., Westrich H. R. Ca self-diffusion in grossular garnet// American Mineralogist, 1996, vol. 81, pp. 448–451.
Ключевые слова
кальций, , восстановление оксида кальция, диссоциация карбида кальция, вакуумная печь, алюминотермическое и металлотермическое восстановление., алюминотермическое и металлотермическое восстановлениеПохожие статьи
Исследование процесса конверсии хлорида калия с нитратом...
9. Сушка выделенного хлорида кальция. Рис. 3. Принципиальная блок-схема технологии производства нитрата калия конверсионным методом.
Влияние объемной скорости исходной газовой смеси на выход... Исследование процесса конверсии хлорида калия с нитратом...
Формамидные координационные соединения ацетата кальция
Оксид цинка является прямозонным полупроводниковым соединением с шириной запрещенной зоны эВ у объемного образца и эВ у пленки при 300 К, n — типа проводимости.
По завершении реакции, смесь держали в течение 24 часов при комнатной температуре, что. Выход 65 %.
Иммерсионная цинкатная обработка алюминиевых изделий
Пленки оксида и гидроксида на поверхности металла, с одной стороны защищают его от
1) Нанесение тонкого металлического слоя химическим или электрохимическим способом.
Химическая иммерсия — процесс контактного восстановления металла с большим...
Технология получения ферратов, предусматривающая...
Другой метод анализа использовал Розе [8]. Он включал восстановление в растворе феррата калия, полученного электрохимическим окислением, газообразным диоксидом серы до оксида железа(Ш), отделение
Исследование процесса конверсии хлорида калия с нитратом кальция.
Получение чардж-хрома современным методом с использованием...
В целом использование кремнистых восстановителей для металлотермического процесса
Вокруг электродов выходит 10–15 % колошникового газа с температурой ~650°С. Давление
Получение чардж-хрома основано на восстановлении оксидов хрома и железа углеродом из...
Разработка автоматизированной системы управления процессом...
...с образованием свободной окиси кальция (CaO) и двуокиси углерода — углекислого газа (CO2) [13]: CaCO3= CaO+ CO2 Эта реакция обратимая и в зависимости от условий (температуры и давления) может идти в том и другом направлениях.
Техногенные ванадийсодержащие отходы и возможность их...
Выщелачивание этой шихты проводили при температуре 65–70
Махоткина Е. С., Шубина М. В. Шлаки процесса прямого восстановления железа как
В результате в зависимости от состава шлака, например, от содержания катионов кальция, возможно различное развитие процессов...
Возврат в процесс пыли кремниевого производства
– при восстановлении оксидов углеродом выделяемый высококалорийный газ может быть
1. Елкин К. С. Производство металлического кремния в России — состояние и перспективы
Электрическая печь для производства карбида кремния относится к типу электропечи...
О возможности комплексного использования доломитов...
Оксид кальция, полученный при низких температурах обжига, имел пониженную плотность и максимальную пористость. Время гашения его водой, характеризующее реакционную способность измеряется до температуры 800оС секундами.
Похожие статьи
Исследование процесса конверсии хлорида калия с нитратом...
9. Сушка выделенного хлорида кальция. Рис. 3. Принципиальная блок-схема технологии производства нитрата калия конверсионным методом.
Влияние объемной скорости исходной газовой смеси на выход... Исследование процесса конверсии хлорида калия с нитратом...
Формамидные координационные соединения ацетата кальция
Оксид цинка является прямозонным полупроводниковым соединением с шириной запрещенной зоны эВ у объемного образца и эВ у пленки при 300 К, n — типа проводимости.
По завершении реакции, смесь держали в течение 24 часов при комнатной температуре, что. Выход 65 %.
Иммерсионная цинкатная обработка алюминиевых изделий
Пленки оксида и гидроксида на поверхности металла, с одной стороны защищают его от
1) Нанесение тонкого металлического слоя химическим или электрохимическим способом.
Химическая иммерсия — процесс контактного восстановления металла с большим...
Технология получения ферратов, предусматривающая...
Другой метод анализа использовал Розе [8]. Он включал восстановление в растворе феррата калия, полученного электрохимическим окислением, газообразным диоксидом серы до оксида железа(Ш), отделение
Исследование процесса конверсии хлорида калия с нитратом кальция.
Получение чардж-хрома современным методом с использованием...
В целом использование кремнистых восстановителей для металлотермического процесса
Вокруг электродов выходит 10–15 % колошникового газа с температурой ~650°С. Давление
Получение чардж-хрома основано на восстановлении оксидов хрома и железа углеродом из...
Разработка автоматизированной системы управления процессом...
...с образованием свободной окиси кальция (CaO) и двуокиси углерода — углекислого газа (CO2) [13]: CaCO3= CaO+ CO2 Эта реакция обратимая и в зависимости от условий (температуры и давления) может идти в том и другом направлениях.
Техногенные ванадийсодержащие отходы и возможность их...
Выщелачивание этой шихты проводили при температуре 65–70
Махоткина Е. С., Шубина М. В. Шлаки процесса прямого восстановления железа как
В результате в зависимости от состава шлака, например, от содержания катионов кальция, возможно различное развитие процессов...
Возврат в процесс пыли кремниевого производства
– при восстановлении оксидов углеродом выделяемый высококалорийный газ может быть
1. Елкин К. С. Производство металлического кремния в России — состояние и перспективы
Электрическая печь для производства карбида кремния относится к типу электропечи...
О возможности комплексного использования доломитов...
Оксид кальция, полученный при низких температурах обжига, имел пониженную плотность и максимальную пористость. Время гашения его водой, характеризующее реакционную способность измеряется до температуры 800оС секундами.











