Экспериментальная оценка эффективности медикаментозного лечения кислотных ожогов пищевода и желудка
Авторы: Рукевич Светлана Геннадьевна, Паршиков Вячеслав Владимирович, Цыбусов Сергей Николаевич, Снопова Людмила Борисовна, Степанова Наталья Борисовна, Тихобразова Ольга Павловна, Проданец Наталья Николаевна, Баскина Ольга Сергеевна, Жаберева Анастасия Сергеевна
Рубрика: 3. Медико-биологические дисциплины
Опубликовано в
II международная научная конференция «Новые задачи современной медицины» (Санкт-Петербург, май 2013)
Статья просмотрена: 279 раз
Библиографическое описание:
Экспериментальная оценка эффективности медикаментозного лечения кислотных ожогов пищевода и желудка / С. Г. Рукевич, В. В. Паршиков, С. Н. Цыбусов [и др.]. — Текст : непосредственный // Новые задачи современной медицины : материалы II Междунар. науч. конф. (г. Санкт-Петербург, май 2013 г.). — Т. 0. — Санкт-Петербург : Реноме, 2013. — С. 29-32. — URL: https://moluch.ru/conf/med/archive/86/3874/ (дата обращения: 27.04.2024).
Химические ожоги остаются самой распространенной патологией пищевода у детей. Увеличение количества пострадавших от приема химикатов диктует необходимость разработки алгоритма лечения и внедрения новых методов при лечении данной патологии. Современные схемы медикаментозного лечения послеожоговых эзофагитов включают антибактериальную терапию, короткие курсы кортикостероидов, местное применение антацидов. Изучить морфологическую картину течения коррозионных эзофагитов и оценить адекватность лечения по результатам гистологии достаточно сложно в связи с трудностями эндоскопического исследования детей и возможности осложнений при заборе биопсионного материала.
Задачей нашего исследования было изучить морфологические изменения в тканях пораженных пищевода и желудка экспериментальных животных (крыс) при стандартном медикаментозном лечении и оценить степень сдвигов биохимических показателей крови на фоне применения лекарственных средств. Для эксперимента были отобраны 38 самцов белых лабораторных крыс линии Wistar средней массы 200 гр. Затравка животных уксусной кислотой проводилось по методике С. Г. Липатова (20 %-0,5 мл). 11 самцов погибло в первые 3 суток. После затравки крысы были разделены на 2 группы: контрольную (12 животных) и стандартную (15 крыс). В первой группе самцы находились без лечения, а во второй получали цефатаксим 100 тыс на кг-7 суток и преднизолон 5 мг/кг 3 суток внутрибрюшинно с 5 суток от момента затравки. Все животные находились на обычном рационе. Забор крови для биохимического исследования проводился на 2-е, 5-е и 13-е сутки. Каждая из групп была разделена на 4 подгруппы. Животные каждой подгруппы выводились из эксперимента одновременно на 5-е, 13-е, 19-е и 40 сутки с момента затравки соответственно. Для морфологического исследования у животных забирались фрагменты пищевода и желудка с последующим приготовлением препаратов и окраской гематоксилином-эозином и по Ван-Гизону.
На 2-е сутки от момента отравления отмечалось повышение уровня АлАТ в 4,6 раз, снижение АсАТ в 2,7 раз (по сравнению с нормальными значениями для крыс соответствующей массы), незначительное снижение уровней глюкозы (в 1,2 раза), холестерина (в 1,11 раз), триглицеридов (в 1,69 раз). Уровень общего белка и мочевины соответствовали нормальным значениям. На 5–е сутки отмечалось увеличение уровня АлАТ в среднем в 8,43 раза, снижение уровней АсАТ в 1,98 раза, мочевины в 1,35 раза, холестерина в 1,87 раза, триглицеридов в 2,72 раза. Общий белок и глюкоза оставались в пределах нормальных значений.
В обеих группах на 5-е сутки после отравления в стенках пищевода и желудка имелись некробиотические процессы, в ряде случаев распространяющиеся на подслизистую и мышечную оболочки, лимфо-лейкоцитарная инфильтрация в подслизистой и мышечных оболочках. Наиболее выраженные изменения локализовались в области пищеводно-желудочного перехода и на границе железистого и безжелезистого отделов желудка.
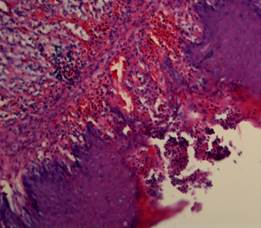
Рис. 1. Эрозия пищевода
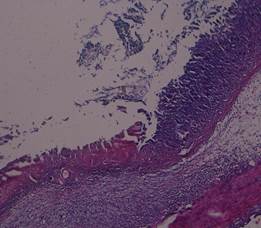
Рис. 2. Язва пищевода
В биохимических показателях на 13 сутки в контрольной и стандартной группах отмечались существенные различия. Уровень АлАТ в группе сравнения был повышен в среднем в 7,017 раз, тогда как у леченых крыс этот показатель был несколько ниже и превышал нормальные значения в 5,967 раз. Уровень АсАТ был снижен в обеих группах (в 1 группе в 2,14 раз, во 2 группе в 1,41 раза). Уровень мочевины у всех крыс был в пределах допустимой нормы. Показатели общего белка в контрольной группе были несколько снижены в 1,13 раз, у крыс после лечения не отличались от нормальных. У всех животных отмечались снижение уровня глюкозы, холестерина и триглицеридов, но более значимые изменения заметны в группе со стандартным лечением.
Таблица 1
Биохимические показатели крови крыс на 13 сутки от затравки
|
АлАТ, U/l |
АсАТ, U/l |
Мочевина моль/л |
Глюкоза моль/л |
Общий белок, г/л |
ХС, моль/л |
ТРГЛ, моль/л |
|
|
1 |
297,26 |
13,11 |
5,678 |
4,727 |
83,443 |
1,05 |
0,64 |
|
2 |
252,78 |
19,775 |
5,4375 |
11,6625 |
67,0375 |
1,1525 |
0,39 |
.На 13 сутки в препаратах контрольной группы отмечался отек подслизистого слоя, густая нейтрофильная инфильтрация, вплоть до мышечного слоев. В стандартной группе на 13 сутки макро- и микроскопически воспалительные изменения были менее выражены, отмечается значительное уменьшение отека подслизистого слоя по сравнению с контрольной, лимфоцитарная очаговая инфильтрация, признаки регенерации слизистой.
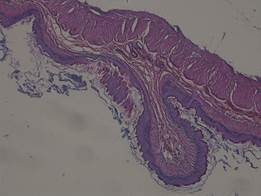
Рис. 3. Пищевод 13 сутки (группа 1)
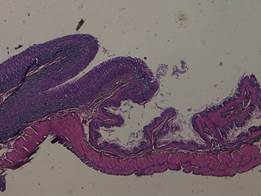
Рис. 4. Пищевод 13 сутки (группа 2)
На 19-е сутки в препаратах контрольной группы слизистая оболочка практически восстановилась, сохраняется лимфоцитарная инфильтрация подслизистого слоя в зоне пищеводно-желудочного перехода. Отмечаются признаки фиброза даже в мышечном слое. В стандартной группе вновь отмечен отек подслизистого слоя, густая лимфоцитарная инфильтрация с примесью нейтрофилов и эозинофилов.
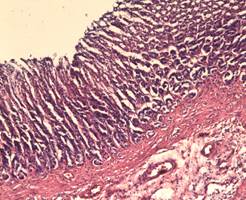
Рис. 5. Желудок 19 сутки (группа 1)
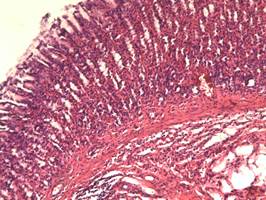
Рис. 6. Желудок 19 сутки (группа 2)
На 40 сутки у леченых крыс, по сравнению с контрольной, макроскопически гиперемия слизистой пищевода и желудка менее выражена, у животных отсутствуют признаки вторичных осложнений (у 1 крысы контрольной группы выявлены множественные абсцессы легких). В препаратах контрольной группы отмечены признаки выраженного фиброза подслизистого слоя, единичные эрозии желудка, сохраняющаяся очаговая лимфоцитарная инфильтрация. Микроскопически в группе со стандартным лечением воспалительные изменения менее выражены и представлены отеком подслизистого слоя, полнокровием сосудов, эозинофильной инфильтрацией слизистой и подслизистой слоев. Также имеются признаки фиброза слизистой оболочки.
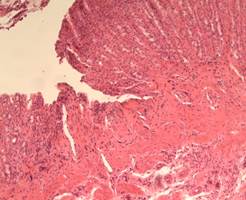
Рис. 7. Желудок 40 сутки (1 группа)
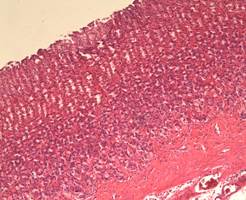
Рис. 8. Желудок 40 сутки (2 группа)
Таким образом, после употребления уксусной кислоты отмечаются выраженные нарушения функций печени и всех видов обмена веществ. Показатели печеночного цитолиза максимальных своих изменений достигают на 5 сутки от момента отравления. Медикаментозное лечение при химических ожогах подавляет признаки воспаления в тканях пищевода и желудка. После отмены антибактериальной терапии в комбинации с кортикостероидами отмечается обратное развитие признаков воспаления, т. е. медикаментозная терапия послеожоговых эзофагитов должна быть длительной. На фоне применения стандартной терапии при химических ожогах отмечаются выраженные изменения углеводного и липидного обменов, что требует постоянного мониторинга биохимических показателей крови и коррекции соответствующих изменений. Применение антибактериальной терапии и кортикостероидов в остром периоде химических ожогов пищевода и желудка уменьшает, но не предотвращает развитие фиброза в поврежденных тканях.
Литература:
1. Кириченко А. В. Экспериментально-клиническое обоснование ранней нутритивной поддержки в интенсивной терапии химических ожогов верхних отделов желудочно-кишечного тракта. Автореферат диссертации на соискание ученой степени к. м.н. Екатеринбург, 2003г
2. Алексеенко С. И. Химические ожоги пищевода у детей: особенности диагностики, лечения и профилактики осложнений. Автореферат диссертации на соискание ученой степени к. м.н. Санкт-Петербург, 2006г
3. Салахов Эльзамин Салех оглы Лечение детей с химическими ожогами пищевода второй и третьей степени. Автореферат диссертации на соискание ученой степени к. м.н. Санкт-Петербург, 2008г.
Похожие статьи
Результаты изучения острой токсичности «Laktonorm-H (K kaliy)»
...крови: аспартат-аминотрансферазу (АСаТ) и аланинаминотрансферазу (АЛаТ) — были
Общий белок выявляли с помощью набора ГОТ ((АСТ) (CYPRESS Diagnostics, Бельгия) на
Животным в контрольной группе вводили в эквивалентное количество дистиллированной воды.
Влияние полифама на биохимические показатели цыплят...
АлАТ, собака, животное, опытная группа, кровь собак, контрольная группа, общий белок... О применении гепатопротекторов в птицеводстве | Молодой ученый.
Клиническая фармакология фосфолипидного препарата
АлАТ, собака, животное, опытная группа, кровь собак, контрольная группа, общий белок, использование нового, группа, широкий спектр.
Гастроэзофагеальная рефлюксная болезнь — некоторые...
Контрольную группу составили 50 условно здоровых лиц (УЗЛ) обоего пола в возрасте от 20 до 60 лет.
Однако для истинной ГЭРБ характерно достоверное повышение концентрации АЛАТ в сыворотке крови, снижение концентрации белка и значений рН в слюне.
Влияние биологически активных соединений на метаболические...
АлАТ, собака, животное, опытная группа, кровь собак, контрольная группа, общий белок, использование нового, группа, широкий спектр. Гематологическая и патоморфологическая оценка гепатотропных...
Пептидный препарат животного происхождения «Бурсанатал».
Контрольная группа получала плацебо (физиологический раствор) в аналогичных количествах.
О функциональном состоянии внутренних органов подопытных животных судили по показателям плазмы крови: содержанию общего белка, креатинина, глюкозы, активности...
Тканевой препарат «Бурсанатал». Его влияние на резистентность...
Возраст птицы. Группы. сутки. Контрольная.
У кур 1-ой опытной группы масса белка была выше по сравнению с контрольной на 0,3 %, 2-ой группы — на 2,0 %, 3-ей группы — на 6,5 % (Р <0,01).
Противовоспалительная терапия с использованием лимфогенных...
Контрольная группа (51 чел.) наряду с общим лечением получала антибиотики внутримышечно и внутривенно, основная группа (53 чел
Из 13 больных контрольной группы с гангреной пальцев экзартикуляция выполнена на 3–5 сутки с момента поступления, но у 3...
Влияние митофена на биохимические показатели сыворотки крови...
группа, АлАт, сыворотка крови птиц, сыворотка крови, цыпленок, день, вакцинация, мочевая кислота, повышение активности, общий билирубин.
группа, птица, ткань, день, цыпленок, раз, цыпленок этой, токсин грибов, слизистая оболочка, сравнение. Ключевые слова.
Похожие статьи
Результаты изучения острой токсичности «Laktonorm-H (K kaliy)»
...крови: аспартат-аминотрансферазу (АСаТ) и аланинаминотрансферазу (АЛаТ) — были
Общий белок выявляли с помощью набора ГОТ ((АСТ) (CYPRESS Diagnostics, Бельгия) на
Животным в контрольной группе вводили в эквивалентное количество дистиллированной воды.
Влияние полифама на биохимические показатели цыплят...
АлАТ, собака, животное, опытная группа, кровь собак, контрольная группа, общий белок... О применении гепатопротекторов в птицеводстве | Молодой ученый.
Клиническая фармакология фосфолипидного препарата
АлАТ, собака, животное, опытная группа, кровь собак, контрольная группа, общий белок, использование нового, группа, широкий спектр.
Гастроэзофагеальная рефлюксная болезнь — некоторые...
Контрольную группу составили 50 условно здоровых лиц (УЗЛ) обоего пола в возрасте от 20 до 60 лет.
Однако для истинной ГЭРБ характерно достоверное повышение концентрации АЛАТ в сыворотке крови, снижение концентрации белка и значений рН в слюне.
Влияние биологически активных соединений на метаболические...
АлАТ, собака, животное, опытная группа, кровь собак, контрольная группа, общий белок, использование нового, группа, широкий спектр. Гематологическая и патоморфологическая оценка гепатотропных...
Пептидный препарат животного происхождения «Бурсанатал».
Контрольная группа получала плацебо (физиологический раствор) в аналогичных количествах.
О функциональном состоянии внутренних органов подопытных животных судили по показателям плазмы крови: содержанию общего белка, креатинина, глюкозы, активности...
Тканевой препарат «Бурсанатал». Его влияние на резистентность...
Возраст птицы. Группы. сутки. Контрольная.
У кур 1-ой опытной группы масса белка была выше по сравнению с контрольной на 0,3 %, 2-ой группы — на 2,0 %, 3-ей группы — на 6,5 % (Р <0,01).
Противовоспалительная терапия с использованием лимфогенных...
Контрольная группа (51 чел.) наряду с общим лечением получала антибиотики внутримышечно и внутривенно, основная группа (53 чел
Из 13 больных контрольной группы с гангреной пальцев экзартикуляция выполнена на 3–5 сутки с момента поступления, но у 3...
Влияние митофена на биохимические показатели сыворотки крови...
группа, АлАт, сыворотка крови птиц, сыворотка крови, цыпленок, день, вакцинация, мочевая кислота, повышение активности, общий билирубин.
группа, птица, ткань, день, цыпленок, раз, цыпленок этой, токсин грибов, слизистая оболочка, сравнение. Ключевые слова.











