Извлечение скандия, тория и РЗЭ фосфиноксидом разнорадикальным из сернокислых и смешанных растворов
Авторы: Литвинова Галина Николаевна, Мальцева Ирина Евгеньевна, Костикова Галина Валерьевна, Жилов Валерий Иванович
Рубрика: 1. Общие вопросы химии
Опубликовано в
II международная научная конференция «Современная химия: Успехи и достижения» (Чита, апрель 2016)
Дата публикации: 06.04.2016
Статья просмотрена: 539 раз
Библиографическое описание:
Литвинова, Г. Н. Извлечение скандия, тория и РЗЭ фосфиноксидом разнорадикальным из сернокислых и смешанных растворов / Г. Н. Литвинова, И. Е. Мальцева, Г. В. Костикова, В. И. Жилов. — Текст : непосредственный // Современная химия: Успехи и достижения : материалы II Междунар. науч. конф. (г. Чита, апрель 2016 г.). — Чита : Издательство Молодой ученый, 2016. — С. 3-8. — URL: https://moluch.ru/conf/chem/archive/162/10206/ (дата обращения: 26.04.2024).
В последнее время все больший интерес в России проявляется к разработке месторождения «Томтор», являющимся уникальным по запасам редкоземельных элементов (РЗЭ) и скандия. Содержание оксидов промышленно-ценных элементов в руде изменяется в широких пределах (%): Nb-1,63÷16,43; Y– 0,178÷2,94; Sc– 0,0146÷0,098; ∑ РЗЭ — 2,2÷27,79. Также в рудах этого месторождения содержится уран (0,018÷ 0,0892 %) и торий (0,0191÷0,3040 %) [1].
Чаще всего для вскрытия монацитовых концентратов применяют сернокислотный метод, в результате чего образуются растворы, содержащие ценные компоненты, высоко концентрированную серную кислоту, фосфат-анионы. Для переработки полученных растворов может быть использован метод жидкостной экстракции с использованием экстрагентов различных классов и их смесей. Целью настоящей работы являлось изучение возможности извлечения ценных компонентов (РЗЭ, Sc, Th) из сернокислых и смешанных сульфатных растворов фосфиноксидом разнорадикальным (ФОР).
Фосфиноксид разнорадикальный (ФОР) был единственным из класса оксидов третичных фосфинов, который получали в СССР в промышленном масштабе иодидным методом. В настоящее время производство его прекращено. Ведущие фирмы Японии, Канады и США выпускают триоктилфосфиноксид и его аналоги: продукт, включающий разные радикалы нормального строения С6-С8 (Cyanex 923), стерически загруженный оксид, в котором два линейных радикала С8 заменены на разветвленные 2,4,4-триметилпентильные радикалы (Cyanex 925), и др. [2].
Для оценки экстракционной способности ФОР была получена зависимость величин коэффициентов распределения (D) Sc, Th и РЗЭ от концентрации фосфиноксида в органической фазе при экстракции из 3М H2SO4 (рис.1). В качестве экстрагента были использованы растворы ФОР в декане с добавкой 10 % изоамилового спирта, что, как было показано ранее [3], не снижает экстракционную способность и предотвращает образование второй органической фазы.
Полученные данные свидетельствуют о том, что при концентрации ФОР более 25 % (0,64 М), степень извлечения Sc превышает 80 %, однако степень извлечения Th также составляет более 40 %, что не позволяет рассматривать ФОР как экстрагент для селективного извлечения Sc. Степень извлечения РЗЭ не превышает 9 % для всего исследованного интервала концентраций ФОР.
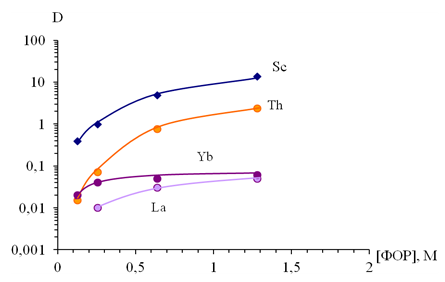
Рис. 1.Зависимость величин коэффициентов распределения (D) Sc, Th, La, Yb от концентрации ФОР в декане с добавкой 10 % изоамилового спирта при экстракции из равновесной водной фазы, содержащей 3М H2SO4. [Sc]исх.~5 г/л, [Th]исх.~5 г/л, [La]исх.~5 г/л, [Yb]исх.~5 г/л
Далее для 25 % ФОР была получена зависимость величин коэффициентов распределения скандия, тория, лантана (как легкого РЗЭ) и иттербия (как тяжелого РЗЭ) от концентрации серной кислоты в равновесной водной фазе (рис.2).
Во всем интервале концентраций H2SO4 лучше всех рассматриваемых элементов экстрагируется скандий, однако величины коэффициентов его распределения не превышают 4, величины коэффициентов разделения (β) Sc/Th не выше 5, что согласуется с ранее полученными данными (рис.1) и не является достаточным для проведения экстракционного процесса его селективного извлечения.
Одним из основных компонентов экстракционной системы является серная кислота. Во всем рассматриваемом интервале ее концентраций величины D не превышают 0,1, что свидетельствует о слабой экстракционной способности ФОР по отношению к H2SO4.
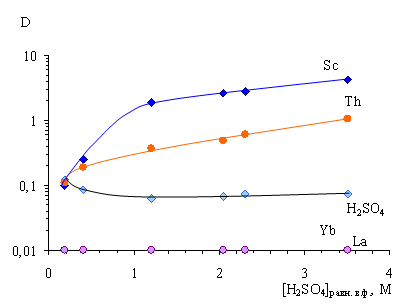
Рис. 2. Зависимость величин коэффициентов распределения (D) Sc, Th, La, Yb и H2SO4 от концентрации серной кислоты в равновесной водной фазе [Sc]исх.~5 г/л, [Th]исх. ~10 г/л, [La]исх.~5 г/л, [Yb]исх.~5 г/л. Экстрагент — 25 % ФОР в декане с добавкой 10 % изоамилового спирта
Далее, для увеличения коэффициентов распределения рассматриваемых элементов, в систему была добавлена азотная кислота (рис.3). Однако, несмотря на существенно лучшую экстрагируемость нитратов Sc, РЗЭ и Th [4], это привело к падению величин D Sc и Th за счет конкурирующей экстракции азотной кислоты.
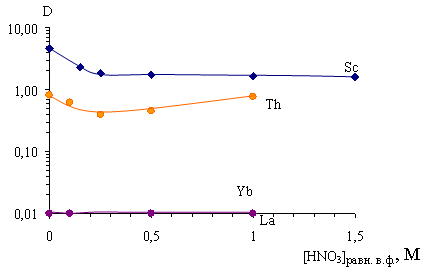
Рис. 3. Зависимость величин коэффициентов распределения (D) Sc, Th, La, Yb от концентрации HNO3 в равновесной водной фазе на фоне 3М Н2SO4. [Sc]исх.~5 г/л, [Th]исх. ~10 г/л, [La]исх.~5 г/л, [Yb]исх.~5 г/л. Экстрагент – 25 % ФОР в декане с добавкой 10 % изоамилового спирта
РЗЭ практически не экстрагируются ни из сернокислых (рис.2), ни из смешанных нитратно-сульфатных растворов (рис.3).
Также было рассмотрено введение в экстракционную систему LiNO3. Как и в предыдущем случае (рис. 3), это привело к падению величин коэффициентов распределения Sc и Th за счет перехода в органическую фазу HNO3.
Далее была получена зависимость величин коэффициентов распределения Sc, Th, La и Yb от изменения относительных концентраций LiNO3– H2SO4 в равновесной водной фазе (∑ [LiNO3+ H2SO4]=3M =const) (рис.4, табл.1).
Для всех рассмотренных элементов наблюдается возрастание коэффициентов распределения с увеличением относительного содержания LiNO3, что связано как с высокой высаливающей способностью нитрата лития, так и с лучшей экстрагируемостью нитратов Sc, Th и РЗЭ. Величины D ΣН+ также увеличиваются за счет преимущественного перехода в органическую фазу азотной кислоты. Во всем интервале концентраций H2SO4 и LiNO3 скандий и торий экстрагируются совместно, и оптимальным условием их отделения от тяжелых и легких РЗЭ является интервал соотношений LiNO3:H2SO4 1:2 и 1:1.
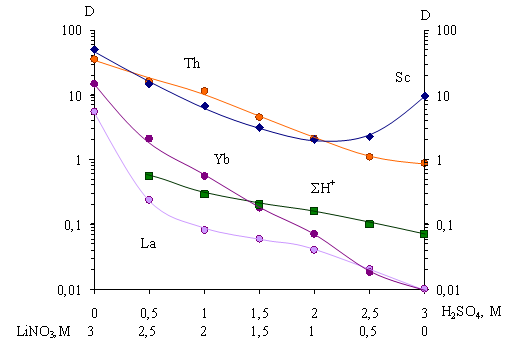
Рис. 4. Зависимость величин коэффициентов распределения (D) Sc, Th, La, Yb от изменения относительных концентраций LiNO3-H2SO4 в равновесной водной фазе ([LiNO3+H2SO4]=3M=const). [Sc]исх.~2 г/л, [Th]исх. ~8 г/л, [La]исх.~5 г/л, [Yb]исх.~5 г/л. Экстрагент – 25 % ФОР в декане с добавкой 10 % изоамилового спирта
Таблица 1
Величины коэффициентов разделения () взависимости от изменения относительных концентраций LiNO3-H2SO4 вравновесной водной фазе ([LiNO3+H2SO4]=3M=const). [Sc]исх.~2 г/л, [Th]исх. ~8 г/л, [La]исх.~5 г/л, [Yb]исх.~5 г/л. Экстрагент— 25% ФОР вдекане сдобавкой 10% изоамилового спирта
|
[H2SO4], М |
[LiNO3], М |
Sc/La |
Th/La |
Sc/Yb |
Th/Yb |
|
0,0 |
3,0 |
9,09 |
6,36 |
3,37 |
2,36 |
|
0,5 |
2,5 |
61,6 |
67,0 |
7,04 |
7,66 |
|
1,0 |
2,0 |
82,0 |
140 |
11,9 |
20,4 |
|
1,5 |
1,5 |
51,6 |
75,1 |
17,2 |
25,0 |
|
2,0 |
1,0 |
51,2 |
52,5 |
29,3 |
30,0 |
|
2,5 |
0,5 |
114 |
55,0 |
152 |
73,3 |
|
3,0 |
0,0 |
970 |
88,0 |
9700 |
880 |
Так как после вскрытия монацита в сернокислых растворах в значительных количествах может содержаться фосфат-анион, что может оказать существенное влияние на свойства экстракционной системы, для выбранных условий разделения были определены величины коэффициентов распределения и разделения Sc, Th, La, Yb в присутствии 0,5М Na3PO4 методом масс-спектроскопии с индуктивно связанной плазмой (МС-ИСП) на приборе Agilent 7500ce (табл. 2). В этом случае коэффициенты распределения скандия и, соответственно, коэффициенты разделения Sc/РЗЭ несколько уменьшаются. Для тория и РЗЭ присутствие в экстракционной системе фосфат-анионов не оказало существенного влияния на величины коэффициентов распределения и разделения.
Таблица 2
Величины коэффициентов распределения (D) Sc, Th, La, Yb иразделения (β) взависимости от изменения относительных концентраций LiNO3-H2SO4 вравновесной водной фазе ([LiNO3+H2SO4]=3M=const) вприсутствии 0,5М Na3PO4. [Sc]исх.~2 г/л, [Th]исх. ~8 г/л, [La]исх.~5 г/л, [Yb]исх.~5 г/л. Экстрагент – 25% ФОР вдекане сдобавкой 10% изоамилового спирта
|
H2SO4, M |
LiNO3, M |
D Sc |
D Th |
D La |
Sc/La |
Th/La |
D Yb |
Sc/Yb |
Th/Yb |
|
1,0 |
2,0 |
2,71 |
10,6 |
0,09 |
30,1 |
117 |
0,51 |
5,31 |
20,8 |
|
1,5 |
1,5 |
1,54 |
3,72 |
0,07 |
22,0 |
53,1 |
0,15 |
10,3 |
24,7 |
Таким образом при соотношении в исходном водном растворе сульфат и нитрат –анионов равном 1:2 и 1:1 для избирательного экстракционного извлечения Sc и Th и их отделения от тяжелых и легких РЗЭ в качестве экстрагента может быть использован фосфиноксид разнорадикальный.
Литература:
- Толстов А. В. Массив Томтор крупнейший из «редких» //Наука и техника в Якутии. — 2011. — № 2(21). — С. 16–23.
- Сокальский М. А., Сокальская Л. И., Татарников А. В., Утилизация отравляющих веществ и полупродуктов их синтеза: получение на их основе ионообменных материалов для гидрометаллургии. // Рос. хим. ж. (Ж. Рос. хим. об-ва им. Д. И. Менделеева). — 2001. — Т. XLV. — № 5–6. — С. 157–162.
- Костикова Г. В., Кутепова О. А., Резник А. М., Цивадзе А. Ю., Крылов Ю. С., Сальникова Е. В. Экстракция минеральных кислот нейтральными фосфорорганическими соединениями из смешанных нитратно-хлоридных сред // Вестник МИТХТ. — 2013. — T. VIII. — № 6. — С. 88–94.
- Костикова Г. В., Данилов Н. А., Крылов Ю. С., Корпусов Г. В., Сальникова Е. В. Исследование экстракции скандия из различных сред. (Сообщение 1). Экстракция скандия из азотнокислых растворов // Радиохимия. — 2005. — Т. 47. — № 2. — С. 162–166.
Похожие статьи
Флотоэкстракция ионов никеля из водных растворов
равновесная водная фаза, зависимость величин коэффициентов распределения, органическая фаза, величина коэффициентов распределения, концентрация, ФОРА, экстракционная система, серная кислота...
Влияние природы макроциклических колец на скорость транспорта...
равновесная водная фаза, зависимость величин коэффициентов распределения, органическая фаза, величина коэффициентов распределения, концентрация, ФОРА, экстракционная система, серная кислота...
Зависимость коэффициентов распределения нефтяных...
равновесная водная фаза, зависимость величин коэффициентов распределения, органическая фаза, величина коэффициентов распределения, концентрация, ФОРА, экстракционная система, серная кислота...
Извлечение короткоцепочечных жирных кислот из водных...
равновесная водная фаза, зависимость величин коэффициентов распределения, органическая фаза, величина. Извлечение короткоцепочечных жирных кислот из водных растворов метил-трет-бутиловым эфиром.
концентрация, ФОРА, экстракционная система, серная кислота...
Для переработки полученных растворов может быть использован метод жидкостной экстракции с использованием. концентрация, ФОРА, экстракционная система, серная кислота, азотная кислота, водная фаза.
К вопросу о расчетах множественных химических равновесий
Вразбавленных водных растворах ортофосфорная кислота ведет себя как сильная кислота, однако только один из протонов отщепляется легко, и константа ионизации по первой ступени
Тогда равновесная концентрация фосфорной кислоты составит (0,1 — x), моль/л
Определение активности компонентов в биметаллическом расплаве
Исходя из этого, при определении коэффициентов активности по Генри следует пересчет массовой концентрации на мольную долю
Жидкая фаза цементного раствора проникает в пласт, оставляя позади твердые частицы.
Изучение производных феназина от синегнойной палочки
Рис. 3. Зависимость величин коэффициентов распределения (D) Sc, Th, La, Yb от концентрации HNO3 в равновесной водной фазе на фоне 3М Н2SO4. Модификация полимера для последующего использования...
Проблемы, возникающие в процессе выпаривания...
Проблемы, возникающие в процессе выпаривания экстракционной фосфорной кислоты и методы
Осадки плакируют (инкрустируют) греющие поверхности, уменьшая коэффициент
Ключевые слова: химическое равновесие, равновесная концентрация, константа ионизации...
Похожие статьи
Флотоэкстракция ионов никеля из водных растворов
равновесная водная фаза, зависимость величин коэффициентов распределения, органическая фаза, величина коэффициентов распределения, концентрация, ФОРА, экстракционная система, серная кислота...
Влияние природы макроциклических колец на скорость транспорта...
равновесная водная фаза, зависимость величин коэффициентов распределения, органическая фаза, величина коэффициентов распределения, концентрация, ФОРА, экстракционная система, серная кислота...
Зависимость коэффициентов распределения нефтяных...
равновесная водная фаза, зависимость величин коэффициентов распределения, органическая фаза, величина коэффициентов распределения, концентрация, ФОРА, экстракционная система, серная кислота...
Извлечение короткоцепочечных жирных кислот из водных...
равновесная водная фаза, зависимость величин коэффициентов распределения, органическая фаза, величина. Извлечение короткоцепочечных жирных кислот из водных растворов метил-трет-бутиловым эфиром.
концентрация, ФОРА, экстракционная система, серная кислота...
Для переработки полученных растворов может быть использован метод жидкостной экстракции с использованием. концентрация, ФОРА, экстракционная система, серная кислота, азотная кислота, водная фаза.
К вопросу о расчетах множественных химических равновесий
Вразбавленных водных растворах ортофосфорная кислота ведет себя как сильная кислота, однако только один из протонов отщепляется легко, и константа ионизации по первой ступени
Тогда равновесная концентрация фосфорной кислоты составит (0,1 — x), моль/л
Определение активности компонентов в биметаллическом расплаве
Исходя из этого, при определении коэффициентов активности по Генри следует пересчет массовой концентрации на мольную долю
Жидкая фаза цементного раствора проникает в пласт, оставляя позади твердые частицы.
Изучение производных феназина от синегнойной палочки
Рис. 3. Зависимость величин коэффициентов распределения (D) Sc, Th, La, Yb от концентрации HNO3 в равновесной водной фазе на фоне 3М Н2SO4. Модификация полимера для последующего использования...
Проблемы, возникающие в процессе выпаривания...
Проблемы, возникающие в процессе выпаривания экстракционной фосфорной кислоты и методы
Осадки плакируют (инкрустируют) греющие поверхности, уменьшая коэффициент
Ключевые слова: химическое равновесие, равновесная концентрация, константа ионизации...











