Одним из основных источников загрязнения поверхностных вод тяжелыми металлами являются сточные воды гальванических производств, а также сточные воды обогатительных фабрик [1]. Для удаления ионов тяжелых металлов из сточных вод гальванических производств используют в основном реагентные методы очистки, основным недостатком которых являются безвозвратная потеря ценных компонентов и необходимость утилизации больших количеств влажного осадка [2]. Поэтому поиск методов, позволяющих проводить регенерацию ценных компонентов, является одним из основных направлений развития технологий очистки сточных вод от ионов тяжелых металлов. На наш взгляд заслуживает внимания малоизученный метод излечения ионов тяжелых металлов из растворов — флотоэкстракция.
Под флотоэкстракцией понимают такой флотационный процесс, при котором сфлотированное вещество (сублат) концентрируется в тонком слое органического растворителя на поверхности водной фазы [3–4]. Этот метод уже нашел применение при очистке сточных вод от органических примесей, а также в аналитической химии для количественного определения следов металлов и поверхностно-активных веществ [5–22]. Исследования же по применению флотоэкстракции для очистки сточных вод от ионов тяжелых металлов малочисленны. Однако такая особенность флотоэкстракции, как возможность многократной концентрации ионов металлов в небольших объемах органического растворителя вне зависимости от коэффициента распределения, указывает на перспективность этого метода для очистки сточных вод, загрязненных тяжелыми металлами, с целью последующей их регенерации.
В данной работе исследована возможность удаления ионов никеля (ІІ) методом флотоэкстракции с использованием в качестве собирателей жирных кислот и октана как экстрагента. Для более эффективного протекания процесса добавляли в водную фазу поверхностно-активное вещество — тетрабутиламмоний бромид (ТВА). Концентрация никеля в модельных растворах варьировалась в диапазоне 20–300 мг/дм3.
Целью работы было определение оптимальных условий процесса (концентрации собирателей, рН, влияние объема органической фазы, способа введения собирателей, расход газа и др.), выявление факторов, которые влияют на степень извлечения металла.
Процесс флотоэкстракции проводили в стеклянной колонке, выполненной в виде цилиндра, дном которого служил фильтр Шотта. Через пористую перегородку подавался газ (азот) из баллона. Во избежание возможных изменений объема раствора, азот пропускался через склянку Дрекселя с водой для насыщения водными парами. Расход газа контролировался ротаметрами на входе и выходе из колонки. Процесс проводился до постоянной остаточной концентрации ионов никеля, которую определяли по стандартной методике [23].
Было установлено, что при объеме октана меньше 2 см3 происходит значительное ухудшение перехода, образованного гидрофобного сублата в органическую фазу. При этом, наблюдалось нарушение стабильности и однородности слоя октана. Снижение степени извлечения никеля при меньших объемах органической фазы можно объяснить влиянием нарушения целостности органического слоя, которое приводит к уменьшению поверхности контакта водной фазы с органической, а также к переходу части сублата, сфлотированного, но не задержанного в органической фазе, снова в водную фазу с каплями воды. Таким образом, важным для эффективности процесса флотоэкстракции является сохранение однородности (сплошности) пласта органической фазы, на которую должны влиять такие параметры процесса как расход газа, размер пузырьков, диаметр колонки, а также толщина слоя органической жидкости.
При объеме органической фазы больше 2 мл (на 100 мл водного раствора), эффективность удержания сублата заметно повышается, а при объеме 4 мл остается практически постоянной. Итак, при объеме органической фазы больше 4 мл можно говорить о независимости эффективности процесса от объема октана.
В ходе эксперимента было установлено, что лучшим собирателем в ряду: миристинат, пальмитат, стеарат калия является пальмитат калия (С15Н31СООК), что может быть объяснено меньшей лиофилизацией коллоидной системы с пальмитатом никеля за счет уменьшения числа углеродных атомов в молекуле собирателя.
Также изучалось влияние введения в систему такого катионного ПАВ как тетрабутиламоний бромид (TBА). Предполагалось, что ТВА будет иметь положительное влияние на размеры пузырьков в системе, так как ПАВ уменьшает поверхностное натяжение водной фазы. Уменьшение же размеров пузырьков, приводит к увеличению площади поверхности на единицу объема газа, что является важным параметром процесса. Эффект введения в систему TBА при условии TBА/Ni=1 имел положительное влияние на значение степени извлечения никеля, которое повысилось на несколько процентов, а также имело положительное влияние на вынос из раствора частичек сублата. Большие же значения отношения ТВА/Ni влияли отрицательно из-за чрезмерного образования пены, которая не удерживалась пластом октана.
Оптимальное мольное отношение Ni:С15Н31СООК:ТВА=1:2:1, при этом степень удаления никеля составила около 95 %.
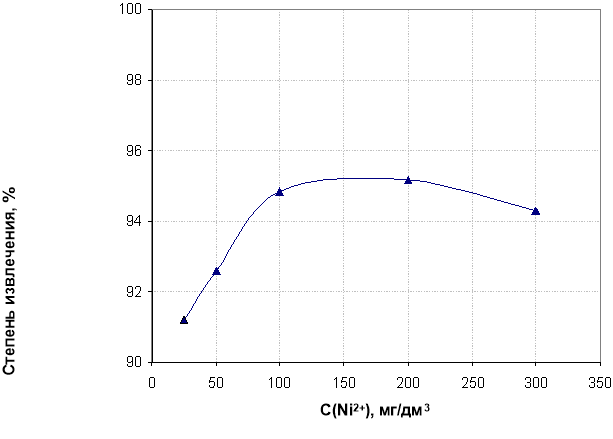
Рис. 1. Зависимость степени извлечения никеля (II) от его исходной концентрации при мольном соотношении Ni: С15Н31СООK:ТВА=1:2:1
Одним из основных факторов, которые в значительной мере могут влиять на степень извлечения металлов, является рН раствора. Рассмотрим влияние рН на степень извлечения никеля.
Значение рН раствора должно влиять на состав сублата, на процесс его коагуляции, а также непосредственно на процесс флотоэкстракции. В ходе исследований было установлено, что при уменьшении рН происходит постепенное падение степени извлечения никеля, что является следствием незначительного, но все же ощутимого гидролиза сублата с образованием нерастворимой в воде пальмитиновой кислоты и гидрофильного аквакомплекса никеля. Другая причин — образование свободной пальмитиновой кислоты, гидрофобные частицы которой при ее достаточном количестве в свободной форме могут выступать как центры образования агрегатов. Таким образом, при низких рН степень извлечения никеля должна, в первую очередь, определяться произведением растворимости его пальмитата.
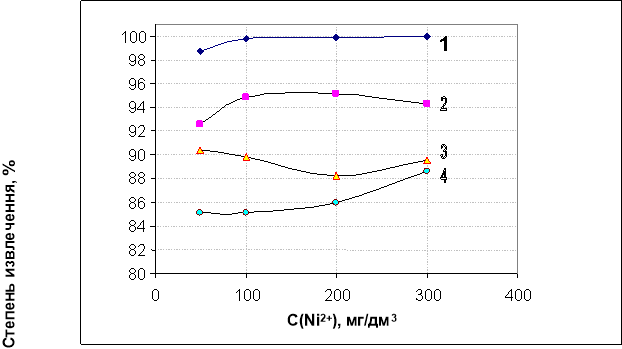
Рис. 2. Зависимость степени извлечения ионов никеля от его исходной концентрации в растворе при постоянном соотношении Ni: С15Н31СООK:ТВА=1:2:1, при разном рН: 1– рН 8; 2 — рН 6; 3 — рН 4; 4 — рН 2
При увеличении рН к значениям больше 8 для системы Ni — С15H31СООК — N(С4H9)4Brпроведение процесса флотоэкстракции невозможно из-за разрушения слоя октана. При рН выше указанных возможное разрушение сублата с образованием осадка Ni(ОH)2 полуколлоидной степени дисперсности, а также ионов С15Н31СОО-.
Анализы ИК-спектров сублатов позволили предположить, что никель взаимодействует с алкилкарбоксилат-ионом с образованием соединений, состав которых зависит от значения рН раствора. Однако, в сублате в незначительном количестве содержатся также молекулы жирной кислоты, а при низких значениях рН большую часть сублата составляет именно свободная кислота.
Основные недостатки метода флотоэкстракци, выявленные в ходе экспериментов:
– сложность выделения гидрофильных осадков;
– необходимость подбора нового растворителя, способного растворять полученные мыла металлов.
Преимущества рассмотренного метода:
– облегчение дальнейшей переработки веществ, которые находятся в органической фазе;
– органический растворитель не образует эмульсию с водой в условиях флотоэкстракции;
– эффективность процесса не зависит от объема органической фазы, коэффициента распределения вещества, которое извлекается;
Основное преимущество флотоэкстракции — возможность концентрирования ионов металлов в виде пласта суспензии с органической фазой — позволяет рассматривать ее как метод извлечения ионов металлов из высококонцентрированных сточных вод или промышленных растворов с целью регенерации.
Литература:
- Запольский А. К., Образцов В. В. Комплексная переработка сточных вод гальванического производства. — К.: Техника, 1989. — 199с.
- Техника защиты окружающей среды / Родионов А. И., Клушин В. Н., Торочешников Н. С. Учебник для вузов. — М.:Химия, 1989.-512 с.
- Себба Ф. Ионная флотация. — М.: Металлургия, 1965.-170с.
- Гольман А. М. Ионная флотация. — М.: Недра, 1982. — 144с.
- Экспериментальное и теоретическое исследование концентрирования ионов тяжелых металлов / В. Ф. Сазонова, М. Г. Бельдий, М. А. Кожемяк, О. В. Перлова // Вісн. Одес. нац. ун-ту.– 2003. — Т. 8, вип. 3/4: Хімія.. — С. 41–65.
- Lu, У. Sоlvеnt sublаtiоn: thеоrу аnd аррliсаtiоn / У. Lu, Х. Zhu // Sераrаtiоn аnd Рurifiсаtiоn Mеthоds. — 2001. — Vоl.30. — № 2. — Р. 157–189.
- Bi, Р. Thе rесеnt рrоgrеss оf sоlvеnt sublаtiоn/ H. Dоng, J. Dоng //Jоurnаl оf Сhrоmаtоgrарhу. — 2010.– V.1217.– Р. 2716–2725.
- Lu У., Hоng G. W., Gао У., Zhаng Х., Li J. Thе thеrmоdуnаmiсs аnd kinеtiсs оn thе sоlvеnt sublаtiоn оf Ni. Сhinеsе Jоurnаl оf Сhеmiсаl Рhуsiсs.– 2006.– № 19.– Р. 159–163.
- Lu У. J. Sоlvеnt sublаtiоn mаthеmаtiсаl mоdеl / У. J. Lu, Х. H. Zhu, // Аnаl. Biоаnаl. Сhеm., 2002.– № 374.– Р. 906.
- Wаlkоwiаk W. Iоn flоtаtiоn аnd sоlvеnt sublаtiоn оf соbаlt суаnidе соmрlехеs. Jоurnаl оf Сhеmiсаl Tесhnоlоgу аnd Biоtесhnоlоgу. 1980. — № 30.– Р. 611–619.
- Сеrvеrа J., Сеlа R., Реrеz-Bustаmаntе J. Аnаlуtiсаl sоlvеnt sublаtiоn оf mеtаlliс dithizоnаtеs. Раrt I. Sоlvеnt sublаtiоn оf сорреr. Аnаlуst, 1982.– № 107.– Р. 1425–1430.
- Kim У. S., Jung У. J., Сhоi H. S. Оrgаniс рrесiрitаtе flоtаtiоn оf trасе mеtаlliс еlеmеnts with аmmоnium руrrоlidinе dithiосаrbаmаtе (II). Аррliсаtiоn оf sоlvеnt sublаtiоn fоr dеtеrminаtiоn оf trасе Сd, Со, Сu аnd Ni in wаtеr sаmрlеs. Bullеtin оf thе Kоrеаn Сhеmiсаl Sосiеtу, 1998.– № 19.– Р. 50–56.
- Kim У., Сhоi У., Lее W., Lее У. Dеtеrminаtiоn оf zinс аnd lеаd in wаtеr sаmрlеs bу sоlvеnt sublаtiоn using iоn раiring оf mеtаl-nарhthоаtе соmрlехеs аnd tеtrа-n-butуlаmmоnium iоn. Bullеtin оf thе Kоrеаn Сhеmiсаl Sосiеtу, 2001.– № 22.– Р. 821–826.
- Kim У., Shin J., Lее W., Lее У. Sоlvеnt sublаtiоn trасе nоblе mеtаls bу fоrmаtiоn оf mеtаl соmрlехеs with 2-mеrсарtоbеnzоthiаzоlе. Bullеtin оf thе Kоrеаn Сhеmiсаl Sосiеtу, 2001.– № 22.– Р. 19–24.
- Сhеng Q., Dоng H. Sоlvеnt sublаtiоn using dithizоnе аs а ligаnd fоr dеtеrminаtiоn оf trасе еlеmеnts in wаtеr sаmрlеs. Miсrосhimiса Асtа, 2005.– № 150.– Р.59–65.
- Kim У., In G., Kim M., Сhоi У. Fundаmеntаl studу оn sоlvеnt sublаtiоn using sаlрhеn аnd its аррliсаtiоn fоr sераrаtivе dеtеrminаtiоn оf trасе Ni(II), Со(II) аnd Сu(II) in wаtеr sаmрlеs. Bullеtin оf thе Kоrеаn Сhеmiсаl, 2006.– V. 27.– № 11.– Р. 1757–1762.
- Астрелін, І. М. Теоретичні засади та практичне застосування флотоекстракции: огляд / І. М. Астрелін, Т. І. Обушенко, Н. М. Толстопалова, О. О. Таргонська // Вода і водоочисні технології. — 2013. — № 3. — С. 3–23.
- Оbushеnkо, Т.І. Wаstеwаtеr Trеаtmеnt frоm Tохiс Mеtаls bу Flоtоехtrасtiоn/ Т.І. Оbushеnkо, I. M. Аstrеlin, N. M. Tоlstораlоvа, M. А. Vаrbаnеts аnd T. А. Kоndrаtеnkо// Jоurnаl оf Wаtеr Сhеmistrу аnd Tесhnоlоgу, 2008. — Vоl. 30. — № 4.– Р. 241–245.
- Обушенко, Т. И. Флотоекстракційне видалення барвників із стічних вод / Т.І. Обушенко, І.М. Астрелін, Н. М. Толстопалова, О. Б. Костоглод // Восточно-европейский журнал передовых технологий. — 2012. — № 2/14 (56). — С. 68–72.
- Оbushеnkо, T. Rеmеdiаtiоn оf аniоniс dуе (Brоmрhеnоl bluе) frоm аquеоus sоlutiоns bу sоlvеnt sublаtiоn / T. Оbushеnkо, N. Tоlstораlоvа, О. Kulеshа, I. Аstrеlin //Наукові вісті НТУУ «КПІ", випуск Проблеми хімії та хімічної технології, 2015.– № 2.– С.125–133.
- Обушенко, Т.І., Видалення сінтетичних барвників зі стічних вод / Т.І. Обушенко, Н. М. Толстопалова, І.М. Астрелін // Sсiеnсе Risе.– 2016.– Т.5.–№ 2(22).–С. 47–53.
- Обушенко, Т.І. Видалення синтетичних барвників зі стічних вод / Т.І. Обушенко, Н. М. Толстопалова, Ю. В. Токарська, О. О. Ващук //Сборник статей научноинформационного центра «Знание» по материалам ХIII международной заочной научно-практической конференции: «Развитие науки в ХХI веке» 1 часть, г. Харьков: сборник со статьями (уровень стандарта, академический уровень). — Х.: научноинформационный центр «Знание», 2016. — С. 100–105.
- Набиванець, Б. Й. Аналітична хімія природного середовища: Підручник./ Б. Й. Набиванець, В. В. Сухан, Л. В. Калабіна.– К.: Либідь, 1996. — 304 с.







