Актуальность. Наиболее частым осложнением острого панкреатита, развивающимся у 20–60 % пациентов, перенесших деструктивный панкреатит, являются псевдокисты поджелудочной железы (ПЖ) [4, 8, 10]. При деструктивных формах острого панкреатита и травме ПЖ кисты формируются в 50–92 % наблюдений [6]. Хронический панкреатит осложняется формированием кистозных образований в 20–40 % случаев [1, 2].
Частота осложнений и летальность при псевдокистах ПЖ сохраняется на высоком уровне. Инфицирование содержимого кист в среднем составляет 20 %, при этом послеоперационная летальность варьирует от 28 до 67 %. Частота аррозивного кровотечения в полость кисты, брюшную полость или желудочно-кишечный тракт составляет 1,6–20 %. Перфорация кист в свободную брюшную полость, сальниковую сумку или полый орган достигает 20 % от числа всех осложнений. Наиболее опасной формой этого осложнения является прорыв кисты в брюшную полость с развитием перитонита, что наблюдают у 5–15 % больных. Сдавление различных отделов желудочно-кишечного тракта кистами ПЖ возникает в 3–4 % случаев [3, 6, 7].
Выделяют три основных варианта хирургического лечения кист ПЖ: резекция с удалением части поджелудочной железы или цистэктомия в изолированном варианте, наружное или внутреннее дренирование [9]. Все эти опреации достаточно травматичны, сопряжаны с риском возникновения интра- и послеоперационных осложнений, продолжительным периодом стационарного и поликлинического периодов лечения. Формированием длительно функционирующего наружного панкреатического свища [5, 6, 9].
В настоящее время все большую актуальность приобретают методы малонвазивных вмешательств при кистах ПЖ: чрезкожные пункции с установкой катетера в полость кисты под контролем УЗИ или КТ, а также выполнение внутреннего эндоскопического (транслюминального) дренирования. [2, 10, 11].
При псевдокистах, локализующихся в области головки поджелудочной железы и диаметре до 5 см, имеющих связь с протоковой системой органа возможна транспапиллярная эндоскопическая установка дренажа в полость кисты. По данным различных авторов пункционно-дренирующие вмешательства под контролем лучевых методов диагностики и эндоcкопии приводят к окончательному выздоровлению от 11,8 до 69,6 %. [2, 5, 6, 8, 9,10]
В России эндоскопическая цистогастростомия впервые была выполнена 2 февраля 1986 г. [11]. В настоящее время транслюминальное дренирование рекомендовано в качестве терапии первой линии для неосложненных кист, доступных для эндоскопических манипуляций. Применение этой технологии для лечения осложненных кист ПЖ, в том числе инфицированных является весьма актуальным и перспективным.
Материалы и методы. Метод транслюминального дренирования кист ПЖ был применен у 13 пациентов, находившихся на стационарном лечении в клинике Краевой клинической больнице г. Касноярска в период с ноября 2013 по февраль 2015 г. У всех больных был установлен диагноз: «Псевдокиста поджелудочной железы». Пациентов мужского пола было 9, женского — 4, средний возраст составил 49 ± 14,9 лет. У 8 пациентов причиной кистоных образований был хронический постнекротический панкреатит (Давность пакреонекроза — от 4 до 10 месяцев), у 5 пациентов — острые кисты (Давность панкреонекроза от 1 до 2 недель). Диагноз устанавливался на основании данных анамнеза, общеклинических и инструментальных методах исследования: УЗИ, МСКТ брюшной полости, при необходимости выполняли диагностические пункции жидкостных образований с исследованием их содержимого. Жалобами при поступлении были — болевой синдром, чувство «тяжести» в эпигастрии, периодические подъемы температуры тела до субфибрильных цифр, слабость.
В зависимости от размера псевдокисты (По данным УЗИ и МСКТ) пациенты распределились следующи образом: гигантские (более 15 см) — 2, большие (от 10 до 15 см) — 7, средние (от 5 до 10 см) — 4. У 2 пациентов с гигантскими псевдокистами имело мест сдавление окружающих органов и тканей (желудок, ДПК, гепатоудоденальная связка), при этом явлений механической желтухи и признаков стеноза выходного отдела желудка не отмечалось. По характеру содежимого кисты: у 8 пациентов кисты были инфицированными (в полости гной, у нескольких пациентов с элементами секвестрации ПЖ), у 5 пациентов -неинфицированные. У 12 пацентов связи полости псевдокисты с вирсунговым протоком выявлено не было, у 1 пациента (после резекции ПЖ) вирсунгов проток сообщался с полостью псевдокисты.
Выбор метода стентирования постнекротических кист определялся непосредственно при эндоскопическом исследовании и зависел от расположения кистозного образования, стоения стенок, взаимоотношения с соседними органами и характера содержимого кисты.
Показанием к выбору пластиковых стентов было гомогенное содержимое кисты. Для выбора металлических самораспраляющихся стентов показаниями служили: отсутствие четкой стенки образования, наличие секвестров, инфицирование образования, киста более 6 см в диаметре, толщина ткани между стенкой ЖКТ и образованием не более 1 см, наличие бессодудистой зоны.
Для транслюминального дренирования исползовали стандартное оборудование марки для проведения эндоскопической ретроградной холангиопанркетографии (ЭРХПГ), эндоскопической папиллосфинктеротомии (ЭПСТ), билиарного эндоротезирования: гастроскоп и дуоденоскоп фирмы «Olympus», C-дуга «Dixion Cyberbloc», пластиковые стенты «Olympus» и металлическе саморасправлющиеся стенты «HANAROSTENT».
Первым этапом в условиях общей внутривенной анестезии проводили осмотр стенок желудка и ДПК, выявляли выбухание стенки желудка к которой предположительно предлежит кистозное образование, окончательная верификация кисты выполнялась с помощью эндоскопической ультрасонографии (Эндо-УЗИ) (рис. 1). Эндо-УЗИ позволяет точно лоцировать псевдокисту, определить расстояние между стенками псевдокисты и верхних отделов ЖКТ, характер содерижимого кисты, выявить бессосудистую области для безопасной установки дренажного устройства (Рис.2)
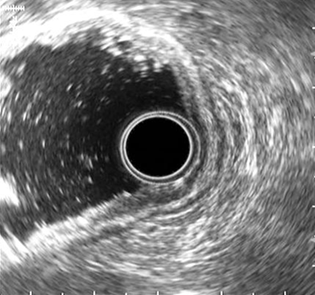
Рис. 1. Эндоскопическая ультрасонография (ЭУС): Определяем расстояние между стенкой желудка и стенкой псевдокисты, эхо-характер содежимого
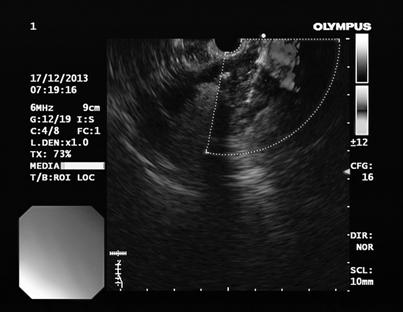
Рис. 2. Эндо-ультрасонография с доплерографией для выявления бессосудистой области стенки желудка
Далее через бессосудистую зону стенки желудка в полость кисты вводится струна-проводник. С помощью С-дуги производится рентген-контроль введения проводника в полость кисты (Рис. 3). Выполняется контрастирование полости кисты для установления разгермитизации протоков поджелудочной железы. У всех 13 пациентов сообщения полости образования с панкреатическим протоком ывявлено не было. По струне проводнику в полость кисты устанавливается пластиковый или металлический стент. Инструменты извлекаются, и проводится визуальный осмотр стента (Рис. 4).
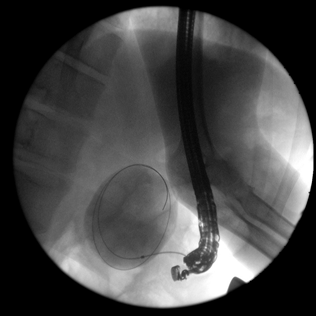
Рис. 3. Рентген-контроль введения струны-проводника в полость кисты
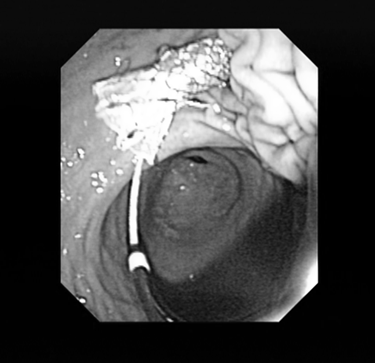
Рис. 4. Визуальный осмотр установленного стента
Пациентам с гигантскими псевдокистами в дополнение к транслюминальному дренированию было выполено наружное дренирование псевдокист под УЗИ-контролем, 1 паценту с послеоперационной псевдокистой после резекции хвоста ПЖ — выполнено ЭРХПГ, ЭПСТ, стентирование вирсунгового протока, 7 пациентам только трансгастральное дренирование.
Всем пациентам было выполнено трансгастральное дренирование с использованием пластиковых и металлических саморасправляющихся стентов.
После проведенного транслюминального дренирования псевдокист ПЖ для оценки динамики полости кисты мы использовали УЗИ и МСКТ.
Результаты. Пациент Ч., 25 лет, поступил с клиникой гигансткой псевдокисты ПЖ. Давность панкреонекроза 6 месяцев. По данным УЗИ брюшной полости при поступлении: в проекции хвоста поджелудочной железы объемное жидкостное образование 9,5*8,6см, кпереди от него аналогичное образование 7,3*4,9см, в области эпигастрия, по передней брюшной стенке -- жидкостное образование неоднородной структуры 4,9*2,2см (вероятно это одно многокамерное обр-е, общим размером 12,6*7,8см). По данным МСКТ: в области хвоста поджелудочной железы по передней поверхности, крупное неправильной формы жидкостное образования с наличием перетяжек, четко отграниченная капсула, общие размеры 12,8х8,7х21,2 см., расположенного между задней стенкой желудка, селезенкой и левой почкой, распространяется вдоль переднего листка фасции Герота до левой подвздошной области. (Рис. 5, 6)
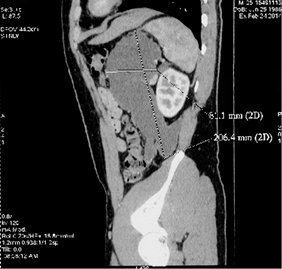
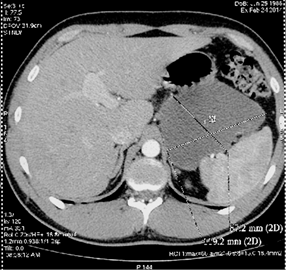
Рис. 5, 6. МСКТ брюшной полости с конратированием пациента Ч.
Учитывая клинику и данные обслдедований, пациенту Ч. проведено трансгастральное дренирование псевдокисты под ЭУС-наведением. (Рис. 7, 8)
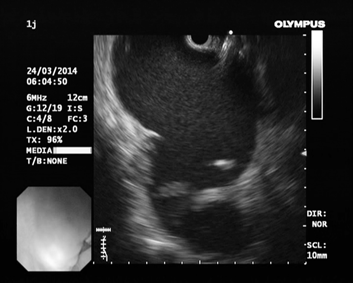
Рис. 7 Эндосонография (ЭУС)
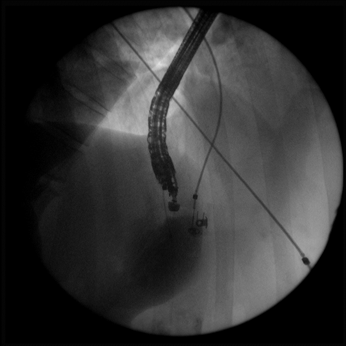
Рис. 8 Рентген-контроль установки проводника
В послеоперационном периоде у пациента Ч. возникла лихорадка до 39 гр С, обусловлена резорбцией содержимого псевдокисты. Пациенту проводилась консервативная системная антибактериальная, противовоспалительная терапия. Температура тела нормализовалась через 3 дня. Пациент был выписан в удовлетворительном состоянии. На контрольном УЗИ брюшной полости через месяц после вмешательства: остаточная полость до 1,23*1,0 см.
У одного пациента по время манипуляци произошел прорыв содержимого псевдокисты в сальниковую сумку, в связи с чем пациент был экстренно оперирован. У одного пациента на контрольном осмотре произошла дислокация стента в полость кисты, повторное стентирование также привело к дислокации стента, в связи с чем пациент был оперирован открыто. У 6 пациентов с инфицированными кистам в раннем послеоперационном периоде наблюдался субфибриллитет, жалобы на боль в эпигастрии, лабораторно умеренный лейкоцитоз, пациентам проводилась системная антибактериальная, противовоспалительная терапия, на фоне которой температура тела и лабораторные показатели нормализовались, болевой синдром полностью купирован. У 5 пациентов с неинфицированными кистами в раннем послеоперационном периоде были жалобы на боли в эпигастрии в течение 2 дней после операции, подъемов температуры тела не наблюдалось, лейкоцитоза за весь период наблюдения не было, пациентам с профилактической целью проводилась системная антибактериальная терапия. Все 11 пациентов были выписаны в удовлетворительном состоянии.
По данным контрольных исследований (УЗИ, МСКТ) остаточная полость кисты значительно уменьшилась: при гигантских кистах с 19 ± 2.8 см до 5.4 ± 5.9 см, при больших кистах с 11.4 ± 1.2 см до 5.9 ± 1.6 см (р < 0,05), при средних кистах с 7.55 см ± 1.3 см до 1.45 ± 2.05 см.
Средний срок госпитализации при неинфицированных кистах составил 17.75 ± 4.79 к/дней, при нагноившихся кистах — 20 ± 10.6 к/дней.
Выводы:
На основании результатов представленнего первого клинического опыта, можно сделать следующие выводы.
1. Выполнение трансгастрального дренирования псевдокист ПЖ под ЭУС-наведенем является малоинвазивным щадящим методом лечения, позволяющим избежать или снизить риск развития таких грозных послеоперационных осложнений, как кровотечение, перфорация, перитонит.
2. Эндоскопичсекая методика лечения позволяет достичь хороших клинических результатов, сопоставимых с традиционными методами лечения: у всех 11 пациентов полость кисты значительно уменьшилась.
3. Применение трансгстрального дренирования позволило, в среднем, на 15–23 суток сократить продолжительность пребывания больных в стационаре в сравнении с традиционными открытыми хирургическими вмешательствами.
Таким образом, трансгастральное дренирование под ЭУС-наведением является эффективным, малоинвазивным и достаточно безопасным способом лечения псевдокист ПЖ, метод заслуживает более широкого внедрения в клиническую практику.
Литература:
1. Lerch M. M., Stier A., Wahnschaffe U., Mayerle J. Pancreatic Pseudocysts. Observation, Endoscopic Drainage, or Resection? // Dtsch. Arztebl. Int. 2009. Vol. 106(38). Р. 614–621.
2. Libera E. D., Siqueira E. S., Morais M., et al. Pancreatic pseudocysts transpapillary and transmural drainage // HPB Surg. 2000. Vol. 11, № 5. P. 333–338.
3. Багненко С. Ф., Курыгин А. А., Рухляда Н. В., Смирнов А. Д. Хронический панкреатит. СПб., 2000. 416 с.
4. Бебуришвили А. Г., Бурчуладзе Н. Ш., Михайлов Д. В. Панкреонекроз и острые псевдокисты парапанкреатической клетчатки // Мат. XVII международного Конгресса хирургов-гепатологовстран СНГ: «Актуальные проблемы хирургической гепатологии». Уфа, 2010.
5. Быкова Ю. Ф., Соловьев М. М., Фатюшина О. А., Руденко Т. О. Оценка методов оперативного лечения псевдокист поджелудочной железы // Сибирский медицинский журнал. 2014. № 1. С. 53–57.
6. Гостищев В. К., Афанасьев А. Н., Устименко А. В. Диагностика и лечение осложненных постнекротических кист поджелудочной железы // Хирургия. 2006. № 6. С. 47–57.
7. Данилов М. В., Фёдоров В. Д. Хирургия поджелудочной железы. Руководство для врачей. М.: Медицина, 1995. 512 с.
8. Кадощук Т. А., Каниковский О. Е., Петрушенко В. В., Стукан С. С. Оценка эффективности способов дренирования осложненных кист поджелудочной железы // Мат. XVII международного Конгресса хирургов-гепатологов стран СНГ: «Актуальные проблемы хирургической гепатологии». Уфа, 2010.
9. Клиническая хирургия: национальное руководство: в 3 т. / под ред.В. С. Савельева, А. И. Кириенко. — М.: Геотар-Медия, 2009. — Т II. — С.495–512
10. Кубачев К. Г., Хромов В. В., Качабеков М. С. Трансдуоденальные эндоскопические вмешательства при кистах поджелудочной железы // Мат. XVII международного Конгресса хирурговгепатологов стран СНГ: «Актуальные проблемы хирургической гепатологии». Уфа, 2010.
11. Парфенов И. П., А. А. Карпачев, С. П. Францев, М. В. Судаков, О. М. Ждановский, А. Л. Ярош, А. В. Солошенко, О. С. Сергеев. Эндоскопические вмешательства при псевдокистах поджелудочной железы // Анналы хирургической гепатологии. 2009. том 15. № 1. С. 27–33.







