Введение
Научно-исследовательская консервация растений направлена на сохранение биологической структуры и химического состава образцов для последующего анализа, с целью замедлить деградацию растительных тканей.
Данная тема заинтересовала меня после посещения музея лекарственных растений ВГМУ им. Бурденко в июне 2025 года при прохождении летней естественно-научной школы МБОУ лицей № 7. Я заметил, что растения в глицерине изменяют цвет и быстро гниют, а также имеют большую массу глицерина и высокую стоимость приготовления, тогда я решил разработать собственную методику.
Актуальность проекта. Проект решает проблему технической сложности консервации растительных тканей, из-за высокой стоимости дорогостоящих компонентов раствора, а также проблему потери окраски из-за попадания бактерий в жидкость. Сейчас наблюдается активное стремление понижения стоимости и повышения срока хранения мёртвых органических материалов для последующего использования в качестве демонстрационного материала и способов его исследования.
Созданный в ходе данной работы метод консервации растений можно использовать в образовательных целях, а также для создания растительного генного банка.
Цель проекта: заключается в том, чтобы упростить технический процесс консервации растительных тканей, а также разработать собственную методику в условиях школьной лаборатории.
Задачи:
- Изучить принципы и процесс консервации растительных тканей;
- Подобрать компоненты раствора для консервации;
- Подобрать доли содержания компонентов раствора и провести молекулярное моделирование;
- Составить технологию новой методики консервации;
- Провести практическое тестирование новой методики на различных органах и тканях растительного образца;
- Сделать выводы на основании проведенного исследования.
Гипотеза: не имея дорогостоящего оборудования и реактивов, можно успешно провести консервацию растительных тканей в пределах школьной лаборатории.
Объект исследования : растительные ткани бегонии тигровой — ( Begonia Bowerae «Tiger» ), драцены Сандера — ( Dracaena Sanderiana Lucky Bamboo ) и пеларгонии пачкающей — ( Pelargonium inquinans ) (Приложение 3, фото 1).
Методы исследования : изучение, обзор литературных источников, эксперимент (физико-химический метод консервации), наблюдение, сравнение, анализ, обобщение.
Практическая значимость заключается в том, чтобы разработать новую методику консервации растительных тканей, которая позволяет упростить и сделать доступным технический процесс консервации растительных тканей.
- Теоретическая часть
Люди начали консервировать растения ещё в древнем мире, в основном это использовалось для продления срока хранения пищи [2]. В средневековье некоторые учёные стали консервировать растения для изучения.
В викторианской Великобритании консервацию начали использовать, как дизайнерскую идею [1]. Изученные принципы и методы консервации помогут в составлении новой методики исследования.
- Принципы и процессы консервации растительных тканей
Консервация растительных тканей — это процесс, направленный на длительное сохранение жизнеспособности клеток и тканей растений.
Согласно принципам консервации растительных тканей, следует производить забор взрослых, не застарелых, здоровых растительных тканей.
В случае если подразумевается забор образцов именно определённого состояния или возраста, тогда качество консервации может снизиться.
Согласно общей методике консервации растительных тканей в специальных жидкостях выделяют следующие этапы:
- Забор образцов взрослых, не застарелых, здоровых растительных тканей;
- Образцы поместить в стерильные условия, хранить не более 48 часов;
- Дезинфицировать растение, инструменты и емкость для консервации;
- Изготовить раствор для консервации;
- Поместить растение в раствор;
- Извлечь растение из раствора;
- Изготовить новый раствор;
- Поместить растение в новый раствор;
- Хранить раствор в заданных методикой условиях [3].
Физико-химический процесс консервации растительных тканей
Для каждой методики существует собственный физико-химический процесс консервации растительных тканей.
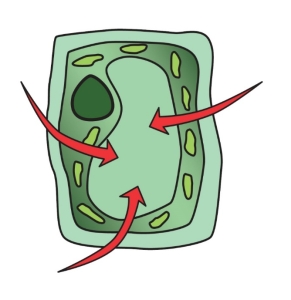
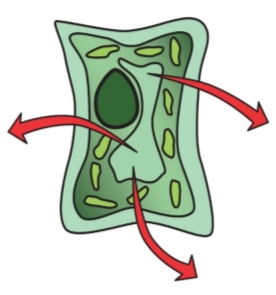
От 70 % до 95 % массы растения приходиться на воду, причём растения имеют массовую концентрацию солей менее 1 %. В результате погружения растительных тканей в среду с большими концентрациями веществ происходит понижение осмотического давления в клетках, из-за которого возникает гипертония клеток (Приложение 1) [4].
Гипертония клеток помогает частично сохранить ДНК, из-за малого повреждения ядрышка, следовательно, на основе методик, вызывающих гипертонию, можно создавать генетические банки. Также гипертония клеток не даёт развиваться микроорганизмам в растворе и растений.
- Практическая часть
2.1 Подбор компонентов раствора для консервации растительных тканей
Подбор агента контроля pH среды. Растения могут произрастать и гнить в кислотных и нормальных условиях, щёлочь приостанавливает процесс роста и замедляет гниение растительных тканей на долгое время. Также щёлочи блокируют усвоение питательных веществ (особенно натриевые и калиевые), которые присутствуют в воде и самих растениях в первые несколько суток после консервации, при 8,5pH [8].
При избытке щёлочь начинает разрушать ткани, поэтому следует выбирать не сильно агрессивные вещества, следует придерживаться водородного показателя от 8pH до 9pH. С этими требованиями хорошо справятся пищевые агенты контроля pH — гидрокарбонат натрия, карбонат натрия, карбонат калия. Самая доступная и неагрессивная из них — гидрокарбонат натрия (пищевая сода), её выбираем как агент контроля pH среды.
В процессе практического исследования водородный показатель раствора находился в пределах 8,5–9 pH.
Подбор основного компонента раствора, вызывающий осмос. Для данного компонента с древних времён используется хлорид натрия (поваренная соль), самая распространённая соль в мире, одна из часто поступающих в организмы и, благодаря своей распространённости с помощью неё легко вызвать осмотическое давление, что также отмечает её малое влияние на водородный показатель.
Подбор антисептика. Для данного компонента требуются бесцветные, бесспиртовые, не кислотные, не агрессивные для растений вещества, с доказанной эффективностью, это могут быть: четвертичные аммониевые соединения, с доказанной эффективностью (бензалкония хлорид, цетилтриметиламмония бромид, цетримониум хлорид, цетилпиридиния хлорид, хлорид бензетония,бензалкония хлорид); (1 E )-2- [6- [[amino- [€- [amino-(4-chloroanilino)methylidene]amino]methylidene]amino]hexyl]1 [amino(4chloroanilino)methylidene]guanidine;bis((2 R ,3 S ,4 R ,5 R )2,3,4,5,6pentahydroxyhexanoic acid), далее — хлоргексидина биглюконат; октенидина дигидрохлорид [9].
Основной целью антисептика в растворе является уничтожение бактерий, грибков, спор и микроорганизмов, которые провоцируют гниение тканей. Вирусы не входят в эту группу, потому что они не способны размножаться в живых организмах, а при консервации растительные ткани часто погибают, следовательно, обработка от вирусов бесполезна. Самый доступный из вышеприведённых антисептиков — хлоргексидина биглюконат, что отмечает его большую популярность и частое применение.
Важный фактор для всех приведённых компонентов — доступность.
Растворителем по умолчанию определяется оксидан (вода).
Все вещества должны быть растворимы в оксидане (воде).
Подбор долей содержания компонентов в жидкости
Массовая доля —
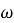
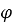
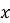
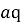
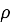
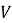
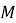
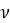
Для удобства изготовления приведены массовые доли 1 % и «круглые» массовые доли (5 %; 10 %; 15 %; 20 % и т. Д.).
Используются данные при стандартных условиях (
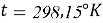
Подбор долей гидрокарбоната натрия.
Требуется водородный показатель от 8pH до 9pH, гидрокарбонат натрия при
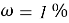
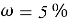
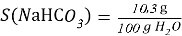
В 100g раствора, при вышеуказанном значении ω, масса гидрокарбоната натрия составит 5g, масса оксидана составит 95g.
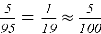
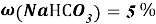
Подбор долей хлорида натрия.
Водный раствор хлорида натрия имеет нейтральную среду, следовательно, не влияет на общий водородный показатель. Для того, чтобы произошёл тургор: ω внешней среды должна быть более 2 %. При этом
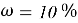
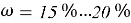
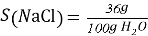
В 100g раствора, при вышеуказанном значении ω, масса хлорида натрия составит 20g, масса оксидана составит 80g
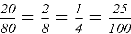
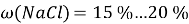
Подбор долей (1
E
)-2- [6- [[amino- [€- [amino-(4-chloroanilino) methylidene] amino]methylidene]amino]hexyl]1 [amino(4chloroanilino)methylidene]guanidine;bis((2
R
,3
S
,4
R
,5
R
)2,3,4,5,6pentahydroxyhexanoic acid), далее — хлоргексидина биглюконат или Ch-Bi.Следует учесть токсичность, эффективность хлоргексидина биглюконата. Хлоргексидина биглюконат уничтожает 99,9 % всех микроорганизмов в среде при
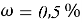
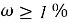
Проверка по растворимости производиться не будет, так как хлоргексидина биглюконат не продаётся рознично в порошковом виде, поэтому можно использовать готовые растворы хлоргексидина биглюконата, добавляя их в основной раствор, предварительно проведя вычисления. Итого, мы получили:
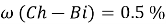
- Расчёты для 1000g раствора.
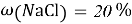
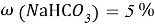
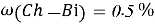
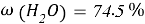
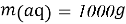
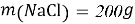
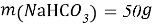
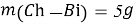
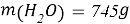
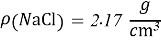
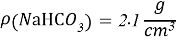
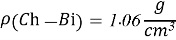
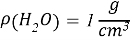
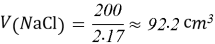
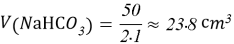
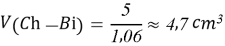
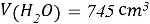
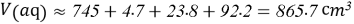
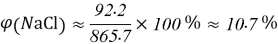
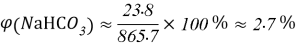
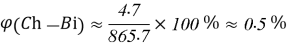
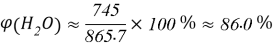
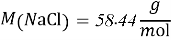
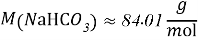
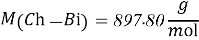
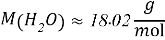
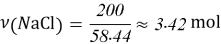
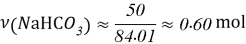
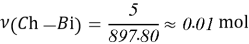
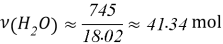
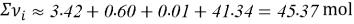
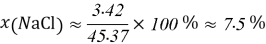
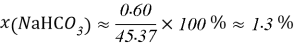
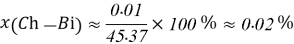
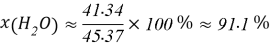
Постоянные концентрации жидкости для консервации:
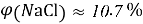
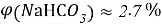
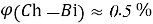
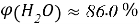
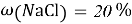
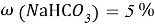
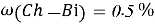
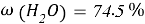
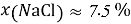
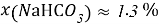
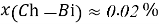
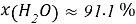
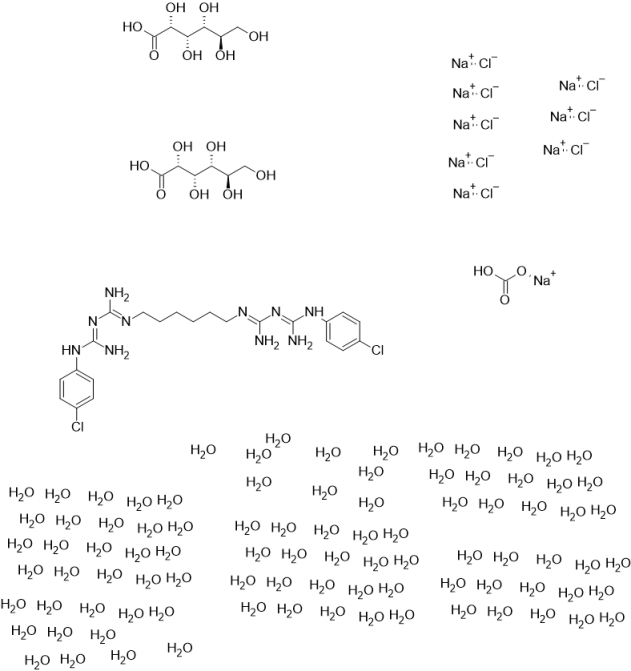
Молекулярное моделирование раствора. Если округлить мольные доли до целых значения, то с помощью ресурса ChemScetch можно составить молекулярную модель раствора. В результате округления получились следующие мольные доли:
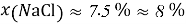
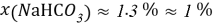
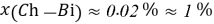
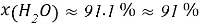
Округлённая мольная доля — количество молекул каждого вещества, что помогает составить примерную молекулярную модель раствора в количестве 101 молекулы (Приложение 2).
- Методика консервации
Методика включает следующие этапы:
- Произвести забор взрослых, не застарелых, здоровых растительных тканей; Образцы поместить в стерильные условия, хранить не более 48 часов (Приложение 3, фото 1).
-
Подготовить: стеклянный или пластиковый, закрывающийся резервуар с крышкой, объёмом в соответствии с размерами консервируемого растения; устройство для кипячения оксидана; растение; оксидан очищенный или дистиллированный, в массе из расчёта:
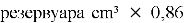
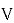
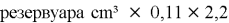
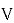
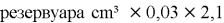
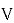
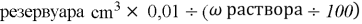
- Дезинфицировать растение, инструменты и емкость для консервации (растение и приспособления для консервации и в разных растворах) в мыльном дезинфицирующем растворе (Приложение 3, фото 3–4); стерилизовать ёмкость для консервации в кипящем оксидане.
- Приготовить раствор для консервации. Используя кипящий оксидан, изготовить раствор в нижеприведённых концентрациях:
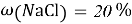
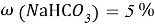
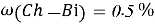
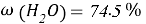
- Если образовались выделения раствора, удалить их.
- Поместить растение в раствор, и закрыть ёмкость (Приложение 3, фото 8).
- Хранить образец в первые 168 часов в тёмном месте, при температуре 293,15°K (20°C; 68°F) — 298,15°K (25°C; 77°F), не допускать попадания ультрафиолетовых лучей более чем на 2 минуты (Приложение 3, фото 9); после 168 часов хранить образец при температуре 288,15°K (15°C; 59°F) — 303,15°K (30°C; 86°F), не допускать попадания прямых ультрафиолетовых лучей (Приложение 3, фото 10).
Заключение
Выдвинутая мною гипотеза в результате исследования полностью подтвердилась. Не имея дорогостоящего оборудования и реактивов, можно успешно провести консервацию растительных тканей в пределах школьной лаборатории.
Изучив литературные источники, были изучены принципы и процессы консервации растительных тканей, была рассмотрена и скорректирована общая методика консервации, а также процесс тургора, благодаря чему стало возможно разработать новую методику.
В результате исследования были успешно подобраны компоненты для новой методики консервации растительных тканей, подобраны доли содержания компонентов раствора и проведено молекулярное моделирование новой методики, что помогло создать хорошую химическую базу, которая упрощает процесс консервации. Была проведена обширная работа по различным химико-биологическим и физико-математическим направлениям.
В ходе исследования было проведено практическое тестирование новой методики, что помогло скорректировать пройденные ранее этапы, а также окончательно подтвердить низкую стоимость и простоту новой методики и сделать следующий вывод:
Все объекты изучения относятся к светолюбивым растениям. Спустя 168 часов у бегонии тигровой — ( Begonia Bowerae «Tiger» ) и пеларгонии пачкающей — ( Pelargonium inquinans) наблюдается изменение цвета листьев с зелёной окраски на желтовато-коричневую, что обусловлено низким содержанием хлорофилла из-за сокращения светового дня и снижения температуры, что ограничивает синтез хлорофилла, а также помутнее раствора из-за изменения структуры антоцианов связанных с изменением pH среды, а у драцены Сандера — ( Dracaena Sanderiana Lucky Bamboo) цвет листьев не изменил окраску, что говорит о высоком содержании хлорофилла. В процессе практического исследования водородный показатель раствора находился в пределах 8,5–9 pH.
Созданный в ходе данной работы метод консервации растений можно использовать в образовательных целях, а также создания растительного генного банка, что возможно даже в обычной школьной лаборатории.
Приложение 1
Взаимодействие растительной клетки с растворами от их осмотического давления
|
|
|
|
Рис. 1. Гипотонический раствор. Вода поступает в клетку, вакуоли увеличиваются и давят на клеточную стенку |
Рис. 2. Гипертонический раствор. При нехватке воды протопласт клетки сжимается и отходит от клеточной стенки из-за потери воды и растение вянет |
Приложение 2
Молекулярная модель раствора для консервации
Приложение 3
|
|
|
|
|
Пеларгония пачкающая |
Бегония тигровая |
Драцена Сандера |
Фото 1. Забор образцов растительных тканей

Фото 2. Приготовление оборудования



Фото 3. Дезинфекция растения, инструментов и ёмкости для консервации


Фото 4. Удаление раствора для дезинфекции



Фото 5. Приготовление раствора для консервации

Фото 6. Определение pH раствора



Фото 7. Распределение растительных образцов в ёмкости для хранения


Фото 8. Консервация растительных образцов

Фото 9. Хранение образцов в первые 168 часов

Фото 10. Образцы после 168 часов
Литература:
- Стабилизация растений для ленивых романтиков. Ну и гиков тоже. — Текст: электронный // Хабр: [сайт]. — URL: https://habr.com/ru/companies/leader-id/articles/527492/ (дата обращения: 01.02.2026).
- История консервной банки: мумии, Наполеон и советские геологи. — Текст: электронный // ГАСТРОНОМЪ: [сайт]. — URL: https://www.gastronom.ru/text/den-konservnoj-banki-1014152 (дата обращения: 01.02.2026).
- Коган, Е. А. Метод консервации и/или окрашивания растительного материала, в том числе срезанных цветов / Е. А. Коган. — Текст: электронный // Google Патенты: [сайт]. — URL: https://patents.google.com/patent/RU2698058C1/ru (дата обращения: 01.02.2026).
- Процесс осмоса в клетках растений и крови человека. — Текст: электронный // nsportal.ru: [сайт]. — URL: https://nsportal.ru/shkola/biologiya/library/2022/04/03/protsess-osmosa-v-kletkah-rasteniy-i-krovi-cheloveka (дата обращения: 24.03.2026).
- Sodium Bicarbonate. — Текст: электронный // PubChem: [сайт]. — URL: https://pubchem.ncbi.nlm.nih.gov/compound/516892 (дата обращения: 24.03.2026).
- Sodium Chloride. — Текст: электронный // PubChem: [сайт]. — URL: https://pubchem.ncbi.nlm.nih.gov/compound/5234 (дата обращения: 24.03.2026).
- Chlorhexidine Gluconate. — Текст: электронный // PubChem: [сайт]. — URL: https://pubchem.ncbi.nlm.nih.gov/compound/9552081 (дата обращения: 24.03.2026).
- Полехов, Р. О. Влияние рН среды на рост растений / Р. О. Полехов. — Текст: электронный // XXIV Международный конкурс научно-исследовательских и творческих работ учащихся Старт в науке: [сайт]. — URL: https://school-science.ru/24/13/61090 (дата обращения: 24.03.2026).
- Антисептики. — Текст: электронный // Рувики: [сайт]. — URL: https://ru.ruwiki.ru/wiki/Антисептики (дата обращения: 24.03.2026).
- Compendium of Chemical Terminology Gold Book / А. Д. Макнот, А. Уилкинсон. — 2-е. —: International Union of Pure and Applied Chemistry, 2014. — 1622 c. — Текст: непосредственный.