Введение
Традиционная стратегия защиты сельскохозяйственных растений, основанная на применении химических пестицидов, сталкивается с растущими проблемами: появление резистентных рас патогена, негативное воздействие на здоровье человека, а также накопление остатков пестицидов в окружающей среде. Переход к высокопродуктивному и экологически чистому агрохозяйству требует создания новых эффективных и безопасных средств защиты растений от патогенов и вредителей. В качестве таких средств защиты выступают биопестициды на основе производного хитина — хитозана. Хитин является основным веществом оболочек грибов, бактерий, насекомых, в том числе, патогенных, поэтому сходный по структуре хитозан вызывает ту же реакцию у растения, что и при встрече с вредным организмом (эффект элиситора). Растение после обработки хитозаном заранее подготавливается к инфекции, в нем начинают работать гены защиты, что приводит к синтезу в тканях растений различных веществ, подавляющих развитие патогена. Один из таких генов — ген PR4 (Pathogenesis Related; относящийся к патогенезу), который кодирует белок — хитиназу, разрушающую хитин патогенных грибов, растительноядных насекомых и нематод [1]. Однако, хитозан имеет ряд недостатков: плохо растворяется в воде, структурно неоднороден, что требует контроля качества. Недавно был получен шарообразный хитозан, или Новохизоль, который гомогенен, а значит имеет предсказуемое действие, хорошо растворяется в воде при любом рН [2]. Кроме того, для него характерны свойства сорбента, способного поглощать другие биологически активные вещества и служить их переносчиком. Благодаря этому может достигаться синергический эффект за счет элиситорного действия Новохизоля и того или иного действия (фунгицидного, антимикробного или антивирусного) добавочного компонента. Отсюда возникла идея: создать комплекс Новохизоля с природным антибиотиком — усниновой кислотой, которая в большом количестве содержится в лишайнике Уснея бородатая [3]. Этот лишайник широко распространен в лесной зоне России, поэтому нет недостатка сырья для выделения этого вещества (Рис. 1).
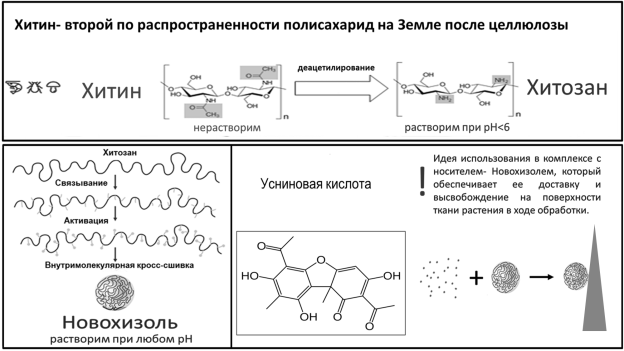
Рис. 1. Схема получения хитозана, Новохизоля и комплекса Новохизоль/усниновая кислота
Стеблевая ржавчина — одно из наиболее разрушительных заболеваний пшеницы, известное с древности. Ее возбудитель, гриб Puccinia graminis f. sp. tritici поражает листья и стебли растения, что приводит к значительному снижению урожая (до 60 %). Стеблевая ржавчина встречается повсеместно, но наиболее вредоносна в регионах с умеренным и тёплым климатом. Основной метод контроля — выращивание устойчивых сортов, однако из-за высокой генетической изменчивости патогена их устойчивость часто быстро преодолевается. Поэтому комплексная защита, сочетающая отбор генетически устойчивых сортов с применением фунгицидов, остаётся важнейшим инструментом контроля данного заболевания.
Цель исследования — изучить действие биопрепарата Новохизоль/ усниновая кислота на восприимчивость растений пшеницы мягкой ( Triticum aestivum L.) к стеблевой ржавчине и активность гена защиты PR4 в течении инфекционного процесса. Для достижения этой цели были поставлены следующие задачи: 1) провести фитопатологическую оценку влияния биопрепарата на восприимчивость растений к стеблевой ржавчине; 2) оценить с помощью ПЦР с обратной транскрипцией (ОТ-ПЦР) уровень транскрипции гена PR4 .
Материалы и методы
В качестве растительного материала была использована мягкая пшеница сорта Новосибирская 29. В качестве патогена — сборная популяция возбудителя стеблевой ржавчины, собранная на территории Западной Сибири, из коллекции Института Цитологии и Генетики СО РАН (ИЦиГ, г. Новосибирск).
Раствор чистого Новохизоля (0.125 %) и 0,125 % раствор Новохизоля с 0,075 % усниновой кислотой (УК) были предоставлены сотрудниками Института Органической Химии СО РАН (ИОХ, г. Новосибирск).
Схема эксперимента, который проводился на базе ИЦиГ, представлена на рис. 2. Растения выращивали в пластиковых горшках с почвой. Были посеяны следующие группы растений, по 50 растений в каждой группе: 1) контроль (растения без обработки и зараженные); 2) обработанные Новохизолем и зараженные; 3) обработанные комплексом Новохизоль/УК и зараженные. Растворы биопрепаратов наносили на растения с помощью бытового опрыскивателя. Спустя 4 суток проводили заражение растений спорами стеблевой ржавчины, смешанными с минеральным маслом (выполнял сотрудник ИЦиГ). Зараженные растения инкубировали в вегетационных камерах, в условиях, необходимых для прорастания спор и дальнейшего процесса инфекции. Через 3, 24, 48, 72 и 144 часа отдельные листья срезали с каждого растения и замораживали в жидком азоте. Собранный материал хранили при -80 °С перед выделением РНК.
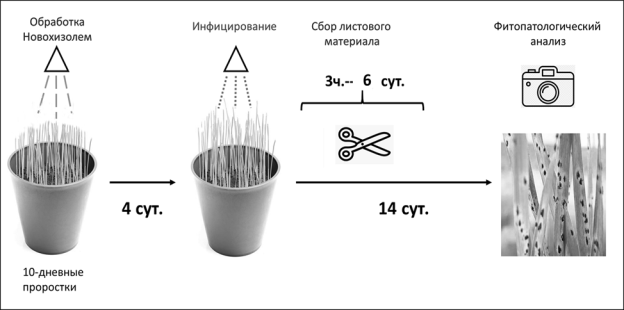
Рис. 2. Схема лабораторного эксперимента
Общую РНК выделяли с помощью специального набора для выделения (Биолабмикс, Новосибирск) в соответствии с инструкцией. Концентрацию РНК измеряли на спектрофотометре. Для оценки качества пробы РНК наносили на 1 % агарозный гель с красителем (бромид этидия) и проводили электрофорез.
кДНК (комплементарная ДНК) была получена с помощью специального набора для обратной транскрипции матричной РНК (Биолабмикс). Далее с образцами кДНК проводили ОТ-ПЦР. Для этого использовали синтезированные в компании «Биосет» праймеры к гену PR4 и гену GAPDH , использованному в качестве референсного. Структура праймеров была взята из статьи [1]. ПЦР-смесь для ОТ-ПЦР (25 мкл) содержала 50 нг кДНК, стандартные количества каждого праймера и дНТФ, 1× реакционный буфер и 1 единицу Taq ДНК-полимеразы. ПЦР начиналась с инкубации при 94 ºC в течение 3 мин., за которой следовали 35 циклов: 94 ºC (30 сек.), 60 ºC (30 сек.), 72 ºC (30 сек.). Продукты ПЦР разделяли методом электрофореза в 2 % агарозном геле. Гель фотографировали в UV свете для визуализации продуктов.
Степень восприимчивости растений к стеблевой ржавчине оценивали через 14 дней после заражения с использованием шкалы инфекционных типов (ИТ) Стэкмана [4]. ИТ «1» и «2» интерпретировались как устойчивые, а «3» и «4» — как восприимчивые. Для оценки количественной составляющей восприимчивости подсчитывали суммарное количество пустул для каждого ИТ (устойчивые/восприимчивые) на листьях 50 растений каждой группы.
Результаты и обсуждение
Для фитопатологической оценки применялась визуальная оценка степени восприимчивости растений к стеблевой ржавчине по количеству и размеру пустул (очагов спороношения). В группах заражённых листьев, обработанных препаратами Новохизоль и Новохозоль/усниновая кислота наблюдается явный видимый эффект воздействия препаратов на развитие стеблевой ржавчины. Этот эффект выражается в увеличении соотношения числа пустул устойчивого типа (ИТ 1 и 2) к числу пустул восприимчивого типа (ИТ 3 и 4) от 0,3 — у зараженных растений без обработки до 4–4,6 — у зараженных растений, предварительно обработанных Новохизолем и комплексом Новохизоль/усниновая кислота (Табл. 1). При этом общее число пустул при обработке Новохизолем незначительно возрастало, а при обработке комплексом достоверно снижалось в 1.5 раза относительно зараженных растений без обработки. Таким образом, при обработке комплексом Новохизоль/усниновая кислота наблюдалось ослабление развития болезни как количественное, так и качественное (по уменьшению восприимчивого типа пустул). Данный комплекс был более эффективен для подавления болезни по сравнению с чистым Новохизолем.
Таблица 1
Количество пустул, соответствующих различным типам устойчивости и восприимчивости на листьях экспериментальных групп растений
|
Варианты опыта |
Число пустул, соответствующих типам устойчивости и восприимчивости (всего на 50 листьях) |
Общее число пустул |
Отношение уст./воспр | |
|
ИТ1 и ИТ2 (устойчивые) |
ИТ3 и ИТ4 (восприимчивые) | |||
|
Заражение без обработки |
135 |
427 |
562 |
0,3 |
|
НВХЗ; заражение |
487 |
122 |
609 |
4 |
|
НВХЗ/усниновая; заражение |
300 |
65 |
365 |
4,6 |
Для оценки влияния биопрепаратов на работу генов защиты, нами был выбран ген PR4 , кодирующий белок с хитиназной активностью. Ранее было показано, что транскрипция данного гена у необработанных Новохизолем растений мягкой пшеницы, зараженных возбудителем стеблевой ржавчиной, возрастает только спустя 6 суток (144 ч.) после заражения, тогда как у обработанных этим препаратом растений активация гена происходит гораздо раньше — через 48–72 часа после заражения [1]. Наш результат подтвердил эти данные, показав усиление транскрипции PR4 спустя 72 часа после заражения стеблевой ржавчиной у растений, обработанных чистым Новохизолем (рис. 3). У растений же, обработанных комплексом Новохизоль/усниновая кислота, это усиление происходит еще раньше — через 24 часа. Таким образом, препараты Новохизоля оказывают стимулирующее влияние на транскрипцию гена защиты PR4 на ранних стадиях инфекционного процесса. Данный ген может служить маркером эффективности обработки растений изученными биопрепаратами. Стимулирующий эффект на устойчивость растений и уровень транскрипции PR4 наиболее выражен в случае комплекса Новохизоль/усниновая кислота.
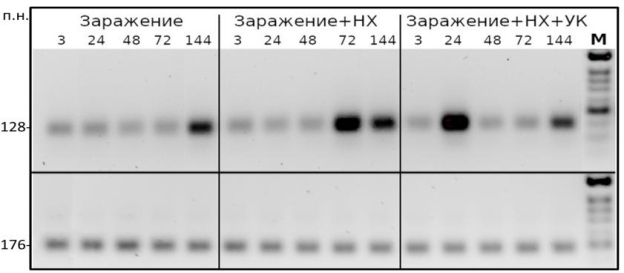
Рис. 3. Результат ОТ-ПЦР генов PR4 (вверху) и GAPDH (внизу) для образцов листовой ткани мягкой пшеницы, собранных в различные временные точки (3–144 ч.) после заражения стеблевой ржавчиной
Выводы
- Комплексный биопрепарат Новохизоль/усниновая кислота вызывает повышение качественной и количественной устойчивости растений мягкой пшеницы к стеблевой ржавчине.
- Выявленное повышение устойчивости растений к грибному патогену под действием препарата Новохизоль/усниновая кислота связано с увеличением транскрипции генов защиты на ранней стадии заражения, что было подтверждено на примере гена PR4 (увеличение транскрипции спустя 24 часа после заражения).
- Комплексный препарат Новохизоль/усниновая кислота является более эффективным по влиянию на устойчивость растений к стеблевой ржавчине и по стимулирующему воздействию на активность гена PR4 по сравнению с чистым Новохизолем.
Благодарности. Автор выражает благодарность своим научным руководителям — сотрудникам ИЦиГ СО РАН Разуваевой Алёне Викторовне и кандидату биологических наук Сколотневой Екатерине Сергеевне.
Литература:
- Щербань А. Б., Разуваева А. В., Сколотнева Е. С., Фоменко В. В. Влияние биопестицида Новохизоль на экспрессию генов защиты при заражении пшеницы стеблевой ржавчиной Puccinia graminis f. sp. tritici . Вавиловский журнал генетики и селекции. 2025; 29(8):1203–1212. doi 10.18699/vjgb-25–127
- Щербань А. Б. Хитозан и его производные как перспективные средства защиты растений. Вавиловcкий журнал генетики и селекции. 2023; 27:1010–1021. doi 614 10.18699/VJGB−23−116
- Соколов Д. Н., Лузина О. А., Салахутдинов Н. Ф. Усниновая кислота: получение, структура, свойства и химические превращения. Успехи химии. 2012; 81: 747–768. doi 10.1070/RC2012v081n08ABEH004245
- Roelfs A. P., Singh R. P., Saari E. E. Rust diseases of wheat: concepts and methods of disease management. — M.: Mexico, CIMMYT, 1992.

