Коррозия – это самопроизвольный процесс разрушения материалов и изделий из них под химическим воздействием окружающей среды.
Коррозия металлов – разрушение металлов вследствие физико-химического воздействия внешней среды, при котором металл переходит в окисленное (ионное) состояние и теряет присущие ему свойства.
В тех случаях, когда окисление металла необходимо для осуществления какого-либо технологического процесса, термин “коррозия” употреблять не следует. Например, нельзя говорить о коррозии растворимого анода в гальванической ванне, поскольку анод должен окислятся, посылая свои ионы в раствор, чтобы протекал нужный процесс. Нельзя также говорить о коррозии алюминия при осуществлении алюмотермического процесса. Но физико-химическая сущность изменений, происходящих с металлом во всех подобных случаях, одинакова: металл окисляется [1].
Проблема защиты металлов от коррозии возникла почти в самом начале их использования. Люди пытались защитить металлы от атмосферного воздействия с помощью жира, масел, а позднее и покрытием другими металлами и, прежде всего, легкоплавким оловом. В трудах древнегреческого историка Геродота (V век до нашей эры) уже имеется упоминание о применении олова для защиты железа от коррозии.
Задачей химиков было и остается выяснение сущности явлений коррозии, разработка мер, препятствующих или замедляющих её протекание. Коррозия металлов осуществляется в соответствии с законами природы и поэтому ее нельзя полностью устранить, а можно лишь замедлить [2].
По типу разрушений различают коррозию наружную (атмосферная и почвенная) и внутреннюю. Основным видом коррозии наружной поверхности промысловых трубопроводов является язвенная коррозия, а внутренней – равномерная или общая, происходящая в результате окислительно-восстановительныхгетерогенных процессов, происходящие на поверхности раздела фаз.
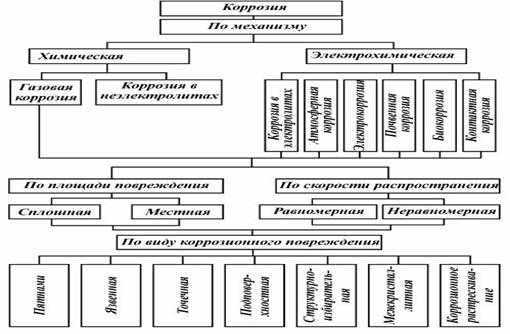
Коррозию классифицируют: по механизму, по площади повреждения, скорости распространения и виду коррозионного повреждения (3-схема).
3-схема.
В зависимости от характера коррозии и условий ее протекания применяются различные методы защиты. Выбор того или иного способа определяется его эффективностью в данном конкретном случае, а также экономической целесообразностью [3].
В производстве широко используется химическое нанесение металлических покрытий на изделия. Процесс химического металлирования является каталитическим или автокаталитическим, а катализатором является поверхность изделия. Используемый раствор содержит соединение наносимого металла и восстановитель. Поскольку катализатором является поверхность изделия, выделение металла и происходит именно на ней, а не в объеме раствора. В настоящее время разработаны методы химического покрытия металлических изделий никелем, кобальтом, железом, палладием, платиной, медью, золотом, серебром, родием, рутением и некоторыми сплавами на основе этих металлов. В качестве восстановителей используют гипофосфит и боргидрид натрия, формальдегид, гидразин. Естественно, что химическим никелированием можно наносить защитное покрытие не на любой металл.
Металлические покрытия делят на две группы:
1. коррозионностойкие;
2. протекторные.
Например, для покрытия сплавов на основе железа в первую группу входят никель, серебро, медь, свинец, хром. Они более электроположительны по отношению к железу, то есть в электрохимическом ряду напряжений металлов стоят правее железа. Во вторую группу входят цинк, кадмий, алюминий. Они более электроотрицательны по отношению к железу.
В повседневной жизни человек чаще всего встречается с покрытиями железа цинком и оловом. Листовое железо, покрытое цинком, называют оцинкованным железом, а покрытое оловом – белой жестью. Первое в больших количествах идет на кровли домов, а второе – на изготовление консервных банок. Впервые способ хранения пищевых продуктов в жестяных банках предложил повар Н.Ф. Аппер в 1810 году. И то, и другое железо получают, главным образом, протягиванием листа железа через расплав соответствующего металла.
Металлические покрытия защищают железо от коррозии при сохранении сплошности. При нарушении же покрывающего слоя коррозия изделия протекает даже более интенсивно, чем без покрытия. Это объясняется работой гальванического элемента железо–металл. Трещины и царапины заполняются влагой, в результате чего образуются растворы, ионные процессы в которых облегчают протекание электрохимического процесса (коррозии) [4].
Применение ингибиторов – один из самых эффективных способов борьбы с коррозией металлов в различных агрессивных средах. Ингибиторы – это вещества, способные в малых количествах замедлять протекание химических процессов или останавливать их. Название ингибитор происходит от латинского inhibere, что означает сдерживать, останавливать. Ещё по данным 1980 года, число известных науке ингибиторов составило более пяти тысяч. Ингибиторы дают народному хозяйству немалую экономию.
Ингибирующее воздействие на металлы, прежде всего на сталь, оказывает целый ряд неорганических и органических веществ, которые часто добавляются в среду, вызывающую коррозию. Ингибиторы имеют свойство создавать на поверхности металла очень тонкую пленку, защищающую металл от коррозии.
Ингибиторы в соответствии с Х. Фишером можно сгруппировать следующим образом:
1) Экранирующие, то есть покрывающие поверхность металла тонкой пленкой. Пленка образуется в результате поверхностной адсорбции. При воздействии физических ингибиторов химических реакций не происходит;
2) Окислители (пассиваторы) типа хроматов, вызывающие образование на поверхности металла плотно прилегающего защитного слоя окисей, которые замедляют протекание анодного процесса. Эти слои не очень стойки и при определенных условиях могут подвергаться восстановлению. Эффективность пассиваторов зависит от толщины образующегося защитного слоя и его проводимости;
3) Катодные – повышающие перенапряжение катодного процесса. Они замедляют коррозию в растворах неокисляющих кислот. К таким ингибиторам относятся соли или окислы мышьяка и висмута.
Эффективность действия ингибиторов зависит в основном от условий среды, поэтому универсальных ингибиторов нет. Для их выбора требуется проведение исследований и испытаний.
Наиболее часто применяются следующие ингибиторы: нитрит натрия, добавляемый, например, к холодильным соляным растворам, фосфаты и силикаты натрия, бихромат натрия, различные органические амины, сульфоокись бензила, крахмал, танин и т. п. Поскольку ингибиторы со временем расходуются, они должны добавляться в агрессивную среду периодически. Количество ингибитора, добавляемого в агрессивные среды, невелико. Например, нитрита натрия добавляют в воду в количестве 0,01-0,05%.
Ингибиторы подбираются в зависимости от кислого или щелочного характера среды. Например, часто применяемый в качестве ингибитора нитрит натрия может использоваться в основном в щелочной среде и перестает быть эффективным даже в слабокислых средах [5, 6].
Металлы составляют одну из основ цивилизации на планете Земля. Их широкое внедрение в промышленное строительство и транспорт произошло на рубеже XVIII-XIX. В это время появился первый чугунный мост, спущено на воду первое судно, корпус которого был изготовлен из стали, созданы первые железные дороги. Начало практического использования человеком железа относят к IX веку до нашей эры. Именно в этот период человечество перешло из бронзового века в век железный.
В XXI веке высокие темпы развития промышленности, интенсификация производственных процессов, повышение основных технологических параметров (температура, давление, концентрация реагирующих средств и др.) предъявляют высокие требования к надежной эксплуатации технологического оборудования и строительных конструкций. Особое место в комплексе мероприятий по обеспечению бесперебойной эксплуатации оборудования отводится надежной защите его от коррозии и применению в связи с этим высококачественных химически стойких материалов.
Необходимость осуществления мероприятий по защите от коррозии диктуется тем обстоятельством, что потери от коррозии приносят чрезвычайно большой ущерб. По имеющимся данным, около 10% ежегодной добычи металла расходуется на покрытие безвозвратных потерь вследствие коррозии и последующего распыления. Основной ущерб от коррозии металла связан не только с потерей больших количеств металла, но и с порчей или выходом из строя самих металлических конструкций, т.к. вследствие коррозии они теряют необходимую прочность, пластичность, герметичность, тепло- и электропроводность, отражательную способность и другие необходимые качества. К потерям, которые терпит народное хозяйство от коррозии, должны быть отнесены также громадные затраты на всякого рода защитные антикоррозионные мероприятия, ущерб от ухудшения качества выпускаемой продукции, выход из строя оборудования, аварий в производстве и так далее.
Защита от коррозии является одной из важнейших проблем, имеющей большое значение для народного хозяйства.
Коррозия является физико-химическим процессом, защита же от коррозии металлов – проблема химии в чистом виде [7].
Сегодня говорить о том, что коррозия металла как процесс его разрушения практически побежден, преждевременно. И проблем здесь хватает. Но ученые прилагают все усилия, чтобы коррозия металла как можно меньше доставляла неудобств в процессе эксплуатации металлических конструкций.
Все больше появляется методов борьбы с этим процессом, все больше появляется материалов, которые гарантируют эффективную защиту. На исследования тратятся большие финансовые средства, поэтому коррозия металла должна отступить в будущем, а точнее сказать, сдать свои позиции. Коррозия металлов и меры борьбы с ней – это одна из главных задач, которую ставят перед собой строители, начиная поднимать новый объект.
Литература:
1. Андреев И.Н. Коррозия металлов и их защита. – Казань: Татарское книжное издательство, 2001. – С. 68-70.
2. Лукьянов П.М. Краткая история химической промышленности. – М.: Издательство АН СССР, 1999. – С. 55-56
3. Чухарева Н.В., Абрамова Р.Н., Болсуновская Л.М. – Коррозионные повреждения при транспорте скважинной продукции. – Томск, 2009. - С. 5-6.
4. Войтович В.А., Мокеева Л.Н. Биологическая коррозия. – М.: Знание, 2000. – С. 70.
5. Шехтер Ю.Н., Ребров И.Ю., Легезин Н.Е. и др. Некоторые проблемы ингибирования коррозии // Защита металлов, 1998, Т.34. - № 6. - С. 638-641.
6. Козлов А.А., Прохорова Н.П., Бограчев А.М. Новейшие тенденции в разработке и применении ингибиторов коррозии для водоохлаждающих систем // Химическая промышленность. – 1986. - № 1. - С. 40-41.
7. Улиг Г.Г., Реви Р.У. Коррозия и борьба с ней. – Л.: Химия, 2000. – С. 30-35.







