Серебро и сплавы на его основе обладают бактерицидными, фунгицидными и противовирусными свойствами [1,2]. Однако по сравнению с множеством других химических элементов серебро отличается относительно низкой токсичностью к клеткам млекопитающих [3]. Поэтому серебро и его формы, в частности, нульвалентный металл в виде наночастиц вызывают интерес в большом круге научных исследователей. Была показана эффективность наночастиц серебра против болезнетворных микроорганизмов: Escherichia coli [4], Staphylococcus aureus [5], Klebsiella mobilis, Mycobacterium tuberculosis [6], Candida albicans [7], вирус гепатита B [8], вирус африканской чумы свиней [9]
Растущая резистентность к антибиотическим препаратам у болезнетворных микроорганизмов является серьезной проблемой медицины, для решения которой требует разработка новых лекарственных форм. Наночастицы серебра являются перспективной альтернативой антибиотикам. Уникальность наночастиц серебра состоит в том, что они являются эффективными средствам против даже полиантибиотикорезистентных штаммов бактерий, это утверждено в ряду научных публикаций [10–14].
Наночастицы серебра могут быть получены различными методами. Суть химического метода получения наночастиц серебра состоит в восстановлении ионов серебра реагентами. Среди популярных реагентов — восстановителей следует назвать боргидрид натрия, цитратом натрия, гидразин, альдегиды… Наночастицы серебра также получают с помощью физических методов: метод лазерной абляции, радиолитические методы или вакуумное испарение металла и электроконденсационный метод Сведберга. Каждый метод имеет свои преимущества и недостатки. Однако химический метод чаще всего применяется в лабораторной и производственной практике, особенно если получаемые наночастицы будут использованы для биологических целей.
Несмотря на большое количество научных публикаций наночастицы серебра остаются интересным исследуемым объектом для многих ученых. Целью большинства работ по данной теме является оптимизация параметров процесса получения, улучшение бактерицидной способности получаемого продукта…
Цель настоящей работы: исследование физико-химических и антибактериальной активности наночастиц серебра, полученных химическим восстановлением боргидридом натрия (NaBH 4 ), стабилизированных хлоридом алкилбензилдиметиламмония.
Материалы и методы исследования
В настоящей работе кроме вышеупомянутых химических реагентов также использован нитрит серебра в качестве прекурсора-предшественника. Все химические реактивы производства Sigma Aldrich. Наночастицы серебра получены по методике, аналогично описанной в [9] с заменой хитозана на хлорид алкилбензилдиметиламмония в качестве стабилизатора. Массовая концентрация наночастиц серебра в полученном растворе составляет 500 мг/л; массовое отношение серебра: стабилизатор составляет 1:10. Хлорид алкилбензилдиметиламмония представляет собой четвертичным аммонийным соединением, также известен под названием «Бензалькония хлорид» с обозначением BKC.
Спектр оптического поглощения растворов наночастиц серебра зарегистрирован на спектрофотометре UH-5300 (Hitachi). Дзета-потенциал наночастиц определен на приборе Nano particle analyzer SZ-100 (Horiba). Антибактериальная активность наночастиц определена по отношению Escherichia coli по методике, описанной в [4]. В качестве эталонов взяты растворы наночастиц серебра, стабилизированных крахмалом и поливинилпирролидоном. Все образцы наночастиц серебра получены по одной и той же методике [9].
Результаты и их обсуждение
Спектр оптического поглощения раствора наночастиц серебра, стабилизированных хлоридом алкилбензилдиметиламмония (образец AgNPs-BKC) представлен на рисунке 1. На полученном для наночастиц серебра спектре зафиксирован максимум, соответствующий длине волн 420 нм. Причиной появления такого характерного спектра является взаимодействие электромагнитного поля светового излучения с электронами проводимости наночастиц серебра.
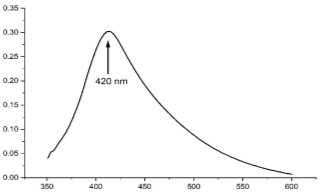
Рис. 1. Спектр оптического поглощения наночастиц серебра AgNP-BKC
Также были сняты спектры оптического поглощения данного образца, подвергнутого хранению на длительные сроки в лабораторных условиях. Значение максимумов спектров представлены в таблице 1. По полученным результатам выявлено смещение пиков в сторону длинных волн, что свидетельствует об укрупнении наночастиц в более крупные агрегаты. Также в таблицу 1 занесены значения дзета-потенциала образца. Довольно высокие значения дзета-потенциала свидетельствуют о высокой агрегативной устойчивости коллоидного раствора по времени.
Таблица 1
Изменение значений физико-химических параметров образца AgNP - BKC по времени
|
Параметр |
Д зета-потенциала (мВ ) |
Максимум спектров (нм) |
||||
|
Время хранения (сутки) |
30 |
180 |
360 |
30 |
180 |
360 |
|
Значение |
+35,4 |
+30,3 |
+28,6 |
420 |
427 |
433 |
Результаты по определению антибактериальной активности представлены на рисунках 2–4. AgNPs-Starch обозначает образец наночастиц серебра, стабилизированных крахмалом; AgNPs-PVP — образец наночастиц серебра, стабилизированных поливинилпирролидоном. По оси абсцисс — время эксперимента, измеримое в часах, по оси ординат — оптическая плотность, измеримая при 600 нм (ОП 600 ).
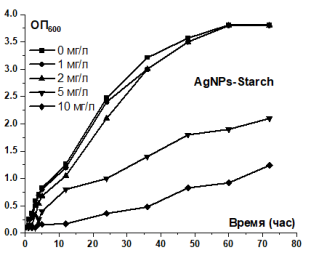
Рис. 2. Антибактериальная активность наночастиц серебра, стабилизированных крахмалом по отношению Escherichia coli
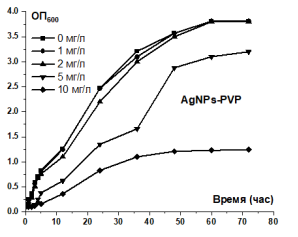
Рис. 3. Антибактериальная активность наночастиц серебра, стабилизированных поливинилпирролидоном по отношению Escherichia coli
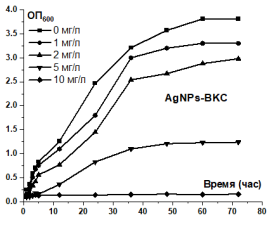
Рис. 4. Антибактериальная активность наночастиц серебра, стабилизированных хлоридом алкилбензилдиметиламмония по отношению Escherichia coli
Анализ кривых роста E.coli под влиянием наночастиц серебра позволяет выявить важную роль стабилизаторов в ингибировании роста бактерий. В образцах наночастиц серебра, стабилизированных крахмалом и поливинилпирролидоном (образцов AgNPs-Starch и AgNPs-PVP), концентрации 1 и 2 мг/л практически не влияли на рост E.coli в экспериментальных условиях, указанные кривые практически совпадали с контрольной кривой (т. е. концентрация наночастиц серебра составляет 0 мг/л). При концентрациях 5 и 10 мг/л способность ингибировать бактерии этих двух образцов была лучше, но все же не достигала минимальной ингибирующей концентрации (МИК) для E.coli в экспериментальных условиях.
Образец наночастиц серебра, стабилизированных хлоридом алкилбензилдиметиламмония, проявляет значительное превосходство по сравнению с двумя образцами, стабилизированными крахмалом и поливинилпирролидоном. Даже при концентрациях 1 и 2 мг/л образец AgNPs-BKC уже оказывал определенное влияние на ингибирование роста E.coli. При концентрации 5 мг/л AgNPs-BKC ингибировал рост E.coli не хуже, чем образцы AgNPs-крахмал и AgNPs-PVP при концентрации 10 мг/л. Особенно при концентрации 10 мг/л после 72 часов эксперимента вообще не наблюдалось роста бактерий, что доказывает, что уровень концентрации 10 мг/л образца AgNPs-BKC можно рассматривать как МИК для данного штамма E.coli .
Заключение
Методом химического восстановления получены наночастицы серебра, стабилизированных хлоридом алкилбензилдиметиламмония. Изучены их физико-химические свойства и антибактериальная активность. По результатам анализа спектров оптического поглощения и дзета-потенциалов выявлена устойчивость полученных наночастиц серебра по времени. Также выявлено влияние стабилизирующего агента на антибактериальную активность наночастиц серебра. Использование хлорида алкилбензилдиметиламмония в качестве стабилизатора улучшает антибактериальную активность наночастиц по сравнению с традиционными веществами — крахмалом и поливинилпирролидоном.
Работа выполнена при финансовой поддержке Департамента Наук и Технологий Правительства города Ханой, номер гранта 01С-09/01–2021–3.
Литература:
- Krutyakov Y. A. et al. Synthesis and properties of silver nanoparticles: advances and prospects // Russ. Chem. Rev. 2008. Vol. 77, № 3. P. 233–257.
- Lok C.-N. et al. Proteomic analysis of the mode of antibacterial action of silver nanoparticles: 4 // J Proteome Res. 2006. Vol. 5, № 4. P. 916–924.
- Zhao G., Stevens S. E. Multiple parameters for the comprehensive evaluation of the susceptibility of Escherichia coli to the silver ion // Biometals. 1998. Vol. 11, № 1. P. 27–32.
- Li W.-R. et al. Antibacterial activity and mechanism of silver nanoparticles on Escherichia coli // Appl Microbiol Biotechnol. 2010. Vol. 85, № 4. P. 1115–1122.
- Li W.-R. et al. Antibacterial effect of silver nanoparticles on Staphylococcus aureus // Biometals. 2011. Vol. 24, № 1. P. 135–141.
- Verkhovskii R. et al. Physical properties and cytotoxicity of silver nanoparticles under different polymeric stabilizers // Heliyon. 2019. Vol. 5, № 3. P. e01305.
- Lara H. H. et al. Effect of silver nanoparticles on Candida albicans biofilms: an ultrastructural study // Journal of Nanobiotechnology. 2015. Vol. 13, № 1. P. 91.
- Lu L. et al. Silver nanoparticles inhibit hepatitis B virus replication: 2 // Antivir Ther. 2008. Vol. 13, № 2. P. 253–262.
- Dung T. T. N. et al. Silver nanoparticles as potential antiviral agents against African swine fever virus: 12 // Mater. Res. Express. IOP Publishing, 2020. Vol. 6, № 12. P. 1250g9.
- Saeb A. T. M. et al. Production of Silver Nanoparticles with Strong and Stable Antimicrobial Activity against Highly Pathogenic and Multidrug Resistant Bacteria // The Scientific World Journal. Hindawi, 2014. Vol. 2014. P. e704708.
- Довнар Р. И. et al. Антибактериальные И Физико-Химические Свойства Наночастиц Серебра И Оксида Цинка // Журнал Гродненского Государственного Медицинского Университета. 2022. Vol. 20, № 1.
- Wahab S. et al. Mechanistic aspects of plant-based silver nanoparticles against multi-drug resistant bacteria // Heliyon. 2021. Vol. 7, № 7. P. e07448.
- Naqvi S. Z. H. et al. Combined efficacy of biologically synthesized silver nanoparticles and different antibiotics against multidrug-resistant bacteria // International Journal of Nanomedicine. Dove Medical Press, 2013. Vol. 8. P. 3187–3195.
- Das B. et al. Green synthesized silver nanoparticles destroy multidrug resistant bacteria via reactive oxygen species mediated membrane damage: 6 // Arabian Journal of Chemistry. 2017. Vol. 10, № 6. P. 862–876.







