У больных с Q-волновым инфарктом миокарда уровень МНУП характеризуется преобладанием средних и средневысоких значений и уровня Аль с преобладанием средневысоких его значений. Установлено, что уровень повышения МНУП и Аль коррелирует с тяжестью ИМ, развитием как ранних, так и поздних осложнений. Низкая ФВ (ФВ<50 %) более характерна для пациентов с передней локализацией ИМ, с наличием предынфарктной стенокардии и сопряжена с развитием острой сердечной недостаточности, аневризмы ЛЖ и ПОЖЭ, не оказывая при этом влияния на частоту развития РПИС.
Ключевые слова: нейрогуморальная регуляция, постинфарктное ремоделирование ЛЖ, острый инфаркт миокарда, прогноз жизни, мозговой натрийуретический пептид, альдостерон.
The research findings of examining 73 patients aged 38 to 65 (average age 55.6 + 4.8 years) who developed ischemic coronar disorder with stable stenocardia disorder of I-II functional class, show that allopurinol and in larger extent “Hepa — Merz”, preseribed additionally for ordinary therapy, put down the level of Urine Acid and brought up the speed of glomerius filtration and exerection with urine acid. Hepa Merz in larger extent promotes increase in membrane erythrocyte, stabilises methabolits of NO2, activates endothelial NO synthetasa, loweres expression of nicotinamidenucleotide phosphate and the level of peroxinitrite (ONOO-), to larger extent than allopurinol. There was identified the distinet correlation between decrease in blood urine acid and positive changes in membrane erythrocytes, the indicatory of NO system condition. On the basis of the above it is recommended to include allopurinol and / or Hepa Merz in the course of therapy in order to correct hyperuricemia.
Keywords: Allopurinol, Hepa — Merz, metabolic symptom, ischemic coronar.
Введение.
Внедрение современных технологий диагностики, лечения и реабилитации при остром инфаркте миокарда (ОИМ) существенно повлияло на течение и исходы заболевания, способствовало увеличению продолжительности жизни и улучшению её качества у лиц, перенесших ИМ. Тем не менее, ИМ сохраняет за собой первенство среди причин летальности от сердечно-сосудистых заболеваний. В связи с этим идентификация предикторов неблагоприятного прогноза в ранние сроки ОИМ на сегодняшний день является одной из актуальных задач современной кардиологии. Многочисленными исследованиями доказана прогностическая роль постинфарктного ремоделирования (ПИР) левого желудочка (ЛЖ) для риск-стратификации больных с перенесенным ИМ [4, 6]. Среди нейрогуморальных факторов (НГФ) в патогенезе ПИР ЛЖ особую роль играют натрийуретические пептиды (НУП), концентрация которых увеличивается уже на ранних стадиях развития дисфункции ЛЖ [3, 7]. Многочисленными исследованиями показано, что среди НУП важную роль в оценке прогноза играет мозговой НУП (МНУП). Весьма перспективным является использование МНУП как маркера долгосрочного прогноза у больных с ОИМ [9]. В течение последних полутора десятилетий также получены убедительные доказательства роли альдостерона (Аль) в процессах структурных изменений сердца и сосудов, что имеет особое значение при ремоделировании сердечно-сосудистой системы у больных с ОИМ и хронической сердечной недостаточностью (ХСН) [1].
Цель исследования. Оценить значимость влияния исходных показателей сократимости миокарда левого желудочка, локализации ОИМ и уровней МНУП и альдостерона на прогностические показатели у больных, перенесших Q-волновой ИМ.
Материалы иметоды. Обследовано 80 мужчин, с первичным Q-волновым ИМ в возрасте от 29 до 60 лет (средний возраст 50,8±0,98 лет). Диагноз подтверждался на основании критериев ВОЗ. Критериями исключения были: повторный ИМ, сопутствующие злокачественные новообразования, системные заболевания легких, заболевания почек. Все включенные в исследование больные принимали стандартную терапию, включающую иАПФ, бета-блокаторы, статины, антиагреганты, антикоагулянты, диуретики и антиаритмические средства при наличии сложных нарушений ритма сердца. Контрольную группу составили 14 здоровых добровольцев мужского пола, сопоставимого возраста. Плазменный уровень NT-proBNP и Аль определялись на 7 сутки заболевания на иммуноферментном анализаторе ELISA с использованием реактивов фирмы «Biomedica» (Австрия).
ЭхоКГ и допплерографическое исследование проводилось на аппарате «Sonoline Versa Pro» по стандартной методике с использованием рекомендаций Американского эхокардиографического общества. Измерялись и рассчитывались следующие показатели: толщина задней стенки ЛЖ (ТЗСЛЖ), конечный диастолический размер (КДР) ЛЖ, конечный систолический размер (КСР) ЛЖ, фракция выброса (ФВ) ЛЖ, конечный диастолический объем (КДО) ЛЖ, конечный систолический объем (КСО) ЛЖ. Масса миокарда ЛЖ (ММЛЖ) вычислялась по формуле R.Devereux и соавторов: ММЛЖ=1,04*((КДР+МЖПД+ЗСЛЖД) — КДР)-13,6гр.
Методом допплерэхокардиографии оценивалась диастолическая функция (ДФ). Для характеристики ДФЛЖ оценивались следующие показатели: максимальная скорость кровотока в фазу быстрого наполнения (пик Е, см/с), максимальная скорость кровотока в систолу предсердия (пик А, см/с) и их отношение (Е/А). Признаком нарушения ДФ считалось уменьшение отношения Е/А менее 1,0. Математическая обработка данных проведена с помощью программного пакета STATISTICA-6,0.
Результаты исследования. Для проведения анализа сравнительной характеристики показателей центральной гемодинамики в зависимости от исходных значений ФВ ЛЖ, больные были разделены на две группы: первую группу составили больные с сохранной сократительной способностью миокарда (≥50 %), а вторую — со сниженной сократительной способностью (<50 %) (табл.1).
Таблица 1
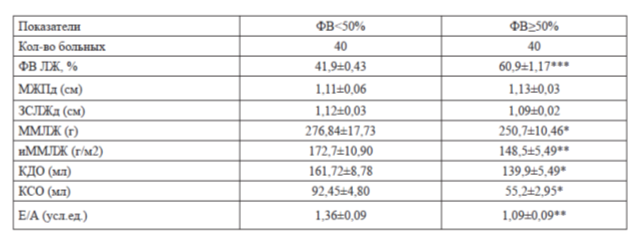
Примечание: *-р<0,05
Как видно из табл.1 у 40 (50 %) больных величина ФВ была менее 50 % и составила в среднем 41,9±0,43 % и у 40 больных ФВ была больше 50 % и составила — 60,9±1,17 %. Следует отметить, что объемные показатели КДО и КСО и иММЛЖ у больных со сниженной сократительной способностью были достоверно меньше на 40 %, 13,4 % и 14 %. соответственно, по сравнению с больными с сохраненной сократительной способностью ЛЖ. Нарушения диастолической функции у больных со сниженной сократимостью также были достоверно более значимыми (на 19,8 %) по сравнению с группой больных с ФВ больше 50 %.
Анализ клинической характеристики больных в зависимости от величины ФВ показал, что 28 пациентов первой группы представлены передней локализацией ОИМ (70 % против 45 %, χ2=4,111, Р<0,05), (табл. 2)
Таблица 2
Клиническая характеристика изучаемых групп
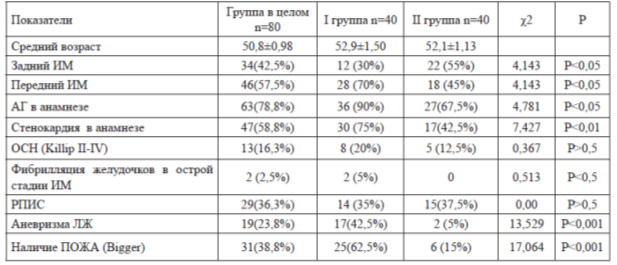
Подавляющее количество больных первой группы в анамнезе имели стенокардию напряжения (75 % против 42,5 %, χ2=7,427, Р<0,01). Кроме того, для острого и подострого периода ОИМ у больных со снижением сократимости миокарда было характерно наиболее частое развитие осложнений: так, в первой группе аневризма имела место в 17 случаях, тогда как во второй группе она осложнила течение ОИМ в 2 случаях (42,5 % против 5 %, χ2=13,529, Р<0,001).
Потенциально опасная желудочковая экстрасистолия (ПОЖЭ) по данным суточного мониторирования ЭКГ, на 10–14 сутки ОИМ имела место у 25 больных I группы и 6 больных II группы (62,5 % против 15 %, χ2=17,064, Р<0,000). По количеству больных с РПИС обе группы достоверно не различались. При анализе полученных результатов нами выявлено, что концентрация МНУП и Аль превышали показатели здоровых лиц, уровень МНУП в 3,4 раза, а концентрация Аль на 15 % (табл. 3).
Таблица 3
Показатели МНУП иАль убольных ОИМ на 7 сутки заболевания

Примечание: Р — достоверность по сравнению с контрольной группой **Р<0,01; ***- Р<0,001
Как видно из таблицы, величина МНУП у больных ИМ на 7 сутки имела большую вариабельность. В связи с этим, для детального анализа нами были составлены гистограммы распределения МНУП с интервалами его низких (≤400 фмоль/мл), средне-низких (≥400≤600фмоль/мл), средних (≥600≤800 фмоль/мл), средневысоких (≥800≤1000 фмоль/мл) и высоких значений (≥1000 фмоль/мл). При распределении пациентов по уровню МНУП большинство их попали в интервалы средних и средневысоких значений.
Учитывая узкий диапазон значений уровня Аль, гистограммы распределения Аль были распределены с интервалами его низких (>200 пг/мл) и высоких (<200 пг/мл) значений.
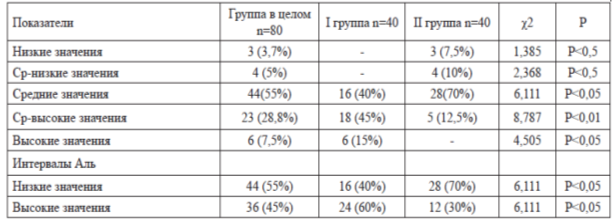
Необходимо отметить, что в группах больных с ФВ<50 % в 60 % случаев отмечались средне-высокие и высокие значения МНУП (45 % и 15 %), средние значения этого показателя регистрировались у 16 (40 %) пациентов. Пациенты с ФВ≥50 % демонстрировали средние уровни МНУП в 70 % случаев, а у 5 (12,5 %) пациентов отмечались средне-высокие значения этого показателя. При этом низкий уровень МНУП был выявлен у 3-х (7,5 %), а средне-низкий у 4-х (10 %) пациентов, причем ни в одном случае в этой группе больных не отмечалось высоких значений МНУП. Сравнительный анализ содержания Аль в плазме крови показал следующее: в 1 группе больных с ФВ<50 % преобладали высокие значения (<200 пг/мл) уровня Аль (60 % и 40 %, соответственно), во 2 группе отмечалось преобладание средне-высоких значений (70 и 30 %). Характерно, что данные изменения носили высокодостоверный характер (табл.4).
При оценке прогноза в исследуемых группах пациентов было выявлено, что в I группе больных за 6 месяцев наблюдения отмечено развитие повторных ИМ в 5 (14,3 %) случаях, в том числе 2 фатальных и 3 нефатальных, а также 1(2,9 %) внезапная смерть. Тогда как во II группе повторный ОИМ (нефатальный) развился у 2 (6,7 %) больных.
Таблица 4
Взаимосвязь между концентрацией НГФ исократительной способностью миокарда
Обсуждение
Как известно ОИМ сопровождается нейрогуморальной активацией, которая является компенсаторным механизмом, направленным на поддержание сердечного выброса. Из большого количества нейрогормонов, участвующих в процессах компенсации сниженной систолической функции ЛЖ, в настоящее время МНУП привлекают внимание в связи с тем, что этот гормон признан как индикатор прогноза у больных ОИМ. Повышение уровня МНУП у пациентов с ОИМ служит предиктором неблагоприятного прогноза в отношении риска смерти и развития повторного ИМ. Влияние МНУП на прогноз определяется его способностью отражать объёмную нагрузку на миокард ЛЖ и нарушения систолической функции сердца, ведущие к развитию СН [2, 8].
По данным различных авторов, Аль также отводится важное место в развитии и прогрессировании сердечной недостаточности. Получены убедительные доказательства роли Аль в процессах структурных изменений сердца и сосудов, что имеет особое значение при ремоделировании сердечно-сосудистой системы у больных с ОИМ и ХСН.
M. Hayashi и соавторами [10] найдено увеличение уровня интрамиокардиального образования Аль при остром ИМ, по результатам его определения в устье аорты и коронарном синусе; определена положительная связь между уровнем Аль при остром ИМ с индексом конечно-диастолического объема ЛЖ, как показателя ремоделирования через месяц после ИМ. Растянутость во времени процесса ремоделирования ЛЖ при ХСН и переход из адаптивного в дезадаптивное состояние связывают, прежде всего, с гиперактивацией симпатоадреналовой системы и как системной, так и тканевой РААС [1], что характерно и для ПИКС. Известно, что усиление интрамиокардиальной продукции Аль коррелирует с уровнем проколлагена III типа — маркером фиброза миокарда. Установлена экспрессия рецепторов к Аль на кардиомиоцитах, клетках эндотелия, фибробластах миокарда, их активация ведет к усилению синтеза коллагена, пролиферации фибробластов, стимулирует миокардиальный фиброз. При ПИКС, по сравнению с таковыми при ИБС без инфаркта, выявлены достоверно более высокие величины уровня Аль. Таким образом, увеличение уровня Аль при ПИКС после ИМ передней локализации по сравнению с таковым при нижней может быть существенным патогенетическим фактором более тяжелого нарушения структуры и функции миокарда, то есть процесса ПИР после ИМ передней локализации [5, 10].
Нами были установлены сходные факторы, влияющие на прогноз больных, перенесших Q-ИМ. При анализе данных по концентрации МНУП и Аль нами была выявлена их большая вариабельность, что побудило нас создать гистограммы распределения уровня изучаемых нейрогормонов. По величине ФВ в покое больные были разделены на 2 группы: 1-я-ФВ<50 %, 2-я-ФВ≥50 %. Было выявлено, что в I группе больных достоверно были выше КДР ЛЖ, объёмные показатели ЛЖ и предсердий. При оценке корреляционных взаимосвязей между уровнем МНУП, с одной стороны, и ФВ, летальным исходом, развитием ХСН выявлено, что между высокими значениями МНУП и ФВ имеется отрицательная сильная корреляция (r=-0,71), средневысокие значения коррелируют с ФВ с образованием средней степени (r=-0,49). При этом летальность имеет сильную положительную корреляцию с высокими и средневысокими значениями МНУП (соответственно, r=0,79; r=0,70). При сравнительном анализе клинико-анамнестических данных двух групп больных выявлено, что группы достоверно различались по локализации ИМ, наличию двух и более симптомов ОСН в острейшем периоде, а также наличию НК на 10–14 сутки заболевания. Анализ значений НГФ показал достоверное преобладание высоких и средневысоких значений МНУП и высоких значений Аль у больных с низкой сократительной способностью миокарда.
Выводы.
- Низкая ФВ (ФВ<50 %) более характерна для пациентов с передней локализацией ИМ, с наличием предынфарктной стенокардии и сопряжена с развитием острой сердечной недостаточности, аневризмы ЛЖ и ПОЖЭ, не оказывая при этом влияния на частоту развития РПИС.
- Высокие концентрации МНУП в плазме крови являются предикторами неблагоприятного прогноза у больных, перенесших Q-волновой ИМ, увеличивая на 5–29 % риск развития ХСН, повторных коронарных событий, в том числе фатальных, и общую летальность больных в течение шестимесячного наблюдения. Уровень альдостерона имеет прямую взаимосвязь средней степени выраженности (от r=0,32 до r=0,39) с риском развития как фатальных, так и нефатальных событий.
- Уровень МНУП в крови у больных, перенесших Q — волновой инфаркт миокарда, имеет преимущественно средне-высокие (≥800≤1000 фмоль/мл) и высокие (≥1000 фмоль/мл) значения в подавляющем большинстве случаев.
Литература:
- А. Э. Багрий, Л. В. Лукашенко, В. Г. Яковенко, Селективный антагонист альдостерона Инспра(эплеренон) в лечении больных, перенесших инфаркт миокарда. // Тер. архив 1(8) 2007.
- Андреев Д. А. Натрийуретические пептиды В-типа при сердечной недостаточности: диагностика, оценка прогноза и эффективности лечения. // Лаб. Мед. 2003;6.
- Беленков Ю. Н., Привалова Е. В., Чекнева И. С. Мозговой натрийуретический пептид — современный биомаркер хронической сердечной недостаточности // Кардиология. — 2008. — № 6. — С. 62–69.
- Курбанов Р. Д., Киякбаев Г. К. Инфаркт миокарда. Прогноз жизни. — 2001. — 200 с.
- Л. Янчайтите, Д, Растяните. Прогноз у больных, перенесших инфаркт миокарда с зубцом Q нижней или передней локализации // Кардиология, 8, 2007. С. 36–39.
- Antman E., Cohen M., Bernink P. J. et al. The TIMI risk score for unstable angina/non-ST elevation MI: a method for prognostication and therapeutic decision making// JAMA. — 2000. — Vol.284. — P. 835–842.
- Bay M., Kirk V., Parner J. et al. NT-proBNP: a new diagnostic screening tool to differentiate between patients with normal and reduced left ventricular systolic function// Heart. — 2003. — Vol.89. — P.150–154.
- Cheng V., Kazanegra R., Garcia A. et al.A rapid bedside test for B-type natriuretic peptide predicts treatment outcomes in patients admitted for decompensated heart failure: a pilot study. // Am Coll Cardiol 2001; 37: 386–391.
- Christopher H., Christian W. Hamm. N-Terminal Pro-B-Type Natriuretic Peptide Levels for Dynamic Risk Stratification of Patients With Acute Coronary Syndromes// Circulation. — 2004. — Vol. 110. — P. 3206–3212.
- Hayashi M., Tsumamoto T., Wada A. et al. Relationship between transcardiac extraction of aldosterone and left ventricular remodeling in patients with first acute myocardial infarction: extracting aldosterone through the heart promotes ventricular remodeling after acute myocardial infarction // J. Amer. Coll. Cardiology. — 2001. — № 38(5). — P. 1375–1382.







