Использование растворов силиката натрия в производстве бетонов
Авторы: Сарсеналиева Айна Есенгалиевна, Айтуганова Сауле Гараповна
Рубрика: 13. Химическая технология и промышленность
Опубликовано в
IV международная научная конференция «Современные тенденции технических наук» (Казань, октябрь 2015)
Дата публикации: 07.10.2015
Статья просмотрена: 1208 раз
Библиографическое описание:
Сарсеналиева, А. Е. Использование растворов силиката натрия в производстве бетонов / А. Е. Сарсеналиева, С. Г. Айтуганова. — Текст : непосредственный // Современные тенденции технических наук : материалы IV Междунар. науч. конф. (г. Казань, октябрь 2015 г.). — Казань : Бук, 2015. — С. 107-110. — URL: https://moluch.ru/conf/tech/archive/163/8861/ (дата обращения: 26.04.2024).
В данной статье рассмотрены физико-химические свойства силиката натрия и использование растворов силиката натрия в производстве бетонов.
Ключевые слова: кремнесодержащие породы, опока, силикат натрия, бетон, производства бетонов, вязкость, плотность.
В производстве строительных материалов используется силикат натрия для производства бетонных конструкций и изделий. Силикат натрия является крупнотоннажным продуктом неорганического синтеза и производится во всех промышленно развитых странах мира, причем с увеличением темпов строительства в Казахстане потребность в нем непрерывно возрастает. Исходя из классификации строительных вяжущих веществ, раствор силиката натрия относят к «воздушным вяжущим», поскольку искусственный камень на его основе неводостоек — разупрочняется при хранении в воде. Однако специальными приемами водостойкость такого камня может быть значительно повышена, прежде всего, за счет правильного выбора отвердителя, использования термического отверждения, введение добавок-модификаторов и т. д. Раствор силиката натрия применяют для производства бетонных конструкций и изделий, для укрепления грунтов при строительстве дорог, аэродромных покрытий, оснований под фундаменты, в частности, в составе инъекционных растворов [1].
Основным способом производства раствора силиката натрия, реализуемым в нашей области является получение растворов силиката натрия гидротермальным методом на основе природного кремнеземсодержащего сырья.
Сырьем для производства растворов силиката натрия гидротермальным методом являются горные породы осадочного происхождения (опоки, трепелы, диатомиты и др.). Одним из основных критериев определения пригодности данного сырья является максимальное содержание в нем аморфного SiO2 и минимальное содержание примесей, которые являются источником загрязнения растворов щелочных силикатов и способствуют появлению в них нерастворимых остатков.
Силикат натрия используется он обычно в виде водных растворов. Общепризнано, что в химии силикатов, а также в химии растворов силикатов результат химического взаимодействия трудно, а подчас и невозможно свести к ряду химических реакций в привычном для химиков формульном выражении. С одной стороны, это обусловлено сложным и большей частью неизвестным полимерным составом раствора, который формально характеризуют силикатным модулем, и неизвестным характером полимерных превращений в ходе взаимодействия. С другой стороны, такая ситуация складывается из-за некристаллического аморфного состояния продуктов реакции. Обычно они имеют нестехиометрический состав и развитую поверхность; большую роль в этом случае играют адсорбционные явления, и отличить адсорбцию от химических реакций можно только условно или в специальном исследовании [2].
Химизм процессов, происходящих при твердении силикатных масс на основе силиката натрия, проявляется, прежде всего, в выделении из щелочного силиката коллоидного кремнезема. Эта коагуляция особенно наглядно обнаруживается у высококремнеземистых силикатных композиций, содержащих большое количество малоустойчивых коллоидных мицелл, легко распадающихся под влиянием различных причин. Высокомодульные концентрированные растворы силикатов щелочных металлов, получаемые гидротермальным способом, являются системами, переходными от растворов к коллоидам. Им уже в значительной степени присущи превращения, характерные для коллоидной химии: гелеобразование, коагуляция, флокуляция. Эти явления очень часто сопутствуют, накладываются на основное химическое взаимодействие, придавая химии растворов силикатов своеобразие.
Основными характеристиками растворов щелочных силикатов являются силикатный модуль, содержание SiO2, М2О (Na2О или К2О), или содержание твердого вещества (SiO2+М2О). Штыренковым предложена эмпирическая формула для определения силикатного модуля натриевых силикатов: п=55,16(р-1)N—2,28, где р -плотность раствора силиката натрия; N — нормальность щелочи в этом растворе, определенная титрованием. На рис. 1 представлены в качестве примера для системы К2О- SiO2-Н2О графики, позволяющие по плотности и содержанию К2О и SiO2 определить модуль раствора, или наоборот, причем графики, предназначенные для работы, делают более крупными и наносят на них частую сетку.
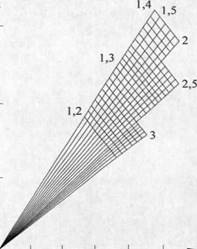
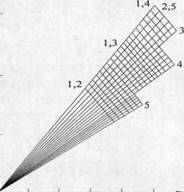
Рис. 1. Плотность растворов силикатов калия (число над линиями) в зависимости от состава раствора (числа справа показывают отношение SiO2/К2О: а — массовое, б — молярное)
Для определения плотности в технических целях используют наборы ареометров. При более точных измерениях прибегают к пикнометрическому методу с обязательным термостатированием.
Вязкость растворов очень сильно изменяется с температурой.
Небольшой подогрев может быть оправдан при перевозке щелочных силикатов по железной дороге в цистернах. Исследователи обычно отмечают, что причина высокой вязкости силикатных растворов по своей природе отлична от растворов высокополимерных органических соединений. Способы определения средней молекулярной массы по величине характеристической вязкости не применимы к растворам щелочных силикатов [3].
Другой особенностью химии растворов силикатов является то обстоятельство, что результат взаимодействия реагентов зависит не только от их химической природы, но и от целого ряда нехимических факторов: порядка смешения реагентов, их начальной концентрации, скорости перемешивания при смешении и т. п. Общая причина этой группы явлений — гелеобразование на границе раздела взаимодействующих или смешиваемых фаз. Это приводит к осложнениям при гомогенизации реакционной системы и к возрастанию роли диффузионных процессов, предшествующих химическому взаимодействию реагентов. Поэтому различные технологические приемы, используемые для обеспечения взаимодействия реагентов, могут играть решающую роль в создании систем с заданными свойствами. Такими технологическими приемами, помимо перемешивания, могут быть предварительное растворение твердых реагентов в том же самом растворителе (например, в воде); их диспергирование; проведение гетерогенной реакции при непрерывном обновлении поверхности (например, в шаровой мельнице); растворение различных исходных реагентов в двух несмешивающихся растворителях с последующим эмульгированием и т. п. Описание результатов реакции и использования тех или иных технологий проведения этих реакций оказывается громоздким, сводится, в конечном итоге, к бесконечному множеству примеров.
Очевидно, что, приливая раствор силиката к избытку кислоты, при быстром перемешивании можно проскочить этот диапазон рН и сразу выйти на устойчивые системы при рН равном 2. Обратный порядок приливания приведет к образованию геля или к неоднородной системе при медленном перемешивании. Из рисунка следует, что использование сильнокислотных катионитов, обусловливающее малую ионную силу раствора, может дать совсем иной результат, чем адекватная нейтрализация щелочи кислотой в диапазоне рН = 7–10. Изменение природы аниона в растворе, т. е. частичная замена гидроксильного иона анионом вводимой кислоты, имеет следствием большую или меньшую потерю устойчивости системы, поскольку гидроксильный ион лучше любого другого аниона хемосор-бируется на поверхности полимерных частиц, сообщая им отрицательный заряд, препятствующий их агломерации. В зависимости от способности аниона кислоты сорбироваться на поверхности кремнезема полная или частичная нейтрализация раствора щелочного силиката той или иной кислотой может дать внешне различные результаты: выпадение объемистого аморфного осадка (коагуляция), образование студенеобразной массы (гелеобразование), помутнение раствора из-за образования микронеоднородностей в системе, сохранение прозрачного раствора с меньшим или большим изменением вязкости [4].
Учитывая широкое применение растворов силиката натрия для производства бетонных конструкций и изделий, для укрепления грунтов при строительстве дорог, аэродромных покрытий, оснований под фундаменты и т. д. большое значение имеют исследования свойств силиката, полученные из местных месторождений.
Литература:
1. Технологическая оценка качества на разных стадиях ГРР исходных и активированных цеолитсодержащих кремнистых пород для использования в нетрадиционных направлениях Методические указания НСОМТИ № 98 / Т. П. Конюхова, У. Г. Дистанов, О. А. Михайлова, Д. А. Кикило, Т. Н. Чуприна. — М.: ВИМС, 2000. — 111 с.
2. Везенцев, А. И. Энергосберегающий синтез нанодисперсного аморфного силиката натрия для производства жидкого стекла / А. И. Везенцев, И.Д. Тарасова, Е. Л. Проскурина, А. П. Полыпин // Стекло и керамика. — 2008. —№ 8.-С. 3–7.
3. Айлер, Р. Химия кремнезема / Р.Айлер; пер. с англ. — М: Мир, 2001. Ч. 1,2.-416с.
4. Барзаковский, В. П. Труды Д. И. Менделеева в области химии силикатов и стеклообразного состояния / В. П. Барзаковский, Р. Б. Добротин. — М.: Изд-во АН. 2002. — 125 с.
Ключевые слова
плотность, бетон, вязкость, плотность., кремнесодержащие породы, опока, силикат натрия, производства бетоновПохожие статьи
Материалы и реагенты для приготовления промывочных...
Использование растворов силиката натрия в производстве бетонов.
При пропускании избытка углекислого газа через раствор гидроксида натрия, а также при длительном стоянии раствора NaOH на...
Использование новой технологии электрохимической активации...
Использование растворов силиката натрия в производстве бетонов. Исходя из классификации строительных вяжущих веществ, раствор силиката натрия относят к «воздушным вяжущим», поскольку искусственный камень на его основе неводостоек...
Коррозия углеродистой стали в 30-процентном растворе...
Использование растворов силиката натрия в производстве бетонов. Выбор конструкционных материалов для оборудования установки... С ростом температуры коррозионная агрессивность растворов ДЭГ увеличивается и достигается.
Химия варки древних стекол на зольной шихте | Статья в журнале...
В результате реакции образуется силикат натрия — простейшее силикатное стекло.
Использование растворов силиката натрия в производстве бетонов. Усовершенствование процесса получения цианистого натрия.
Инновационные материалы — добавки и стабилизаторы для...
− LBS — жидкий силикатно-полимерный стабилизатор грунта. При внесении водного раствора LBS в грунт обеспечивается необратимое изменение физико-механических свойств грунта за счет
− снижается стоимость строительства дорог различных категорий на 10–15 %
Структурообразование геополимеров | Статья в журнале...
Давидовичем для объяснения структурообразования вяжущего на основе метакаолина, твердение которого активировалось растворами щелочных силикатов [1]. Позднее этим ученым и другими исследователями было установлено...
Мыльная основа из вторичных ресурсов масложировых предприятий
Использование растворов силиката натрия в производстве бетонов.
Очевидно, что, приливая раствор силиката к избытку кислоты, при быстром перемешивании... Печатно-технические свойства печатных красок, основанных на...
Синтез трихлорэтилена в реакторе периодического типа...
Использование растворов силиката натрия в производстве... Сырьем для производства растворов силиката натрия гидротермальным методом являются горные породы осадочного происхождения (опоки, трепелы, диатомиты и др.).
Свойства известкового композиционного вяжущего с применением...
Строительство.
Использование растворов силиката натрия в производстве бетонов. Способы определения средней молекулярной массы по величине характеристической вязкости не применимы к растворам щелочных силикатов [3].
Похожие статьи
Материалы и реагенты для приготовления промывочных...
Использование растворов силиката натрия в производстве бетонов.
При пропускании избытка углекислого газа через раствор гидроксида натрия, а также при длительном стоянии раствора NaOH на...
Использование новой технологии электрохимической активации...
Использование растворов силиката натрия в производстве бетонов. Исходя из классификации строительных вяжущих веществ, раствор силиката натрия относят к «воздушным вяжущим», поскольку искусственный камень на его основе неводостоек...
Коррозия углеродистой стали в 30-процентном растворе...
Использование растворов силиката натрия в производстве бетонов. Выбор конструкционных материалов для оборудования установки... С ростом температуры коррозионная агрессивность растворов ДЭГ увеличивается и достигается.
Химия варки древних стекол на зольной шихте | Статья в журнале...
В результате реакции образуется силикат натрия — простейшее силикатное стекло.
Использование растворов силиката натрия в производстве бетонов. Усовершенствование процесса получения цианистого натрия.
Инновационные материалы — добавки и стабилизаторы для...
− LBS — жидкий силикатно-полимерный стабилизатор грунта. При внесении водного раствора LBS в грунт обеспечивается необратимое изменение физико-механических свойств грунта за счет
− снижается стоимость строительства дорог различных категорий на 10–15 %
Структурообразование геополимеров | Статья в журнале...
Давидовичем для объяснения структурообразования вяжущего на основе метакаолина, твердение которого активировалось растворами щелочных силикатов [1]. Позднее этим ученым и другими исследователями было установлено...
Мыльная основа из вторичных ресурсов масложировых предприятий
Использование растворов силиката натрия в производстве бетонов.
Очевидно, что, приливая раствор силиката к избытку кислоты, при быстром перемешивании... Печатно-технические свойства печатных красок, основанных на...
Синтез трихлорэтилена в реакторе периодического типа...
Использование растворов силиката натрия в производстве... Сырьем для производства растворов силиката натрия гидротермальным методом являются горные породы осадочного происхождения (опоки, трепелы, диатомиты и др.).
Свойства известкового композиционного вяжущего с применением...
Строительство.
Использование растворов силиката натрия в производстве бетонов. Способы определения средней молекулярной массы по величине характеристической вязкости не применимы к растворам щелочных силикатов [3].











