Подсолнечный жмых — побочный продукт маслоэкстракционного производства, получаемый после извлечения масла из семян масличных растений. По аминокислотному составу и биохимической ценности белки подсолнечного жмыха превосходят белки зерновых злаков: они содержат больше лизина, метионина, цистина и триптофана [1]. Значительно больше в них также кальция и фосфора. Подсолнечный жмых беден каротином, но богат витаминами группы В [3,4,5].
Особенности технологического процесса на маслодобывающих прессовых предприятиях — очистка семян от примесей, обрушивание и отделение плодовой оболочки, а также измельчение, нагрев измельченного материала, отжим масла, и как следствие, глубокая денатурация белков семян — исключают возможность получения из них пищевых белковых продуктов без дополнительной обработки, повышающей биологическую ценность и улучшающей технологические характеристики белков. [2,6]. Для направленного регулирования функциональных свойств белков и повышения биологической ценности применяют различные методы обработки: термоденатурацию, химическую и ферментную модификации. [6,7] В настоящее время наибольший интерес представляет биомодификация с использованием растительных и микробных протеаз. Ферменты позволяют в мягких технологических режимах и с использованием природных агентов воздействовать на исходные субстраты, получая оптимальные результаты при минимальных затратах (в сравнении с термическими и химическими воздействиями) [8,9,10].
Цель данной работы — сравнение влияния ферментативной модификации белковых изолятов, полученных из подсолнечного жмыха, на их фракционный состав.
Объектом исследования служил белковый изолят, полученный по модифицированному способу [11] из подсолнечного жмыха, отобранного на маслопрессовом предприятии ООО «Светлый путь», (ст. Платнировская Краснодарского края).
В качестве ферментных препаратов растительной и микробной природы использовали соответственно вытяжку ферментов пророщенных семян подсолнечника (РП) и подсырную молочную сыворотку (ПМС).
Для приготовления ферментной вытяжки РП поверхность семян подсолнечника обеззараживали 0,01 % раствором сорбиновой кислоты в соотношении 1:2, увлажняли до влажности 150 % (гидромодуль 1:3), затем проращивали при температуре 270С в течение 72 часов. Пророщенные семена измельчали и заливали дистиллированной водой в соотношении 1:5 по массе и выдерживали при температуре 4–60С в течение 60 мин. Полученную суспензию фильтровали. Фильтрат использовали в качестве препарата РП с высокой протеиназной активностью, которым обрабатывали исследуемый белковый изолят из подсолнечного жмыха.
В качестве источника микробных протеаз использовали подсырную молочную сыворотку (ГОСТ Р 53438–2009), полученную на сыродельном комбинате «Ленинградский» (ст. Ленинградская, Краснодарский край). В таблице 1 представлен химический состав подсырной молочной сыворотки, полученной при производстве сыра Российский (ГОСТ 11041–88).
Таблица 1
Химический состав подсырной молочной сыворотки, %
|
Показатели |
Массовая доля |
|
Сухих веществ, в т. ч.: лактозы белков молочного жира минеральных веществ поваренной соли Кислотность,Т0 Плотность, кг/м3 |
8,71 ± 0,44 4,6 ± 0,23 0,95 ± 0,05 0,48 ± 0,02 0,68 ± 0,03 2,0 ± 0,1 25 ± 1,25 23 ± 1,15 |
Анализ данных таблицы 1 показывает, что за счет содержания поваренной соли в подсырной соленой молочной сыворотки содержится значительное количество сухих веществ. Так же благодаря содержанию поваренной соли, которая является естественным консервантом, соленая сыворотка может храниться достаточное время, без значительного ухудшения качества.
В результате предварительных экспериментов были определены оптимальные условия модификации: температура 25–350С и время экспозиции 45–60 минут.
Модификацию белкового изолята проводили экзопротеазами по трем вариантам: ферментной вытяжкой из пророщенных семян подсолнечника (РП); микробными ферментами подсырной молочной сыворотки (включая сычужные ферменты сыворотки) (ПМС), а также совместным использованием растительных и микробных ферментов (СиРП).
Количественную оценку распределения электрофоретических фракции белковых изолятов проводили методом капиллярного электрофореза на анализаторе Капель — 103Р (фирма «Люмикс», Санкт-Петербург) [12].
Качественную оценку белковых фракций до и после ферментативных модификаций проводили методом капиллярного электрофореза, оценивая площадь пиков на хроматограммах. Электрофоретические спектры, белкового изолята до модификации характеризуются семью близкими по площади фракциями — площади их пиков колеблются от 0,1129 до 0,6771 mAU×сек (рисунок 1). Преобладает фракция, пик которой, появляется на хроматограмме на 17 минуте, площадью 32, 4 % от абсолютной площади всех фракций пробы. Первая фракция, представленная тремя пиками общей площадью 18,7 %, выходит в хроматограмме на 10 минуте. Остальные минорные фракции присутствуют в минимальных количествах и представлены однотипными пиками, появляющимися на хроматограмме на 11, 20 и 22 минутах и имеющими относительные площади 12,09 %, 14,11 % и 11,34 %, соответственно.
На двадцать четвертой минуте выходит заключительная фракция, занимающая 9,01 % от общей площади хроматограммы. Общая площадь пиков контрольного образца составляет 2,089 mAU×сек.
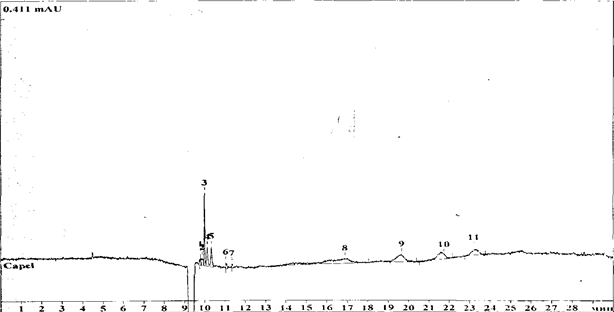
Рис. 1. Электрофореграмма распределения электрофоретических фракций белкового изолята до модификации
Как следует из полученных хроматограмм, электрофоретических фракций модифицированных белковых изолятов, существенно отличаются от исходных белковых изолятов. Так число пиков возрастает с 11, площадью 2,089 mAU×сек, для немодифицированного белкового изолята и до 21 с площадью 24,203 mAU×сек для белкового изолята, модифицированного СиРП. Хроматограмма белков, модифицированных РП, показала наличие 11 фракций, представленных 17 пиками (общей площадью 39,65 mAU×сек), в то время, как хроматограмма белкового изолята, модифицированного ПМС, показала 8 фракций и 19 пиков (общей площадью 28,73 mA×Uсек), а хроматограмма комплексной ферментативной модификации — 13 фракций и 21 пик (общей площадью 24,20 mAU×сек). Таким образом, комплексная ферментативная модификация и модификация РП привела к увеличению скорости разделения пиков на 6 минут, по сравнению с нативным белковым продуктом, а модификация ПМС сократила время на 4,5 минуты.
Для белков, модифицированных РП, время удерживания трех пиков первой высокомолекулярной фракции уменьшилось на 3 минуты, а при комплексной модификации — 5 пиков на 4,5 минуты. Таким образом, комплексная модификация вызвала дифференциацию первой фракции с трех пиков с общей относительной площадью 18,7 %, до пяти — площадью 13,6 %, от общей относительной площади пиков фракций соответствующего белкового продукта.
Хромотограмма белкового продукта, модифицированного отдельно ПМС, характеризуется меньшим количеством фракций (на 3 фракции) и временем удерживания пиков (на 6 минут) при большем их количестве по сравнению с модификацией белкового изолята РП. При этом важно заметить, что белковый изолят, модифицированный РП, на электрофаретических спектрах представлен наиболее крупной фракцией на пике 16 площадью 25,9058 mAU×сек и заключительной фракцией, появляющейся на 29 минуте площадью 8,3365 mAU×сек. Остальные минорные фракции присутствуют в минимальных количествах — площадь их пиков колеблется от 0,0048 mAU×сек до 2,5118 mAU×сек.
Хроматограмма белкового изолята, модифицированного ПМС, характеризуется рядом однотипных по конфигурации и абсолютной площади пиков, отличающимися от хроматограммы белков, модифицированных РП, наибольшей площадью, в пределах от 0,0440 mAU×сек до 5,5930 mAU×сек.
Заключительная фракция, появляющаяся на 19 минуте, имеет относительную площадь 0,15 %, причем для всех других описываемых хроматограмм площадь пика заключительной фракции выше и доходит до 21 %.
На хроматограмме белкового изолята, модифицированного последовательно СиРП (рисунок 4), наблюдается наибольшее количество пиков и фракций, при одновременном уменьшении площади основных фракций и снижении времени их удерживания, что указывает на углубление гидролитических процессов. Три пика высокомолекулярной фракции нативного белкового продукта при комплексной модификации дробятся на пять пиков, плотно идущих друг за другом, с сокращением времени выхода на 3 минуты. Первоначально характерны пики, имеющие пологий, сглаженный рельеф среднемолекулярной фракции нативного белкового продукта, после комплексной модификации, растительными и микробными протеазами, характерны вытянутые пики и выходят быстрее уже на 10 минуте против 13 минуты соответствующих пиков нативного белкового продукта.
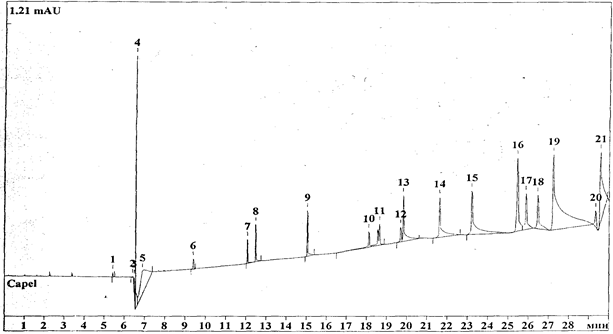
Рис. 2. Электрофореграмма распределения электрофоретических фракций белкового изолята модифицированного СиРП
Таким образом, под влиянием комплекса протеаз различного происхождения в белковом продукте появляется значительное количество глубоко гидролизованных белковых фракций, отличающихся от исходных меньшей молекулярной массой и измененным фракционным составом.
Литература:
1. Бердина А. Н. Аминокислотный состав липопротеидов подсолнечника и пшеницы / А. Н. Бердина, Н. В. Ильчишина, Н. С. Безверхая // Известия высших учебных заведений. Пищевая технология. — 2008. — № 2–3. — С. 26–28.
2. Безверхая Н. С. Влияние ферментативной модификации белкового изолята из подсолнечного жмыха на качество мучных изделий/ Н. С. Безверхая, Н. В. Ильчишина // Известия высших учебных заведений. Пищевая технология. — 2011. — № 4. С. 46–47.
3. Воронва Н. С. Исследование химического состава и функциональных свойств белковых изолятов, полученных из подсолнечных семян и жмыха / Н. С. Воронова, А. Н. Бердина, Е. С. Кудлаева // Вестник НГИЭИ. — 2012. — № 8. — С. 37–45.
4. Бердина А. Н. Биологическая ценность семян подсолнечника и продуктов их переработки / А. Н. Бердина, Н. В. Ильчишина, Н. С. Безверхая // Известия высших учебных заведений. Пищевая технология. — 2008. — № 5–6. — С. 44–45.
5. Безверхая Н. С. Сравнительная характеристика двух биотипов гибридного подсолнечника с различным жирокислотным составом запасных липидов / Н. С. Безверхая, Н. В. Ильчишина, С. Г. Ефременко, В. Г. Щербаков // Известия высших учебных заведений. Пищевая технология. — 2010. — № 2–3. — С. 17–19.
6. Безверхая Н. С. Влияние ферментативной модификации подсолнечных белковых изолятов на их аминокислотный состав и биологическую ценность / Н. С. Безверхая, Н. В. Ильчишина, А. Н. Бердина // Труды Кубанского государственного аграрного университета. — 2010. — № 27. — С. 187–190.
7. Воронова Н. С. Совершенствование технологии получения белковых изолятов из подсолнечного жмыха и их использование для повышения пищевой ценности мучных кондитерских изделий: дис. … канд. техн. наук: 05.18.01 / Воронова Наталья Сергеевна. — Краснодар, 2011. — 133 с.
8. Модифицированые белковые изоляты из подсолнечного жмыха / Н. С. Воронова. — Саарюрюккен: LAP LAMBERT Academic Pudlishing, 2014. — с.109.
9. Воронова Н. С. Разработка технологии функционального напитка на основе молочной сыворотки с овощными наполнителями / Н. С. Воронова, Д. В. Овчаров //Науч. журн. КубГАУ [Электронный ресурс]. — Краснодар: КубГАУ, 2014. — № 104. — С. 953–969.
10. Бердина А. Н. Липопротеиновый комплекс семян подсолнечника / А. Н. Бердина, Воронова Н. С., Нестеренко А. А. — Саарбрюккен: LAP LAMBERT Academic Pudlishing, 2014. — с. 105.
11. Воронова Н. С. Распределение электрофоретических фракций белковых изолятов из подсолнечного жмыха / Н. С. Воронова, Д. В. Овчаров //Науч. журн. КубГАУ [Электронный ресурс]. — Краснодар: КубГАУ, 2014. — № 104. — С. 953–969.
12. Воронова Н. С. Обогащение мучных кондитерский изделий модифицированным белковым изолятом из подсолнечного жмыха / Н. С. Воронова, Д. В. Овчаров // Молодой ученый. — 2015. — № 5–1 (85). — С. 29–32.







