В статье автор исследует свойства воды при кристаллизации.
Ключевые слова: вода, снег, лед, кристаллизация, плавление.
Вода при нормальных условиях находится в жидком состоянии, однако при температуре в 0 °C она переходит в твердое состояние — лед. Лёд встречается в природе в виде льда (материкового, плавающего, подземного), а также в виде снега, инея, изморози, вечной мерзлоты.
Актуальность: стремительно развивается глобальное потепление, изменяется климат в Арктике, тают «вечная» мерзлота и льды Северного полюса. Исследование свойств воды при кристаллизации поможет понять эти проблемы.
Объект исследования: процесс кристаллизации воды.
Предмет исследования: свойства воды при кристаллизации.
Цель работы: выполнить опыты по кристаллизации воды и подготовить предложения по их проведению.
Задачи: изучить информацию по теме; выполнить опыты по кристаллизации воды; сделать анализ результатов практической части.
Гипотеза: можно предположить, что на процесс кристаллизации воды влияет наличие соли в растворе, температура наружного воздуха.
Методы исследования:изучение,наблюдение,исследование, обоснование, анализ.
Практическая значимость работы: экспериментальное изучение процесса кристаллизации воды.
Вода является одним из самых удивительных веществ на планете Земля. Встретить воду можно практически везде в естественных условиях как на поверхности планеты, так и в ее недрах в трех возможных физических состояниях для веществ: жидкое, твердое, газообразное (то есть вода, лед, водяной пар).
При замерзании вода обладает уникальными свойствами расширения. Благодаря таким свойствам лед на воде, которая находится в виде жидкости, плавает.
Вода, как физическое вещество, характеризуется большим сродством сама с собой. Такое сродство у воды является самым большим среди всех жидкостей. Вследствие этого вода на поверхности размещается в виде капель сферической формы, поскольку сфера обладает наименьшей при заданном объеме поверхностью [1, 45].
Замерзание воды происходит не при температурных условиях ее наибольшей плотности (при 4 градусах Цельсия), а при нуле градусов Цельсия. Это свойства пресной воды. Однако, замерзание морской воды происходит при более низких температурах: минус 1,9 градусов Цельсия, при солености 35 %.
Вода обладает очень высокой теплоемкостью, относительно мало нагреваясь при этом.
Температура же в процессе замерзания или при кипении остается неизменной. Дистиллированная вода практически не проводит электрический ток, однако наличие в воде даже небольшого количества солей значительно увеличивает ее токопроводящие свойства [2, 94].
При смешивании соли со снегом наблюдается два процесса: разрушение кристаллической структуры соли, которое происходит с поглощением тепла, и гидрацией ионов. Последний процесс происходит с выделением тепла в окружающую среду. Для поваренной соли и хлористого кальция первый процесс превалирует над вторым. Поэтому при смешивании снега с этими солями происходит активный отбор тепла из окружающей среды. Ещё одна особенность соляных растворов состоит в том, что их точка замерзания ниже 0 градусов.
Чтобы снег на тротуарах таял при температуре ниже 0 градусов, его посыпают этими солями. Снег обладает удивительным свойством — памятью. Он сохраняет следы. По следам можно изучать физику [1, 108].
«Много снега — много хлеба», «Зима без снега — лето без хлеба», — справедливо утверждают старинные русские пословицы. В якутских народных пословицах и поговорках нет пословиц про хлеб. Однако в якутском фольклоре достаточно загадок про значение снега для флоры и фауны:«Некто, скрипя-кряхтя, снежным домом обзавелся» (куропатка), «Под землей горячая крица лежит» (медведь).
Снег — это лучший утеплитель для земли и растений, особенно рыхлый и лёгкий. Он защищает землю от глубокого промерзания и иссушения, а это важно для корневой системы растений. Кроме того, снег является хорошим строительным материалом для различных построек на севере — от иглу (жилищ эскимосов) до больших складских помещений [3, 211].
Снег — плохой проводник тепла. Снегом утепляют дома у нас зимой, насыпая его вокруг стен. Издавна снегом с водой утепляют коровники.
С 1980-х годов каждое десятилетие было теплее предыдущего — причина этого явления — парниковый эффект, который мы наблюдаем и в республике Саха (Якутия). Одним из следствий всемирного потепления является таяние ледников. Таяние ледников может привести к подъему уровня моря, что приведет к затоплению прибрежных районов. Нужно сделать все возможное для удержания глобального потепления в пределах 1,5°С [4].
Для проведения опытов с водой необходимо выбрать те, которые наиболее полно характеризуют и подтверждают свойства воды [5, 69]. Проведенный анализ показал, что лучше всего это будет реализовано при выполнении следующих опытов:
- Замерзание соленой воды.
- Расширение воды при замерзании.
- Замерзание мыльных пузырей.
- Срастание сосульки.
- Скрип сухого снега.
- Примерзание к поверхности.
- Измерение силы трения при движении санок по снегу при разных температурах воздуха.
- Опыт № 1. Замерзание чистой и соленой воды
Налили в три пластиковых стакана воду — чистую и солёную. Вынесли их на мороз. Чистая пресная вода превратилась в лёд через несколько часов, а солёная замёрзла только при сильном морозе.
Замерзание воды происходит при 0 градусов Цельсия. Это свойство пресной воды. При этом, морской лед отличается от пресноводного в ряде отношений. У соленой воды температура замерзания понижается по мере увеличения солености. В диапазоне солености от 30 до 35 % температура замерзания меняется от -1.6 до -1.9 град.
Измерения начали 14.11.2023 г., вечером в 18.00. Температура наружного воздуха была равна -10°С. Температуру измеряли уличным термометром и сверялись с показаниями температуры Вилюйской метеостанции. Данные проведенных опытов приведены в таблицах 1–5.
Таблица 1
Измерение температуры наружного воздуха в г. Вилюйск, ноябрь 2023 г.
|
№ |
Дата |
Температура наружного воздуха |
Скорость ветра по данным метеостанции |
Направление ветра по данным метеостанции | |
|
Утром |
Ночью | ||||
|
1 |
14.11 |
-11 |
-14 |
2 |
Юг-юг-восток |
|
2 |
15.11 |
-12 |
- 14 |
2 |
Южный |
|
3 |
16.11 |
-13 |
-15 |
2 |
Юг-юг-запад |
|
4 |
17.11 |
-2 |
-7 |
3 |
Южный |
|
5 |
18.11 |
-15 |
- 23 |
2 |
Западный |
|
6 |
19.11 |
-20 |
- 29 |
1 |
Восточный |
|
7 |
20.11 |
-11 |
-16 |
4 |
Восток-сев-восток |
|
8 |
21.11 |
-23 |
-29 |
3 |
Западный |
|
9 |
22.11 |
-30 |
-33 |
2 |
Западный |
|
10 |
23.11 |
- 33 |
- 35 |
2 |
Запад- юго-запад |
|
11 |
24.11 |
-37 |
-39 |
2 |
Юго-запад |
|
12 |
25.11 |
-38 |
-33 |
2 |
Запад- юго-запад |
|
13 |
26.11 |
-35 |
-29 |
2 |
Запад- юго-запад |
|
14 |
27.11 |
-22,8 |
-17 |
2 |
Северо-запад |
|
15 |
28.11 |
-13,3 |
-10 |
2 |
Северный |
|
16 |
29.11 |
-22,7 |
-17 |
2,4–3,5 |
Западный |
|
17 |
30.11 |
- 14,5 |
-13 |
4,3–5,4 Порывы до 15м/с |
Западный |
Таблица 2
Измерение температуры чистой воды, помещенной на улице
|
Дата |
Время |
Температура раствора, °С |
Образование льда |
|
14.11 |
18.00 14.11 |
23 |
Корка |
|
14.11 |
19.00 |
-1 |
Корка |
|
14.11 |
21.00 |
-2 |
Корка |
|
14.11 |
22.00 |
-3 |
Корка |
|
14.11 |
23.00 |
-3 |
Корка |
|
15.11 |
06.00 |
-9 |
Полностью заледенела |
Таблица 3
Измерение температуры 10 % соленой воды, помещенной на улице
|
Время |
Температура раствора, °С |
Образование льда |
|
20.00 21 ноября |
20 |
- |
|
21.00 |
- 4 |
Мало льда |
|
22.00 |
- 8 |
Частично лед |
|
23.00 |
-8 |
Частично лед |
|
06.00. 22 ноября |
-23 |
Полностью лед, на поверхности тонкий слой воды |
Вывод:
1) чистая вода, вынесенная на мороз 14 ноября, замерзла полностью при ночной температуре -14°С. Ее температура постепенно понижалась с комнатной температуры (23°С), до температуры кристаллизации 0°С;
2) 10 % раствор соленой воды, вынесенный на мороз 21 ноября, замерз полностью при ночной температуре -29°С;
3) 43 % солёная вода, вынесенная на мороз 14 ноября, не замерзала несколько дней, замерзла 23.11 при ночной температуре –33°С. У соленой воды температура замерзания понижается по мере увеличения солености.
Опыт 2. Наблюдение вымерзания соли из раствора соленой воды
Налили в одноразовые сосуды воду с солью: 40 % и 10 %. Вынесли их на мороз.
Таблица 4
Измерение температуры 43 % соленой воды, помещенной на улице
|
Время |
Температура раствора, °С |
Образование льда |
|
18.00 14.11 |
23 |
Нет |
|
19.00 |
0 |
Нет |
|
20.00 |
-5 |
Нет |
|
21.00 |
-7 |
Нет |
|
22.00 |
-8 |
Нет |
|
23.00 |
-8 |
Нет |
|
06.00 15.11 |
-7 |
Нет |
|
18.00 21.11 |
-18 |
Нет |
|
06.30 21.11 |
- 19 |
Нет |
|
18.00 22.11 |
-23 |
Наблюдается вымерзание соли из воды |
|
06.30 23.11 |
- 23 |
Полностью кристаллизировалась вода. На поверхности льда находится соль |
Оба раствора замерзают по-разному. 22 ноября 2023, температура наружного воздуха -27°С, наблюдается вымерзание соли из воды.
Температура 43 % раствора — 20° С.

Рис. 1. Вымерзание соли из 40 %-го раствора соли при температуре воздуха -27°С.
23.11.2023, 06.30 мин. вода полностью кристаллизовалась. 22.11.2023, температура наружного воздуха -33°С.
Температура 10 % раствора — 15°С. На поверхности наблюдается с вымерзание соли из воды. В центре и по краям находится тонкий слой воды (рис. 2).

Рис. 2. Вымерзание соли из 10 % раствора соли при температура наружного воздуха -33°С.
Наблюдение кристаллизации 43 % соленой воды, помещенной на улице, проводили с 14 ноября по 23 ноября. При небольших морозах (меньше 30°С) 43 % соленая вода не замерзает. При понижении температуры ниже 30°С начинается вымерзание соли из раствора. При температуре -35°С раствор полностью превращается в лед (рис. 5).

Рис. 3. Вымерзание соли в сосудах № 1 (43 %) и № 2 (10 %)
В Сунтарском улусе Республики Саха (Якутия) есть соленое озеро Кэмпэндээйи. В ней солёная вода (90 % рассол) круглосуточно, зимой и летом изливается в бассейн из-под земли по вертикальным трубам. Зимой соль из воды вымораживается. Весной, под действием солнечного тепла, вода постепенно испаряется, и в бассейне накапливается (пищевая) соль.
Летом её сгребают в кучу. Издали кажется, что и летом, в 30-градусную жару все покрыто снегом.
Чем холоднее зима, тем лучше для добытчиков соли. «При сильных морозах из-под земли выходит много соли в виде рассола, которая тут же кристаллизуется, а весной превращается в обычную поваренную соль, которую, как и при царской России, возят на деревянных тележках».
Вывод: вымерзание соли из воды зависит от % содержания соли в растворе. Быстрее соль вымерзла из 10 % раствора, при температуре наружного воздуха –15°С.
Раствор с 43 % содержанием соли не замерзал до 23.11. Соль вымерзла 23.11, при морозе –33°С.
Вымораживание соли можно рассматривать как замерзание пресной воды с вытеснением соли на поверхность льда. Когда температура достигает точки замерзания, образуются кристаллы соли, которые «окружают» не замерзшую воду.
Вымерзание соли зависит от % содержания соли в растворе. Вымерзание соли в растворах с 30 % содержанием соли и больше происходит при морозах ниже 30°С.
Опыт № 3. Расширение воды при замерзании
Наполнили водой пластиковый стакан, пластиковую бутылку и стеклянную бутылку. Выставили их на мороз. Вода в пластиковом стакане замерзая, выпучивается по центру. При замерзании воды в пластиковой бутылке бутылка остается целой.
При замерзании воды в стеклянной бутылке вода разрывает бутылку.
Вывод: замерзая, вода увеличивается в объёме. Замерзшая вода «вылезает» из стакана.
В сильные морозы основная причина аварий на водопроводах — замерзание текучей воды. Происходит ее расширение, так что образующийся лед легко разрывает трубы, так как плотность льда — 917 кг/м 3 , а плотность воды — 1000 кг/м 3 , то есть объем увеличивается в 1,1 раза, что довольно существенно.
Плотность льда — 917 кг/м 3 , а плотность воды — 1000 кг/м 3 , то есть объем увеличивается в 1,1 раза.
Масса = Плотность *Объем
Объем =
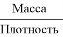
V льда — объем льда, V воды — объем воды
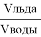
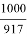
При замерзании водыобъем увеличивается в 1,1 раза. Поэтому стеклянная бутылка разрывается.
Опыт № 4. Замерзание мыльных пузырей (22 ноября, температура воздуха -33°С)
Приготовили мыльный раствор из жидкого мыла. Раствор на морозе держали в рукавице, чтобы он не замёрз. На практике мы увидели, что тонкая мыльная плёнка на морозе быстро замерзает, превращая пузыри в ледяные шарики, которые сразу лопаются [5].
Вывод: тончайшая пленка мыльного пузыря замерзает за считанные секунды и лопается, так как из-за большой разницы температур объем шара увеличивается.
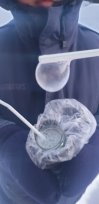


Рис. 4–6
Опыт № 5. Срастание сосульки
Собрали несколько сосулек. Выбрали из них сосульку толщиной 15 мм и шириной 25 мм, закрепили ее горизонтально при помощи двух штативов. Перекинули через неё тонкую проволоку, концы которой утяжелили грузом массой 100 г. Наблюдали, как проволока растапливает лёд, проникает всё глубже в сосульку. Вода над сосулькой вновь замерзает. Это подтверждает поглощение тепла при плавлении льда. Лед нарастает сверху, сразу над проволокой, так как стекающая вниз талая вода замерзает при соприкосновении с холодными стенками сосульки.
Вывод: при подвешивании груза к горизонтально закрепленной сосульке, проволока растапливает лед. Стекающая вниз талая вода замерзает, так как температура стенок сосульки 0°С.
|
Рис. 7. Начало срастания льда |
Рис. 8. Конец плавления |
Опыт № 5. Скрип сухого снега
В морозные дни звук распространяется на большие расстояния. Снег скрипит только в мороз (ниже -5°C), и звук скрипа меняется в зависимости от температуры воздуха — чем крепче мороз, тем выше тон скрипа. Мы записали скрип снега при разных температурах наружного воздуха.
Таблица 5
Измерение зависимости тона скрипа от температуры наружного воздуха
|
Время |
Температура воздух, °С |
Тон скрипа |
|
23.00 (21.11) |
- 24 |
Низкий |
|
23.00 (22.11) |
-27 |
Низкий |
|
23.00 (23.11) |
- 30 |
Средний |
|
24.11 |
-37 |
Высокий |
|
25.11 |
-38 |
Высокий |
Скрип образуется из-за того, что при давлении разрушаются мельчайшие кристаллики снега. Хотя каждый из них по отдельности очень мал, но вместе они ломаются довольно громко.
Усиление морозов делает ледяные кристаллики более твердыми и хрупкими. При каждом шаге ледяные иглы ломаются. При температуре воздуха ниже -50°C скрип снега становится таким сильным, что его можно слышать через тройные стекла (этому способствует также большая плотность морозного воздуха).
Вывод:скрип снега изменяется с понижением температуры наружного воздуха, его тон становится выше.
Заключение
Процесс кристаллизации воды можно изучать в домашних условиях, а также на уроках в средней и начальной школе.
В ходе работы выполнили шесть опытов и описали основные результаты, подготовили предложения по проведению опытов. Мы убедились, что кристаллизация воды зависит от наличия соли в растворе воды. С ростом %-го содержания соли снижается температура замерзания. 10 % раствор соленой воды, вынесенный на мороз, замерзает при ночной температуре -29°С; 43 % солёная вода, вынесенная на мороз 14 ноября, не замерзала несколько дней, замерзла при ночной температуре –33°С.
Вымерзание соли из воды зависит от % содержания соли в растворе. Быстрее соль вымерзла из 10 % раствора, при температуре наружного воздуха — 15°С. Соль из 43 %-го раствора вымерзла 23.11, при морозе –33°С.
Вымораживание соли можно рассматривать как замерзание пресной воды с вытеснением соли на поверхность льда. Когда температура достигает точки замерзания, образуются кристаллы соли, которые «окружают» не замерзшую воду.
Тончайшая пленка мыльного пузыря замерзает за считанные секунды и лопается, так как из-за большой разницы температур объем шара увеличивается.
При подвешивании груза к горизонтально закрепленной сосульке, проволока растапливает лед. Стекающая вниз талая вода замерзает, происходит срастание сосульки, так как температура стенок 0°С.
Скрип снега изменяется с понижением температуры наружного воздуха, его тон становится выше.
При добавлении соли в снег температура смеси резко понижается, кастрюля со снегом примерзает к бумаге и картону, на которой стояла. При смешивании соли со снегом наблюдается сильное охлаждением вследствие большого поглощения теплоты льдом при его плавлении и солью при ее растворении.
Сила трения при скольжении санок по снегу зависит от температуры воздуха: чем мороз крепче, тем больше его значение.
Гипотеза, что на процесс кристаллизации воды влияют наличие соли в растворе и температура наружного воздуха, подтвердилась. Цель достигнута.
Литература:
- Природа и люди. Хрестоматия по природоведению для учителей. Сост. В. П. Горошенко. М., «Просвещение», 1971.- 336 с.с илл.;
- Энциклопедия для любознательных от А до Я: энциклопедия/Л. В. Калинина, Ю. В. Шуйская. — М.: Эксмо, 2016. — 256с: ил.;
- Энциклопедия окружающего мира: энциклопедия/Джон Кларк, Клинт Твист. — М.: Махаон, 2000. — 301с: ил.;
- https://rg.ru/ecology;
- https://rosuchebnik.ru/material/issledovanie-svoystv-vody-pri-kristallizatsii-7383/



