В условиях роста городов и увеличения антропогенной нагрузки важна оценка здоровья почв урбоэкосистем. Почвенные ферменты — биоиндикаторы, быстро реагирующие на химическое загрязнение. Изучение их активности позволяет делать выводы о чувствительности почвенной экосистемы к солевому загрязнению.
Отбор проб проводили весной 2026 г. на проталинах в Гурьяновском лесопарке на удалении от проезжей части в 3 точках по 3 повторности (рис. 1).
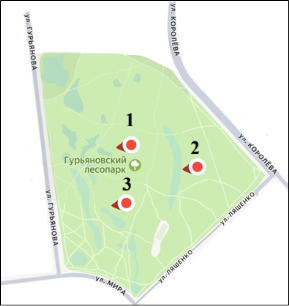
Рис. 1. Места отбора почвенных проб
Гурьяновский лесопарк находится в окружении городской застройки (улицы Королёва, Ляшенко, Мира, Гурьянова) и является важной рекреационной зоной. Почвы в основном дерново-подзолистые различного механического состава, что характерно для северной части Калужской области [2, с. 4]. Прошло более недели после схода снега, участки прогревались солнцем, так что запустилась работа почвенных ферментов. Отбор верхнего слоя почвы проводился на глубине до 5 см, так как в этом слое наблюдается максимальная ферментативная активность [5, с. 48]. Корневая система высших растений является источником анализируемого фермента каталазы в почве. Отделение ризосферы от корневой системы проводили методом встряхивания по Красильникову [5, с. 57]. Для определения биологической активности каталазы использовали биохимические методы (титриметрический метод Р. С. Кацнельсона, В. В. Ершова) [10, с. 33]. Титрование проводили на базе физико-химической лаборатории ИАТЭ НИЯУ МИФИ.
Каталазную активность почвы выражают в миллилитрах 0,1 н KMnO 4 за период времени, объем которого является разностью между опытными и контрольными измерениями. В контрольном образце фермент денатурирует при прогревании почвы в термостате. В опытном образце часть внесенной перекиси водорода разлагается под действием фермента:
2 H 2 O 2 → 2 H 2 O + O 2 ↑
Реакцию останавливают внесением серной кислоты, создавая кислую среду. Количество непрореагировавшей перекиси водорода определяют титрованием перманганатом калия в кислой среде:
5H 2 O 2 + 2 KMnO 4 + 3 H 2 SO 4 → 2 MnSO 4 + K 2 SO 4 + 5 O 2 + 8H 2 O
Разность между количествами перекиси, внесенной в реакционную среду и обнаруженной после взаимодействия с почвенными ферментами, равняется количеству расщепленной перекиси и характеризует активность каталазного действия почвы.
Существует 3 варианта выражения каталазной активности:
— в мл KMnO 4 на 1 г почвы за определённое время (обычно 1 мин или 20 мин):
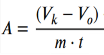
— в мг H 2 O 2 на 1 г почвы за определённое время:
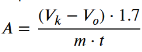
— в см 3 (мл) выделившегося O 2 на 1 г почвы за определенное время [6, с. 17]:
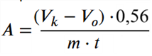
A — каталазная активность,
V k — объем раствора KMnO 4 , пошедший на титрование контрольной пробы, мл,
V 0 — объем раствора KMnO 4 , пошедший на титрование опытной пробы, мл.
m — масса воздушно-сухой почвы, г,
t — время взаимодействия почвы с перекисью, мин.
Также используются коэффициенты 1,7 и 0,56 для пересчета 1 мл 0,1 н раствора KMnO 4 на эквивалент мг H 2 O 2 или O 2 .
Все данные по ферментативной активности почв приведены для воздушно-сухих образцов и статистически обработаны в программе «Microsoft Excel». Результаты каталазной активности почвы до внесения бытового загрязнителя отражены в табл. 1.
Таблица 1
Каталазная активность почвы (А) до внесения бытового загрязнителя
|
№ пробы почвы |
А, мл KMnO 4 / г/20 мин |
А, мл KMnO 4 /г /мин |
А, мг H 2 O 2 /г /мин |
А, cм 3 O 2 /г /мин |
|
экспозиция 20 минут |
экспозиция 150 минут | |||
|
1 |
0,59 ± 0,01 |
4,42 ± 0,03 |
7,51 ± 0,05 |
2,48 ± 0,02 |
|
2 |
0,48 ± 0,01 |
3,62 ± 0,06 |
6,15 ± 0,10 |
2,03 ± 0,03 |
|
3 |
0,63 ± 0,01 |
4,74 ± 0,03 |
8,06 ± 0,06 |
2,65 ± 0,02 |
|
Среднее |
0,57 ± 0,01 |
4,26 ± 0,04 |
7,24 ± 0,06 |
2,39 ± 0,02 |
Данные по изучению активности каталазы почв Обнинска титриметрическими методами практически отсутствуют, нам удалось найти всего одну работу, в которой рассматривалась бы каталазная активность почв Обнинска (опыт) и Боровского района (контроль) [7, с. 10]. Однако каталазная активность была изучена в летний период, когда показатель выше весенних и осенних значений; в опытных образцах он колебался в диапазоне 2,0–4,2 см 3 O 2 /г/мин, а в контроле составлял 3,0–3,5 см 3 O 2 /г/мин. Тем не менее полученные нами в пересчете результаты (2,39 ± 0,02 см 3 O 2 / г/мин) согласуются с данными этого автора для почв нашего города.
Активность каталазы титриметрическими методами в почвах ближайших регионов рассматривается в небольшом числе работ. Так, в почвах природно-рекреационных ландшафтов г. Владимир со слабой техногенной нагрузкой каталазная активность колебалась в пределах 0,2–0,53 мл KMnO4/г/20 мин и соответствовала значениям контрольных образцов с незагрязненных территорий области [4, эл. ресурс]. В нашем случае активность каталазы оказалась близкой по значению (0,48–0,63 мл KMnO4/г/20 мин), и мы предположили, что исследуемые нами почвы центральной части Гурьяновского лесопарка в начале весны также испытывают минимальное техногенное воздействие. В работе Самусик Е. А., Головатый С. Е. получено значение каталазной активности для дерново-подзолистых почв леса (контроль): 2,1–7,0 мл O 2 / г/мин области [9, с. 109]. Наши данные в пересчете (2,39 ± 0,02 см 3 O 2 / г/мин) согласуются с результатами исследований этих авторов для фоновых дерново-подзолистых почв. Однако такой показатель по сравнительной шкале оценки биологической активности почвы характерен для почв с низким (1–3 см 3 O 2 /г/мин) уровнем работы фермента каталазы области [5, c. 47], что, возможно, связано с проведением исследования, спустя небольшой период времени после таяния снега и в целом невысоким естественным плодородием, содержанием микробиоты в дерново-подзолистых почвах.
Работ, в которых проводилось бы изучение загрязнения почв Обнинска бытовыми отходами, нам найти не удалось, в государственных докладах и научных статьях в основном акцентируют внимание на загрязнении почв тяжелыми металлами [3, с.70; 2, с. 170]. Вместе с тем интерес также представляет изучение засоления городской почвы и чувствительности к этому фактору почвенных ферментов. NaCl — самый распространённый компонент противогололедных смесей [1, с. 1081] из-за своей эффективности и низкой стоимости. Галит отличается от пищевой соли более крупным помолом, меньшей степенью очистки и наличием природных примесей, но это все равно NaCl, поэтому мы остановились на выборе данного бытового загрязнителя, поскольку с учетом особенностей зимы 2025–2026 гг. пешеходные дорожки и проезжая часть Обнинска посыпались противогололедными смесями неоднократно и обильно. Мы внесли хлорид натрия во все почвенные пробы и провели повторное титрование через 7 дней (период взаимодействия фермента с перекисью водорода до титрования — 150 мин), полученные данные занесли в таблицу 2.
Таблица 2
Каталазная активность почвы (А) после внесения бытового загрязнителя хлорида натрия (NaCl)
|
№ пробы почвы |
А, мл KMnO 4 /г/мин |
А, мг H 2 O 2 /г/мин |
А, cм 3 O 2 /г/мин |
|
1 |
2,50 ± 0,01 |
4,25 ± 0,04 |
1,40 ± 0,02 |
|
2 |
2,60 ± 0,01 |
4,42 ± 0,03 |
1,46 ± 0,01 |
|
3 |
2,90 ± 0,02 |
4,93 ± 0,04 |
1,62 ± 0,02 |
|
Среднее |
2,67 ± 0,01 |
4,53 ± 0,04 |
1,49 ± 0,02 |
На титрование уходило больше перманганата калия, чем до внесения соли в почву, значит в пробах оставалось много неразложившейся перекиси водорода, следовательно, активность каталазы снизилась. Снижение активности фермента составило 37 %. Это показатель зависит от того, какая соль входит в состав противогололедной смеси и для NaCl обычно приводится диапазон 20–50 % [1, с. 1081]. В Москве, где техногенная нагрузка значительно выше, в 2024 году у дорог содержание хлорида натрия составляло в пересчете на 1 грамм почвы в среднем 2,76 мг [1, с. 1083], фоновое значение в незагрязненной почве может составлять 0,25 мг NaCl/г почвы. Для почв Обнинска подобных данных найти не удалось. На основании этого было решено внести в образцы почвы соль в количестве 1 мг/г почвы.
Снижение ферментативной активности почв объясняется несколькими причинами:
- Осмотический стресс. Высокая концентрация солей приводит к осмотическому обезвоживанию микробных клеток, которые являются основными продуцентами ферментов. Это вызывает гибель клеток и высвобождение внутриклеточных ферментов, которые становятся уязвимыми для разрушения почвенными протеазами.
- Изменение свойств ферментов. Соли могут вызывать конформацию активного центра фермента, нарушая его работу.
- Специфическая ионная токсичность. Ионы Na⁺ и Cl⁻ нарушают метаболизм микроорганизмов, подавляя их рост и синтез новых молекул фермента каталазы мг.
Степень замедления работы фермента зависит от типа действующей соли. По убыванию силы негативного воздействия на ферменты образуется ряд: NaCl > CaCl₂ > Na₂SO₄ [1, с. 1086; 8, с. 84].
Таким образом, мы изучали воздействие одного из наиболее мощных и распространенных бытовых загрязнителей почв города, вызывающего их деградацию и снижение активности каталазы.
Литература:
- Воронина Л. П., Донерьян Л. Г., Сбитнев А. В., Водянова М. А. Определение показателей контроля и уровней безопасности применения противогололёдных материалов для гигиенической оценки объектов окружающей среды // Гигиена и санитария, 2024. — Т. 103, № 10. — С. 1080–1088.
- Доклад о состоянии природных ресурсов и охране окружающей среды на территории Калужской области в 2024 году / Правительство Калужской области; Министерство природных ресурсов и экологии Калужской области — Калуга, 2024. — 745 с.
- Дроздова Н. И., Макаренко Т. В., Куртасова Е. В. Экспериментальное моделирование при изучении биологической активности почв // Экологический вестник, 2016. — № 4 (38). — С. 68–74.
- Забелина О. Н. Ферментативная активность почвы природно-рекреационных ландшафтов урбанизированных территорий // Научное обозрение. Биологические науки, 2015. — № 1. URL: https://science-biology.ru/ru/article/view?id=270 (дата обращения: 04.12.2025).
- Козлов А. В. Методы почвенной микробиологии и энзимологии в экосистемных исследованиях: учебно-методическое пособие для вузов. — М.: Плодородие, 2023. — 152 с.
- Королюк М. А. Метод определения активности каталазы // Лабораторное дело, 1988. — № 1. — С. 16–19.
- Павлова Н. Н. Пространственно-временные изменения биологической активности городских почв (на примере г. Обнинска): автореферат дис.... канд. биол. наук. Москва, 2008. — 21 с.
- Поляк Ю. М., Сухаревич В. И. Почвенные ферменты и загрязнение почв: биодеградация, биоремедиация, биоиндикация // Агрохимия, 2020. — № 3. — С. 83–93.
- Самусик, Е.А., Головатый, С. Е. Ферментативная активность дерново-подзолистых почв в условиях воздействия выбросов предприятия по производству строительных материалов // Журнал Белорусского государственного университета. Экология, 2022. — № 1. — С. 104–113.
- Хазиев Ф. Х. Методы почвенной энзимологии. — М.: Наука, 2005. — 251 с.

