За последние несколько десятилетий интерес учёных сместился в сторону заболеваний, связанных с мозгом, и токсического воздействия металлов. В связи с этим изучению этих металлов было посвящено множество исследований. Достоверно известно, что большая часть повреждений мозга, вызванных воздействием соединений металлов, может привести к необратимым повреждениям мозга или снижению его активности.
Анализ медицинской литературы показал недостаточное наличие сведений о распространенности, масштабах и особенностях нарушения памяти у пациентов с накоплением поливалентных металлов и их роли в патогенезе когнитивных нарушений. В этом исследовании мы стремились изучить особенности мнестических трудностей у лиц с избыточным накоплением поливалентных металлов, уделяя особое внимание взаимосвязи между состоянием когнитивного статуса с учетом длительности заболевания. Мы рассматривали влияние тета-ритма на процесс восстановления памяти и оценивали когнитивный дефицит с помощью шкал и данных нейровизуализации, принимая во внимание показатели лабораторных анализов, результаты электроэнцефалограммы (ЭЭГ).
Гиппокамп является одной из главных структур мозга человека и других позвоночных. В мозге человека гиппокамп, зубчатая извилина и субикулум (от лат. subiculum — подставка, опора) являются компонентами гиппокампальной формации, расположенной в лимбической системе. Гиппокамп играет важную роль в консолидации информации из кратковременной памяти в долговременную, а также в пространственной памяти, обеспечивающей навигацию. При различных формах деменции и снижении памяти гиппокамп является одной из первых областей мозга, которая подвергается повреждению — потеря кратковременной памяти и дезориентация входят в число ранних симптомов.
Актуальность данного исследования состоит в том, что у пациентов с орфанными нейродегенеративными заболеваниями наблюдается нарушение когнитивного статуса, в частности, памяти, приводящее к снижению качества жизни и ухудшению клинического прогноза. Учитывая ограниченное число публикаций по данной проблематике и манифестацию заболевания в молодом и среднем возрасте, существует острая потребность в исследовании подробных характеристик нарушения памяти в зависимости от избыточного накопления меди и железа в головном мозге, а также роли тета-ритма при неинвазивной аудиостимуляции структур гиппокампа. В статье [1] достаточно подробно изложен тот факт, что переходные металлы, железо и медь, являются кофакторами для множества белков, жизненно важных для нормального функционирования клеток.
Современные ученые все большее внимание уделяют методам, объективизирующим информацию о когнитивных функциях [3]. Одни из значимых примеров орфанных заболеваний — болезнь Вильсона — Коновалова (БВК) и нейродегенерации с накоплением железа в мозге (ННЖМ). Во втором случае мозг пациентов содержит включения из отложений железа в виде бурых пятен, что иногда характерно и при «больших» нейродегенерациях [2]. В Международной статистической классификации болезней и проблем, связанных со здоровьем, десятого пересмотра (МКБ-10) болезнь Вильсона -Коновалова обозначают кодом Е83.0 («Нарушения обмена меди»), нейродегенерации с накоплением железа в мозге (ННЖМ, БГШ) — G23.0.
В настоящей статье мы осветим историю открытия болезни Вильсона — Коновалова и на примере клинического случая пациентки с БВК продемонстрируем применение аудиостимуляции.
В 1883 году Карлом Фридрихом Вестфалем, немецким невропатологом и психиатром, было описано заболевание, которое по клиническому сходству с рассеянным склерозом получило название «псевдосклероз». Заболевание характеризовалось распространёнными, размашистыми, ритмичными непроизвольными движениями, повышением мышечного тонуса, амимией, дизартрией и выраженными психическими нарушениями вплоть до такого расстройства интеллекта, как слабоумие. В 1912 году английский невролог Сэмюэль Вильсон описал заболевание, для которого были характерны изменения в головном мозге и постоянное наличие цирроза печени, и дал описание клиники нового заболевания, названного им прогрессивной лентикулярной дегенерацией (лат. lenticularis — чечевицеобразный). В качестве основных симптомов заболевания были отмечены разнообразные непроизвольные движения в конечностях и туловище, мышечная ригидность, приводящая к скованности, дисфагия и дизартрия, аффектные вспышки, иногда психические расстройства, но признаки поражения пирамидных путей отсутствовали.
В дальнейшем оказалось, что прогрессивная лентикулярная дегенерация и псевдосклероз являются разными формами одного и того же заболевания, которое австрийский врач Галль в 1921 году назвал гепатолентикулярной дегенерацией. Изменения в мозге при данном заболевании никогда не ограничиваются лентикулярными ядрами и нередко бывают значительно выражены в других отделах мозга. Поэтому в 1960 году русский невролог Николай Васильевич Коновалов предложил название «гепатоцеребральная дистрофия». Он значительно расширил представления о патофизиологии, патогенезе и клинике этой болезни и выделил новые её формы [4]. На рисунке 1 представлены ученые, которые внесли вклад в изучение заболевания, которое со временем в нашей стране стало называться болезнью Вильсона — Коновалова.

Рис. 1. Карл Фридрих Вестфаль, Сэмюэль Вильсон и Н. В. Коновалов
Болезнь Вильсона — Коновалова — редкое наследственное заболевание, наследуемое по аутосомно-рецессивному типу (мутантный ген расположен в длинном плече 13 хромосомы), проявляющееся преимущественно в молодом возрасте и характеризующееся избыточным накоплением меди в организме, преимущественно в печени и нервной системе (базальные ядра, таламус, мозжечок, кора головного мозга). Распространенность заболевания в среднем — 30 случаев на 1 млн. человек [6]. В мире заболевание регистрируется с частотой 1: 35–100 тыс. новорожденных (уже насчитывается 10–30 млн. больных); носительство патологического гена отмечается в 0,56 % случаев. В США частота выявления болезни Вильсона составляет 1:30 тыс. населения; носители мутантного гена обнаруживаются с частотой 1:90. Высокая заболеваемость отмечается в регионах, где существуют близкородственные браки (Иран, Йемен, Ирландия), а также в Японии и на острове Сардиния. Так, в Японии болезнь Вильсона — Коновалова диагностируется с частотой 1:30 тыс.; для сравнения в Австралии — 1:100 тыс. населения.
Заболевание чаще манифестирует в молодом возрасте и без лечения быстро прогрессирует, заканчиваясь гибелью пациента [7]. Болезнь Вильсона — Коновалова встречается одинаково часто как у мужчин, так и у женщин. Болезнь манифестирует в возрасте 8–16 лет, однако неврологические симптомы появляются только к 19–20 годам. У детей младше 5 лет проявления болезни Вильсона нередко могут отсутствовать, хотя заболевание иногда диагностируется как у пациентов в возрасте до 3 лет, так и у людей, которым уже за 50. Без лечения болезнь Вильсона — Коновалова приводит к летальному исходу (примерно в возрасте 30 лет) в результате печеночной, почечной недостаточности, а также геморрагических осложнений. В основе заболевания лежит нарушение баланса между поступлением и экскрецией меди. Этот избыток меди сначала накапливается в печени, а затем попадает в кровь, центральную нервную систему (ЦНС) и в другие органы [9].
Медь является переходным металлом, и избыточное содержание меди приводит к образованию токсичной гидроксильной группы и усилению окислительного стресса в клетках. Этот окислительный стресс повреждает клетки и приводит к клиническим проявлениям, а именно к печеночной недостаточности, поведенческим и когнитивным нарушениям, расстройствам движений и появление кольца Кайзера-Флейшера в роговице [11].
После того как печень насыщена медью, что в ряде случаев происходит бессимптомно, накопление меди происходит в других органах и системах, прежде всего в базальных ядрах головного мозга, в которых содержание меди увеличивается в 50 и более раз по сравнению с нормой.
Русский невролог Н. В. Коновалов (1960 г.) выделил 5 форм гепатоцеребральной дистрофии [4]:
- Абдоминальная (печеночная) форма — тяжелое поражение печени, приводящее к смерти раньше появления симптомов со стороны нервной системы; заболевают дети. Её продолжительность от нескольких месяцев до 3–5 лет.
- Ригидно-аритмогиперкинетическая (ранняя) форма — отличается быстрым течением; начинается также в детском возрасте. В клинической картине преобладают мышечная ригидность, приводящая к контрактурам, бедность и замедленность движений, хореоатетоидные или торсионные насильственные движения. Характерны дизартрия и дисфагия, судорожный смех и плач, аффективные расстройства и умеренное снижение интеллекта. Заболевание длится 2–3 года, заканчивается летально.
- Дрожательно-ригидная форма — встречается чаще других; начинается с юношеского возраста, течёт медленнее, порой с ремиссиями и внезапными ухудшениями, сопровождающимися субфебрильной температурой; характеризуется одновременным развитием тяжёлой ригидности и дрожания, дрожание очень ритмичное (2–8 дрожаний в секунду), резко усиливается при статическом напряжении мышц, движениях и волнении, в покое и во сне исчезает. Иногда обнаруживаются атетоидные хореоформные насильственные движения. Средняя продолжительность жизни — около шести лет.
- Дрожательная форма заболевания — начинается в возрасте 20–30 лет, течёт довольно медленно (10–15 лет и больше); дрожание резко преобладает, ригидность появляется лишь в конце болезни, иногда наблюдается гипотония мышц; отмечается амимия, медленная монотонная речь, тяжёлые изменения психики, часты аффективные вспышки, эпилептиформные припадки.
- Экстрапирамидно-корковая форма — встречается реже других форм. Типичные для гепатоцеребральной дистрофии нарушения в дальнейшем осложняются пирамидными парезами, эпилептиформными припадками и тяжёлым слабоумием (обнаруживаются обширные размягчения в коре больших полушарий). Длится 6–8 лет, заканчивается летально.
Клиническая картина БВК обширна, поражаются практически все органы и системы. Основными клиническими проявлениями считаются печеночные и неврологические. Они могут сочетаться с психическими, гематологическими, почечными, офтальмологическими (кольцо Кайзера-Флейшера), эндокринными, сердечно-сосудистыми, мышечно-скелетными, желудочно-кишечными (холелитиаз, панкреатит), дерматологическими (голубые лунки у ногтевого ложа, сосудистая пурпура) проявлениями. За свою многоликость болезнь Вильсона — Коновалова получила образное название «великого хамелеона» [6]. При своевременной максимально ранней диагностике и правильной терапии в 80 % случаев возможно купирование синдромов, улучшение прогноза заболевания.
Клинические проявления . Поскольку болезнь Вильсона — Коновалова является наследственным заболеванием, пациенты могут иметь положительный семейный анамнез. Описанный возраст начала болезни от 2 до 60 лет. Не менее чем четверти случаев заболевание не диагностируется, либо диагностируется недопустимо поздно. Суточное потребление меди с пищей составляет около 1 мг. Около 60 мг поглощенной меди (0,6 мг/день) абсорбируется в кишечнике. 0,35 мг меди в день выводится через кожу. 0,2 мг меди вдень экскретируется с желчью («регуляторная» медь). 0,05 мг меди в день выводится с мочой. Примерно у 30–50 % пациентов наблюдаются нервно-психические симптомы, включая асимметричный тремор. Другие симптомы могут включать слюнотечение, атаксию, изменения личности, маскообразные черты лица и неуклюжесть.
Целью настоящего исследования было получение новых знаний о роли поливалентных металлов в патогенезе когнитивных нарушений (памяти), а также поиск эффективных методов реабилитации (тета-ритм) или профилактики снижения когнитивных функций у лиц с орфанными заболеваниями.
Объект исследования — состояние когнитивного статуса (памяти), влияющее на качество жизни лиц с болезнью Вильсона — Коновалова.
Предмет исследования — аппаратный метод аудиостимуляции «ТЕТА-РИТМ», основанный на анализе лабораторных и визуализационных данных лиц с орфанными заболеваниями.
В качестве гипотезы выдвинуто предположение, что тета-ритм играет критически важную роль в процессах внимания и памяти, осуществляющихся с участием гиппокампа, а принцип действия устройства «ТЕТА-РИТМ», основанный на явлении синхронизации электрических потенциалов головного мозга с внешним стимулом (ритмичным звуком), будет являться эффективным методом нейрореабилитации и улучшения оптимального качества жизни лиц с орфанными заболеваниями. В соответствии с целью и гипотезой были поставлены сформулированы следующие задачи:
- Проанализировать и обобщить имеющиеся в научной литературе данные по проблеме влияния поливалентных металлов на патогенез когнитивных нарушений пациентов с избыточным накоплением меди и железа в головном мозге.
- Разработать диагностический блок для исследования нарушений памяти на основе жалоб пациентов с орфанными заболеваниями.
- Проанализировать результаты биохимических факторов, данных нейровизуализации, электроэнцефалограммы и вызванных когнитивных потенциалов лиц с болезнью Вильсона — Коновалова и болезнью Галлервордена — Шпатца.
- Провести под контролем невролога процедуры (в качестве ассистента) пациентам экспериментальной группы с применением аппарата «ТЕТА-РИТМ», относящегося к устройствам для неинвазивной аудиостимуляции структур гиппокампа.
- Оценить взаимосвязь между нарушением памяти и избыточным накоплением поливалентных металлов у лиц с орфанными заболеваниями с учётом возраста манифестации и длительности заболевания, гендерной принадлежности и тяжести заболевания.
- Разработать основные рекомендации по нейрокогнитивной реабилитации взрослых пациентов с избыточным накоплением поливалентных металлов спустя три месяца с начала реабилитации на фоне медикаментозного лечения.
В соответствии с поставленными задачами определены следующие методы исследования:
— теоретические;
— эмпирические (метод анкетирования, изучения медицинской документации, оценка биохимических и нейровизуализационных параметров, результатов нейрофизиологических исследований, динамическое наблюдение);
— математико-статистическая обработка полученных данных с использованием программного пакета «Статистика 12.0», а также аналитических возможностей программы Microsoft Office Excel.
Наше исследование предполагало четыре этапа работы, представленные на рисунке 2:

Рис. 2. Этапы проведения исследования
Базой экспериментального исследования являлось Федеральное государственное бюджетное научное учреждение «Российский центр неврологии и нейронаук» (ФГБНУ РЦНН): консультативно-диагностическое отделение Института клинической и профилактической неврологии, 5-е неврологическое отделение с молекулярно-генетической лабораторией. Период исследования: с 24 марта по 22 декабря 2025 года.
Критериями для постановки диагноза «болезнь Вильсона — Коновалова», согласно Лейпцигской количественной шкале (проводил невролог), служили:
— характерные для БВК нарушения обмена меди;
— изменения при МРТ головного мозга («мордочка гигантской панды» или «мордочка детеныша панды»), наличие роговичных колец Кайзера — Флейшера;
— подтвержденные результаты молекулярно-генетической диагностики (наличие мутаций в гене ATP7B).
Критериями для постановки диагноза «болезнь Галлервордена-Шпатца» (ННЖМ) (проводил невролог), служили:
— — МРТ головного мозга — основополагающий метод диагностики БГШ (овальная симметричная гиперинтенсивная зона в переднемедиальной части внутреннего сегмента бледного шара («зрачок») внутри более обширной гипоинтенсивной зоны —«глаз тигра»);
— данные неврологического статуса и электроэнцефалографии;
— консультация офтальмолога, визиометрия;
— определение типа наследования осуществляет генетик путем составления генеалогического древа.;
— молекулярно-генетический анализ гена PANK2;
— ДНК-диагностика — поиск мутаций в гене пантотенаткиназы.
Анализ научной литературы показал, что гепатолентикулярная дегенерация, известная как гепатоцеребральная дистрофия и болезнь Вильсона — Коновалова (БВК), является аутосомно-рецессивным наследственным заболеванием метаболизма меди с глобальной распространенностью около 1/100 000–3/100 000 [8]. По данным анализа Федерального регистра орфанных заболеваний, в России в 2014 и 2015 гг. было зарегистрировано всего 572 и 602 пациента с гепатолентикулярной дегенерацией, что составило 0,39 и 0,41 % на 100 000 населения соответственно (из них детей 16,9 %) [5].
На сегодняшний день существует крайне мало опубликованных рандомизированных контролируемых исследований по БВК и ННЖМ, что побуждает нас провести собственное исследование по определению роли поливалентных металлов в патогенезе когнитивных нарушений и влиянии тета-ритма в нейрореабилитации.
В основу исследования положен анализ собственных наблюдений и обследования пациентов под руководством опытных неврологов ФГБНУ «Российский центр неврологии и нейронаук» (ФГБНУ РЦНН). Объектом исследования стала группа из 26 пациентов: из них 24 — с БВК (12 мужчин, 12 женщин) в возрасте от 18 до 49 лет (средний возраст — 33,5±15,5 лет), средний возраст мужчин — 31±13 лет, средний возраст женщин — 34±15 лет, и 2 пациента с ННЖМ (1 мужчина и 1 женщина), средний возраст — 30±10 лет, находившихся на амбулаторном и стационарном лечении в поликлиническом отделении Института клинической и профилактической неврологии и 5-м неврологическом отделении с молекулярно-генетической лабораторией ФГБНУ НЦН с 24 марта по 22 декабря 2025 года. Все обследуемые подписали добровольное информированное согласие на проведение анкетирования и участие в исследовании.
Пациенты с ННЖМ были представлены двумя женщинами 25 и 55 лет. У пациентки 25 лет возраст дебюта заболевания составил 12 лет, длительность заболевания — 13 лет. Показатель MoCA как до лечения, также после курса аудиостимуляции составил 24 балла. У пациентки 55 лет заболевание дебютировало в 52 года, длительность заболевания — 3 года. Исходный уровень MoCA составил 23 балла, после курса — 24 балла, что отражает незначительную положительную динамику когнитивного профиля. С учётом крайне малой численности наблюдений (n = 2) проведение статистического анализа в данной подгруппе не проводился.
Распределение пациентов с БВК экспериментальной группы в зависимости от пола и возраста представлено на рисунке 3.
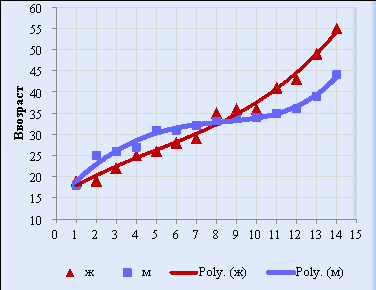
Рис. 3. Распределение пациентов с БВК экспериментальной группы в зависимости от пола и возраста
Среди пациентов с болезнью Вильсона — Коновалова в исследование вошли 14 мужчин и 12 женщин, что составило 53,8 % и 46,2 % соответственно. Возраст пациентов колебался от 18 до 49 лет, Me [Q1–Q3] — 33 [26–36] лет. Возраст дебюта заболевания варьировал от 7 до 29 лет, Me [Q1–Q3] — 20 [16–25] лет. Длительность заболевания составила от 1 до 26 лет, Me [Q1–Q3] — 13 [5–20] лет. На представленном ниже рисунке 4 показано распределение пациентов экспериментальной группы по месту проживания.

Рис. 4. Распределение пациентов экспериментальной группы по месту проживания
Как следует из рис. 4, в Москве проживали 12 (46 %) пациентов, что облегчало их анкетирование и возможность включения в исследование.
На рисунке 5 показана динамика восстановления памяти после курса стимуляции у пациентов в зависимости от гендерного признака.
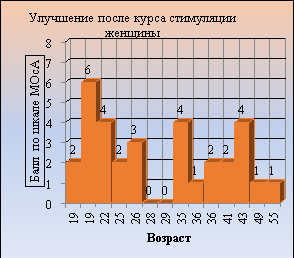
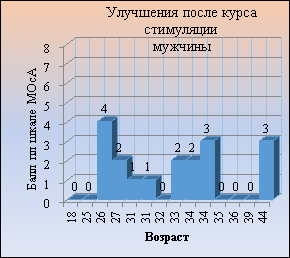
Рис. 5. Динамика восстановления памяти после курса стимуляции у пациентов в зависимости от гендерного признака
Исходный уровень когнитивного функционирования по Монреальской шкале оценки когнитивных функций (Montreal Cognitive Assessment — MoCA) варьировал от 13 до 28 баллов, Me [Q1–Q3] — 21 [20–25] баллов. Выявлена статистически значимая положительная связь между исходным уровнем MoCA и возрастом дебюта заболевания (r = 0,486; p = 0,012), что указывает на более высокие когнитивные показатели при более позднем начале заболевания. Связь между исходным уровнем MoCA и длительностью заболевания была статистически незначимой (r = 0,158; p = 0,441). После курса аудиостимулции значения MoCA составили от 15 до 29 баллов, Мe [Q1–Q3] — 24 [22–26] баллов (рисунок 6).
![Динамика показателей MoCA до и после курса стимуляции на аппарате аудиостимуляции Vibrostim™ модель «ТЕТА-РИТМ» у пациентов с БВК (Me [Q1–Q3]); различия статистически значимы по критерию Вилкоксона (p < 0,001)](https://articles-static-cdn.moluch.org/articles/y/5479/images/5479-7.png)
![Динамика показателей MoCA до и после курса стимуляции на аппарате аудиостимуляции Vibrostim™ модель «ТЕТА-РИТМ» у пациентов с БВК (Me [Q1–Q3]); различия статистически значимы по критерию Вилкоксона (p < 0,001)](https://articles-static-cdn.moluch.org/articles/y/5479/images/5479-8.png)
Рис. 6. Динамика показателей MoCA до и после курса стимуляции на аппарате аудиостимуляции Vibrostim™ модель «ТЕТА-РИТМ» у пациентов с БВК (Me [Q1–Q3]); различия статистически значимы по критерию Вилкоксона (p < 0,001)
Различия между показателями до и после курса стимуляции были статистически значимыми (p<0,001). При стратификации по полу статистически значимые различия сохранялись как у мужчин (p = 0,005), так и у женщин (p = 0,007).
Распределение пациентов с БВК в зависимости от манифестации и длительности заболевания представлено на рисунке 7.
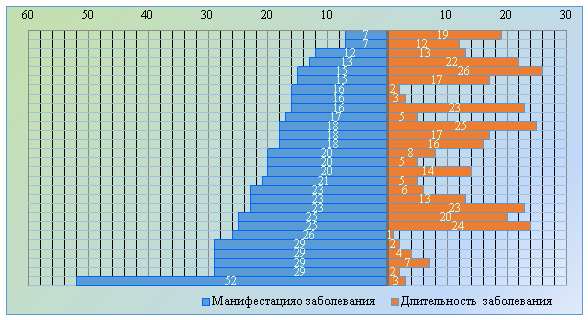
Рис. 7. Распределение пациентов экспериментальной группы в зависимости от манифестации и длительности заболевания
В настоящем исследовании мы стремились изучить особенности мнестических трудностей у лиц с болезнью Вильсона — Коновалова, уделяя особое внимание взаимосвязи между состоянием когнитивного статуса с учетом длительности заболевания. Мы рассматривали влияние тета-ритма на процесс восстановления памяти и оценивали когнитивный дефицит с помощью шкал и данных нейровизуализации, принимая во внимание показатели лабораторных анализов, результаты электроэнцефалограммы (ЭЭГ).
Клинический пример. Больная П. (правша, инвалид II группы, не работает, состоит в браке), находилась в 5 неврологическом отделении с молекулярно-генетической лабораторией ФГБНУ НЦН с диагнозом: Е83.0 — гепатолентикулярная дегенерация, (болезнь Вильсона — Коновалова), дрожательно-ригидная форма; фиброз печени. Предъявляла жалобы на нарушение речи (выраженное снижение звучности, разборчивости, невнятность), снижение памяти, поперхивание жидкой и твердой пищей, выраженное слюнотечение, дрожание правой руки, периодическое дрожание головы и туловища, насильственные движения и спазмы левой руки, изменение почерка, шаткость при ходьбе.Ввозрасте 4-х лет перенесла тяжелую черепно-мозговую травму (в результате ДТП) с развитием спастического левостороннего гемипареза. В дальнейшем развитие без особенностей. В июле 2001 г. (18 лет) появились жалобы на слабость в правых конечностях, нарушение глотания, скованность в ногах. Стаж курения: 28 лет, наследственность не отягощена.
Соматический статус : состояние удовлетворительное. Рост — 173 см, вес — 42 кг, ИМТ — 14 кг/м² (выраженный дефицит массы тела). АД — 125/70 мм.рт.ст., ЧСС — 72 уд/мин, ЧДД — 16/мин.
Неврологический статус: сознание ясное, контактна, ориентирована правильно. Менингиальных симтопомов нет, лицо симметрично, умеренная гипомимия. Слух (при ориентировочной оценке) сохранен. Дистония в левой кисти в виде тыльного переразгибания пальцев кисти и последующего сжатия в кулак, стриарная стопа слева. Походка на расширенной базе, с подволакиванием левой ноги и дистонией в левой руке в виде отведения в сторону сгибания кисти, ахейрокинез справа. При биомикроскопии отмечается наличие колец Кайзера-Флейшера. Оценка когнитивных функций по шкале МоСА отмечается 22/30 баллов. В ЭЭГ регистрируется сохранный корковый ритм, тета-ритм слабо выражен. Стол — 5а. На рисунке 8 изображено МРТ пациентки П.
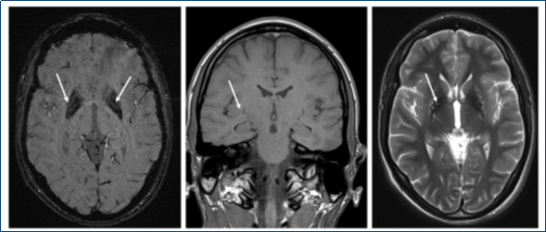
Рис. 8. МРТ пациентки П. Симметричное поражение бледных шаров (отложение меди), уменьшение в объеме лентикулярных ядер
Консультация психолога: пациентка доступна продуктивному контакту. Эйфорична, эмоциональный фон повышен. Уровень психической активности снижен: темп деятельности замедленный, мимика и жесты выразительны, голос громкий, маломодулированный. Во время обследования отмечаются импульсивность, повышенная утомляемость. Речь замедленна, артикуляция «смазанная». В пробе на слухоречевую память отмечается повышенное влияние гетерогенной и гомогенной интерференции, слабость слухоречевых следов при отсроченном воспроизведении, трудности непосредственного воспроизведения после гомогенной интерференции. Заключение: умеренное снижение слухоречевой памяти, умеренная динамическая апраксия, легкая оптико-пространственная агнозия, умеренные нейродинамические нарушения.
Алгоритм проведения процедуры представлен на рисунке 9.
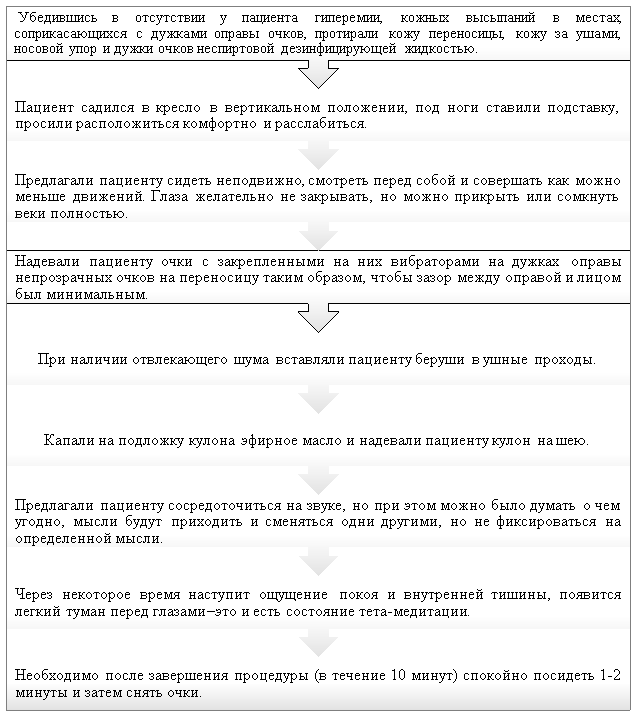
Рис. 9. Алгоритм проведения процедуры
Был проведен курс когнитивной и аппаратной реабилитации в два этапа (20 стационарных занятий и 10 амбулаторных занятий) по восстановлению нарушений памяти у пациентки с ГЛД на фоне медикаментозного лечения. Занятия в стационаре проводили в течение 10 минут 2 раза в день в хорошо проветриваемом помещении со звукоизоляцией. Побочных эффектов зафиксировано не было.
После курса аудиостимуляции больная отметила улучшение самочувствия, после 5-й процедуры со слов больной отпала необходимость запоминать тренировочные тексты с вечера, чтобы с утра их воспроизвести по памяти. Незначительно увеличился объем слухоречевой памяти, что подтверждалось при оценке MoCA до и после курса (22/26) стимуляции на аппарате аудиостимуляции Vibrostim™ — модель «ТЕТА-РИТМ» Также отмечена достоверная динамика показателей по данным клинических оценочных диагностических шкал, что доказывало положительное влияние проводимого неинвазивного воздействия.
Материалы и методы. На рисунке 10 представлена комплектация аппарата аудиостимуляции «ТЕТА-РИТМ», с помощью которого осуществляли стимуляцию пациентов в исследовании. Аппарат был разработан в научно-производственной лаборатории оборудования для нейрореабилитации ИП Лузгина С. А., инструмент для формирования вибрационных стимулов Vibrostim™ модель «ТЕТА-РИТМ». Аппарат «ТЕТА-РИТМ» относится к устройствам для неинвазивной аудиостимуляции структур гиппокампа и предназначен для стимуляции погружения в тета-медиативное состояние. Принцип действия устройства основан на явлении синхронизации электрических потенциалов головного мозга с внешним стимулом-ритмичным звуком. Прибор портативный, компактный и разработан так, чтобы его было очень легко использовать, он создан для того, чтобы сделать доступной методику стимуляции структур гиппокампа в повседневной жизни.

Рис. 10. Комплектация аппарата аудиостимуляции — инструмент для формирования вибрационных стимулов Vibrostim™ модель «ТЕТА-РИТМ»
Заключение
Наши результаты показали, что пациентам с когнитивными нарушениями нейродегенеративного генеза могут быть полезны процедуры с использованием аппаратной аудиостимуляции. При этом наблюдается незначительное улучшение рабочей памяти, концентрации внимания, психоэмоциональной динамики и активности в тета-диапазонах.
Наша гипотеза подтвердилась частично, так как не все пациенты продемонстрировали выраженную положительную динамику (ННЖМ) в восстановлении памяти на фоне проведения аудиостимуляции. Мы связываем это с характером нейродегенеративных заболеваний у пациентов с накоплением поливалентных металлов, ограниченным временем воздействия на гиппокамп и малым составом экспериментальной группы. Полученные нами первые результаты применения инновационного аппарата «ТЕТА-РИТМ», относящегося к устройствам для неинвазивной аудиостимуляции структур гиппокампа, являются мощным стимулом в сохранении здоровья человека и дальнейших научных исследований. предлагая базовый ориентир для начинающих исследователей.
Литература:
- Бердникович, А. М. Роль поливалентных металлов в патогенезе когнитивных нарушений / А. М. Бердникович, Т. Ю. Вяльцева. — Текст: непосредственный // Юный ученый. — 2026. — № 2 (98). — С. 92–103. — URL: https://moluch.ru/young/archive/98/5328.
- Болезни нервной системы. Руководство для врачей / Под ред. Н. Н. Яхно. — М.: Медицина, 2005. — Т. 2. — С. 170–171.
- Зуева И. Б., Ванаева К. И., Санец Е. Л. Когнитивный вызванный потенциал Р300: роль в оценке когнитивных функций у больных с артериальной гипертензией и ожирением // Бюл. СО РАМН. 2012. Т. 32, № 5. С. 55–62.
- Коновалов Н. В. Гепатоцеребральная дегенерация. — М., 1960. — 560 с.
- Красильникова, Е. Ю. Анализ ситуации в сфере оказания медицинской помощи и лекарственного обеспечения пациентов, страдающих редкими заболеваниями, в период 2013–2015 годов / Е. Ю. Красильникова, А. А. Соколов. — Текст: непосредственный // Проблемы стандартизации в здравоохранении. — 2016. — № 3–4.
- Надирова К. Г., Аринова А. А. Болезнь Вильсона. Современные аспекты. Анализ клинического опыта. — СПб., 2001. — 126 с.
- Экстрапирамидные расстройства. Руководство по диагностике и лечению. Под ред. Штока ВН, Ивановой-Смоленской ИА, Левина ОС. Москва: МЕДпресс-информ; 2002 С. 608.
- Cai, H. ATP7B gene therapy of autologous reprogrammed hepatocytes alleviates copper accumulation in a mouse model of Wilson’s disease / H. Cai, X. Cheng, X. P. Wang // Hepatology. — 2022. — № 76 (4). — P. 1046–1057. — DOI:10.1002/hep.32484.
- Gerosa C., Fanni D., Congiu T., Piras M., Cau F., Moi M., Faa G. Liver pathology in Wilson's disease: From copper overload to cirrhosis // Journal of inorganic biochemistry. 2019. V. 193. P. 106–111. https://doi.org/10.1016/j.jinorgbio.2019.01.008
- Medici V., Czlonkowska A., Litwin T., Giulivi C. Diagnosis of Wilson disease and its phenotypes by using artificial intelligence // Biomolecules. 2021. V. 11. № 8. P. 1243. https://doi.org/10.3390/biom11081243
- Takkar B., Temkar S., Venkatesh P. Wilson disease: Copper in the eye // The National medical journal of India. 2018. V. 31. № 2. P. 122–122. https://doi.org/10.4103/0970–258x.253156

