В настоящее время оксиды магния и кальция применяются в различных отраслях промышленности: металлургической, строительной, химической, шинной, электротехнической, теплотехнической, пищевой, а также в медицине. Смесь оксидов магния и кальция в определенных пропорциях – это полуфабрикат для производства магния. Одним из направлений создания новых теплоизоляционных и строительных материалов с повышенными показателями является применение при их изготовлении магнезиальных и доломитовых вяжущих материалов. Основными их достоинствами являются высокая механическая прочность, быстро нарастающая в начальный период твердения, повышенные показатели прочности при изгибе, плотная структура затвердевшего магнезиального камня. Для этих вяжущих характерна низкая теплопроводность, высокая прочность сцепления с заполнителями. Основной причиной, сдерживающей широкое применение магнезиальных и доломитовых вяжущих материалов в настоящее время, является недостаточный объем производства, в частности, каустического магнезита. Его получают обжигом магнезита, который является сырьем для получения более дорогого продукта – металлического магния. В металлургической промышленности используют также доломиты. При этом остаются некондиционные фракции, которые, как правило, попадают в отвал. Наиболее перспективным направлением является их применение для изготовления различных вяжущих материалов, что решит проблему комплексного использования доломитов.
Цель данной работы заключалась в изучении активности материала, полученного обжигом доломита. Этот материал, в зависимости от температуры обжига может быть перспективным сырьем для получения каустического доломита, доломитового цемента и доломитовой извести.
На территории Свердловской области имеются значительные разведанные доломитовые залежи с запасом сырья около 80 млн. тонн. В настоящей работе использованы доломиты Бойцовского месторождения.
Бойцовское месторождение приурочено к северо-западной краевой части Черемшанско-Цибихинской синклинали, входящей в состав Билимбаевского синклинория. Месторождение сложено карбонатными породами силурийского и девонского возраста, в геологическом строении принимают участие отложения среднего и верхнего отделов ордовикской системы, перекрытые рыхлыми отложениями мезокайнозойского возраста. Толща карбонатных пород верхнего ордовика, в которой размещены доломиты, залегает в виде субмеридиональной полосы. Балансовые запасы месторождения составляют 16 млн. тонн доломита.
В теоретическом составе доломита содержание основных компонентов составляет, в мас.%: MgO – 21,86; CaO – 30,41; СО2 – 47,73, а мольное соотношение MgO : СаО = 1:1.
В более ранних работах [1,2,3] исследован химический состав и другие свойства проб руды Бойцовского месторождения. Химический состав исследован методом эмиссионного спектрального анализа с индуктивно-связанной плазмой. Анализ проводился с помощью оптического эмиссионного спектрометра «iCAP 6300 Duo» фирмы «Thermo scientific» США (табл.1).
Таблица 1
Химический состав доломита Бойцовского месторождения
|
Содержание основных компонентов в пересчете на оксиды, % (по массе) | |||||||
|
MgО |
CaO |
Fe2O3 |
Al2O3 |
Na2Oк |
SiO2 |
П.П.П. |
Сумма |
|
20,39 |
31,06 |
0,08 |
0,03 |
0,02 |
0,004 |
48,05 |
99,63 |
Для исследования фазового состава, качественных характеристик образцов доломитовой руды был применен метод рентгенофазового анализа (табл.2). Рентгенофазовый анализ проводили на установке RIGAKU Dmax – 2200 в интервале углов 2θ = 22о – 75о при угловой скорости сканирования 1 град/мин. в CuKα – излучении (40 кВ, 30 мА; λ = 1,54056 Å). Полученные результаты использовались для автоматизированного поиска по базе данных JCPDS.
Таблица 2
Данные рентгенофазового анализа образца доломита
|
Угол - 2θ |
Относительная интенсивность пика, % |
MgCa(CO3)2 |
CaCO3 |
|
29,502 |
11 |
- |
-0,077 (100%) |
|
31,014 |
100 |
0,004 (100%) |
0,256 (2%) |
|
41,207 |
8 |
0,012 (19%) |
- |
|
45,016 |
5 |
0,013 (10%) |
- |
|
50,627 |
6 |
-0,021 (10%) |
- |
|
51,165 |
7 |
-0,017 (13%) |
- |
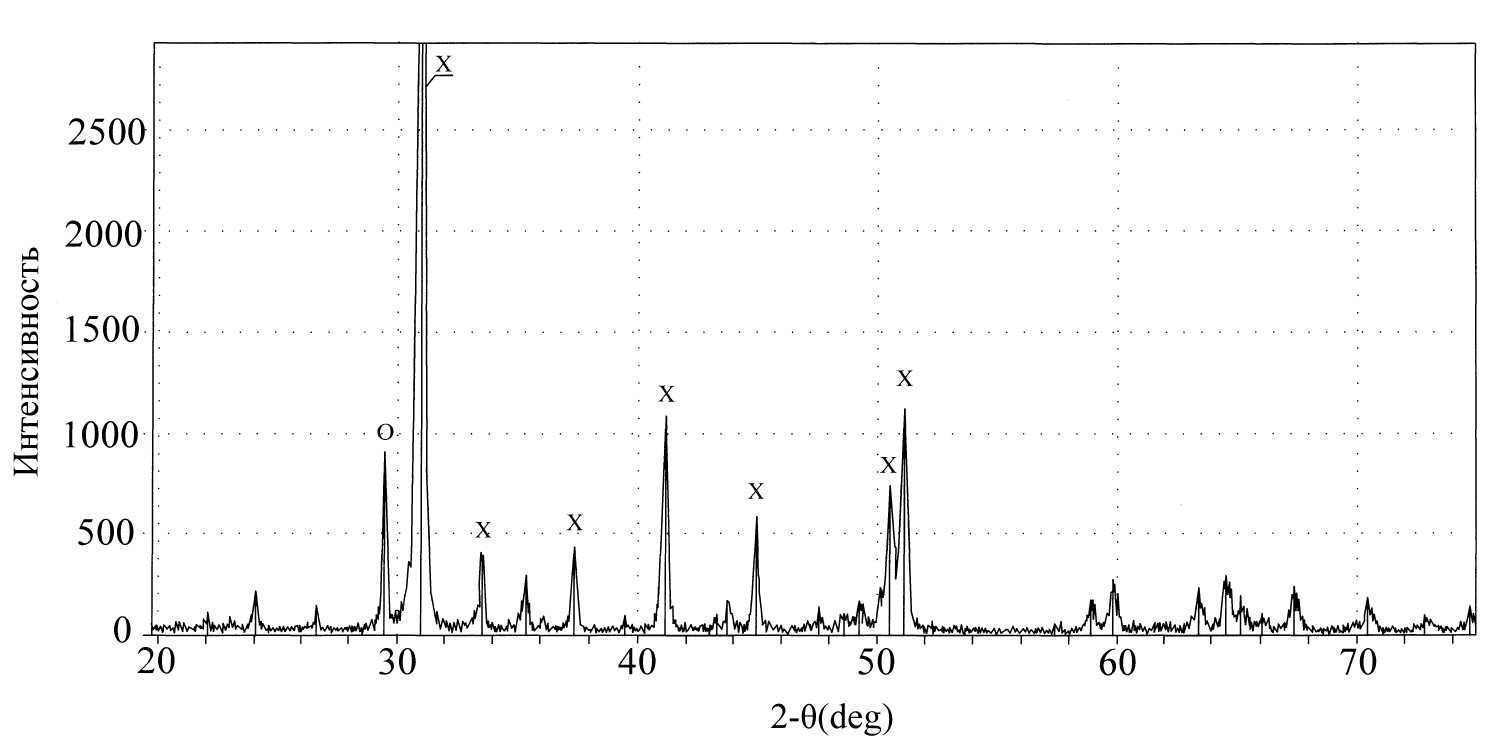
По данным рентгенофазового анализа образец руды Бойцовского месторождения состоит из смеси фаз: основная фаза со структурой доломита (максимальный пик при 2θ = 31,014о) и дополнительная фаза со структурой карбоната кальция (рис. 1). Используя, вышеприведенные данные химического состава руды определено процентное содержание свободного (не связанного с доломитом) карбоната кальция (CaCO3 = 4,9 %).
Рис.1 - Рентгенограмма образца доломита (Х – СаСО3•MgCO3, О - СаСО3)
Разложение карбонатов – сложное явление, отдельные стадии которого – диффузия, адсорбция и десорбция. Химические реакции, кристаллические превращения имеют различную природу. В соответствии с этим скорость разложения зависит от многих обстоятельств, в частности: от состава газовой фазы, скорости нагрева, размера кусков обжигаемого материала [4].
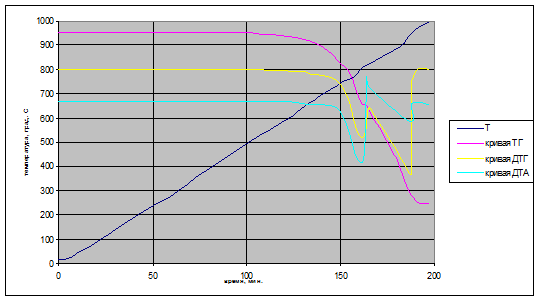
Исследование термических свойств доломитовой руды Бойцовского месторождения проведено методом термографии на дериватографе Q–1500D (рис.2). Опыт проводили в платиновом тигле на воздухе. Навеска составляла 804 мг, температура нагрева – 5 град/мин до 1000оС. Чувствительность ДТА устанавливалась максимальной.
Рис. 2 - Термограмма образца доломита Бойцовского месторождения
Согласно полученным результатам, разложение исследуемого доломита протекает в две стадии: на кривой ДТА видны два чётких эндотермических эффекта. На кривой ДТГ также присутствуют два пика. Температуры пиков на обеих кривых практически совпадают ( Т1=770оС и Т2 = 925оС). Температурный интервал протекания первой стадии диссоциации 743 – 800оС, второй - 887 – 943оС. На кривой ТГ имеются две ступеньки, отражающие убыль массы исходного вещества. Изменение массы исследуемого образца относительно начальной массы навески на первой стадии составляет 20,55 %, на второй – 26,6 %. Суммарная убыль массы образца – 47,15 %. На кривой ДТА между двумя эндотермическими пиками наблюдается экзотермический тепловой эффект, который может быть связан с кристаллизацией аморфного продукта разложения, образовавшегося после первой стадии процесса. На кривых ДТА и ДТГ, полученных при охлаждении, тепловые эффекты отсутствуют, масса образца не меняется. Изменение массы, определенное взвешиванием тигля с пробой до и после опыта (Δm=388 мг.) несколько меньше, чем рассчитанное из кривой ТГ (Δm=397 мг.), поскольку при охлаждении вещество, по-видимому, поглощает из атмосферы пары воды и/или СО2.
Про продукты обжига и спекания доломита известно следующее. В процессе обжига при температуре около 750оС образуется каустический доломит, который состоит в основном из CaCO3 и MgО (не менее15%). При более высоких температурах могут быть получены доломитовый цемент и доломитовая известь. Доломитовый цемент, в состав которого входят MgО, CaO и CaCO3, получают при температуре обжига 800–850оС; доломитовая известь (смесь из MgО и CaO) образуется при температуре обжига 900–1000оС. Более высокие температуры приводят к спеканию доломита и образованию доломитовых огнеупоров.
Известно, что механизм обжига, а затем и спекания известняка, доломитов заключается в том, что мелкие кристаллические зерна под влиянием сил молекулярного сцепления срастаются в кристаллическое тело, при этом часть пор закрываются, далее наблюдается рекристаллизация (рост кристаллов). При спекании параллельно с рекристаллизацией наблюдается процесс «заживления» кристаллов, имеющих искажения в первоначальной кристаллической структуре, который сопровождается понижением активности вещества. Наглядное представление об этом дают результаты определения температурной зависимости истинной и кажущейся плотности оксида кальция. Оксид кальция, полученный при низких температурах обжига, имел пониженную плотность и максимальную пористость. Время гашения его водой, характеризующее реакционную способность измеряется до температуры 800оС секундами. Такая высокая активность определяется наличием большого числа дефектов строения и высокой дисперсностью кристаллов. В интервале с 950-1200оС происходит уплотнение, уменьшается пористость, увеличивается размер зерна. При температуре прокаливания 1200-1400оС наблюдается рекристаллизация, при этом реакционная активность оксида кальция снижается. Таким образом, известь, полученная путем обжига известняка при различных температурах и времени обжига, обладает неодинаковой реакционной способностью. Реакционную активность определяют по времени достижения максимальной температуры при взаимодействии обожженного CaO с водой [5].
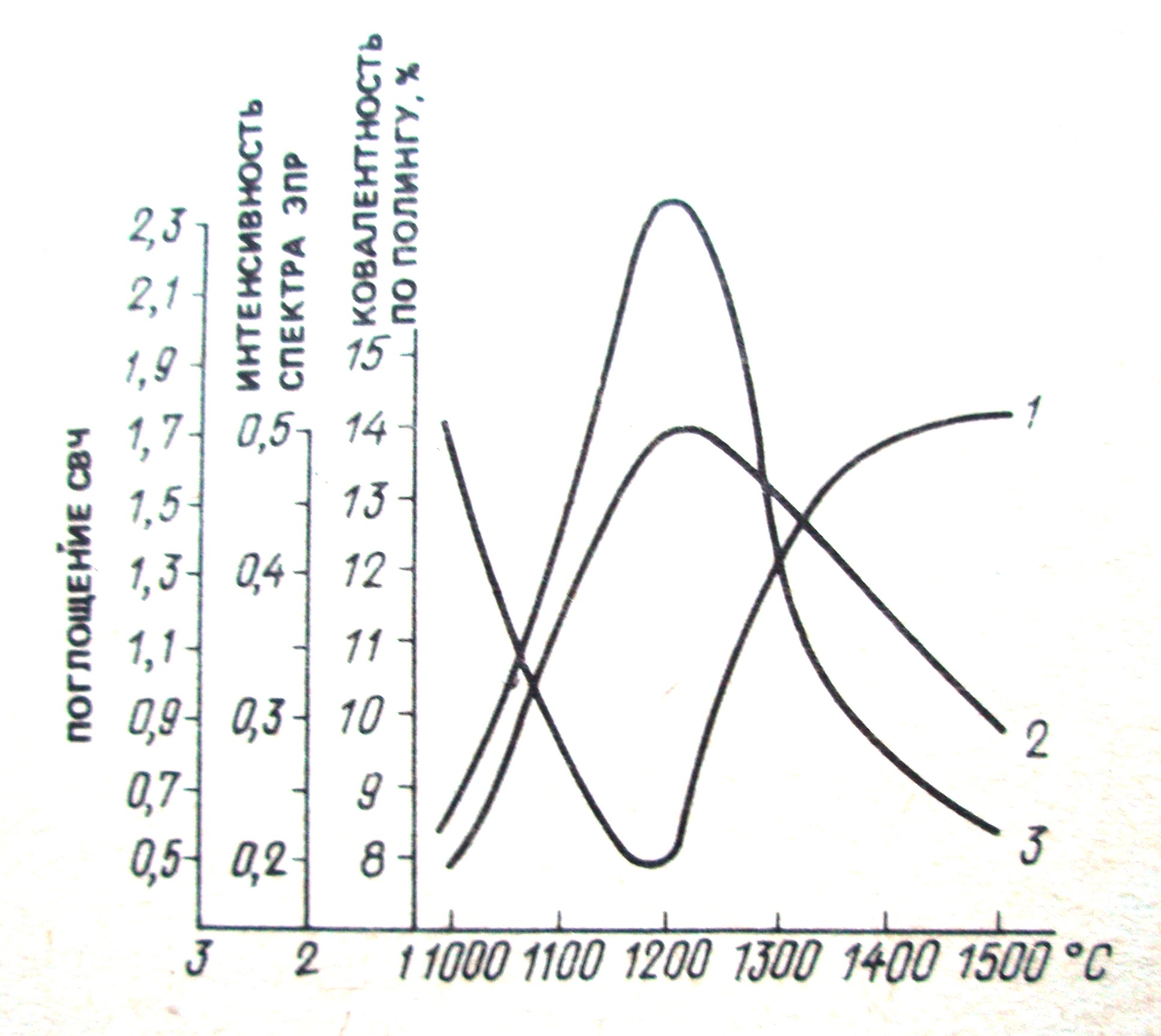
С другой стороны, изменение свойств оксида кальция при нагревании известняка связано с изменением химического потенциала, зависящего от энергии кристаллической решетки этого соединения с характером связи, не отвечающей идеальному ионному распределению зарядов Са2+ и О2- (ковалентность составляет 10% по по Л. Полингу на одну связь Са-О). При нагревании доля ионной связи в решетке СаО растет и достигает максимума при 12000С. Эти данные были получены при помощи метода электронного парамагнитного резонанса (ЭПР) и представлены на рис.3. В химически чистых совершенных кристаллах не может наблюдаться парамагнитного резонанса, так как все электронные оболочки заполнены (неспаренные электроны отсутствуют). Однако наличие дефектов или примесей может привести к появлению нескомпенсированных электронов. Анализ спектров ЭПР позволяет сделать некоторые выводы об энергетическом состоянии дефектов, ионов основной решетки и характере химической связи в исследуемом материале. Следует ожидать, что энергия решетки СаО при этой температуре максимальна, как и её химический потенциал. Это определяет максимальную реакционность способность извести, полученной обжигом в течение 1 ч при данных условиях обжига [6]. Аналогичная картина наблюдается и при прокаливании доломита.
Рис.3 – Изменение свойств оксида кальция при нагревании (по данным ЭПР)
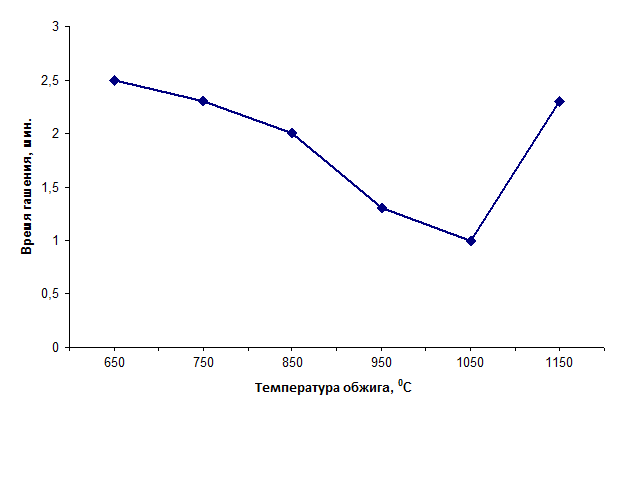
При проведении эксперимента доломит обжигался в печи с одинаковым временем выдержки при заданной температуре. В соответствие с ГОСТ 22688-77 «Известь строительная. Методы испытаний», было проведено исследование зависимости времени гашения доломитовых материалов: магнезиальной извести, доломитового цемента, доломитовой извести от температуры обжига доломита. Испытания проводились в воздушном калориметре. Результаты представлены на рис.4.
Рис. 4 – Зависимость времени гашения доломитовых материалов от температуры обжига доломита
Анализ полученных данных позволяет сделать вывод о том, что из всех доломитовых вяжущих максимальной активностью обладает доломитовая известь, которая получается при температуре обжига доломита около 1050ºС. Время гашения доломитовой извести, которое характеризует её реакционную способность, измеряется секундами. Полученные данные хорошо согласуется c исследованиями процесса обжига известняка и доломитов других месторождений. Наличие оксида магния несколько снижает температуру достижения максимального уровня энергии кристаллической решеткой СаО, и дальнейшее повышение температуры не вызывает увеличения активности извести.
Выводы:
1. Исследования состава доломита, которые были проведены различными методами: эмиссионным спектральным анализом с индуктивно-связанной плазмой и рентгенофазовым анализом показали, что доломитовая руда Бойцовского месторождения содержит минимальное количество примесей, достаточное содержание магния и может быть использована в качестве сырья в производстве магния. Некондиционные фракции пригодны для изготовления доломитовых вяжущих.
2. В результате термографического анализа были определены температурные интервалы двух стадий диссоциации доломита, а также температуры, при которых скорость диссоциации максимальна.
3. Изучено влияние температуры обжига доломита на активность доломитовых материалов. Установлено что доломит пригоден для производства доломитовых вяжущих: каустического доломита, доломитового цемента и доломитовой извести.
-
- Литература:
- О сырьевых источниках силикотермического производства магния / М.В. Белоусов, Ракипов Д.Ф. Современные техника и технологии: сборник трудов XVI международной научно-практической конференции студентов, аспирантов и молодых ученых. В 3 т. Т. 2 / Национально-исследовательский Томский политехнический университет. – Томск: Изд-во Томского политехнического университета, 2010. – С. 101-104.
- Исследование механизма диссоциации доломита методом дериватографии/ Белоусов М.В., Муллагулов М.Ф., Ракипов Д.Ф. Наука и молодежь: проблемы, поиски, решения: Труды Всероссийской научной конференции студентов, аспирантов и молодых ученых / Под общей редакцией Л.П. Мышляева; СибГИУ. – Новокузнецк, 2010. – Вып. 14. – Ч. III. Технические науки. – С. 112-115.
- О возможности использования доломитов Среднего Урала в производстве MgО и CaO / Белоусов М.В., Колесникова М.П., Никоненко Е.А. Новые химические технологии: производство и применение: Сборник статей ХII Всероссийской научно-технической конференции. – Пенза: Приволжский Дом знаний, 2010. – С. 8-10.
- Стрелец Х.Л., Тайц А.Ю., Гуляницкий Б.С. Металлургия магния. М.: Металлургиздат. 1960. 480 с.
5. Табунщиков, Н.П. Производство извести /Н.П. Табунщиков. – М.: Изд-во «Химия», 1974. 240с.
6. Мчелов-Петросян, О.П. Химия неорганических строительных материалов/ М.: Стройиздат, 1988. 304 с.