Профиль жирных кислот интактных и пораженных атеросклерозом артерий эластического типа
Авторы: Осипенко Александр Николаевич, Акулич Николай Васильевич, Бирюков Андрей Евгеньевич
Рубрика: 3. Медико-биологические дисциплины
Опубликовано в
международная научная конференция «Новые задачи современной медицины» (Пермь, январь 2012)
Статья просмотрена: 234 раза
Библиографическое описание:
Осипенко, А. Н. Профиль жирных кислот интактных и пораженных атеросклерозом артерий эластического типа / А. Н. Осипенко, Н. В. Акулич, А. Е. Бирюков. — Текст : непосредственный // Новые задачи современной медицины : материалы I Междунар. науч. конф. (г. Пермь, январь 2012 г.). — Пермь : Меркурий, 2012. — С. 32-34. — URL: https://moluch.ru/conf/med/archive/51/1477/ (дата обращения: 25.04.2024).
Введение. Длительное время существует значительный интерес к проблеме накопления липидов в артериальной стенке при атеросклерозе. Тем не менее, остаются неясными некоторые аспекты, касающиеся как механизмов атеросклеротического поражения артериальных сосудов, так и причин возникновения дислипидемий. Дополнительных исследований требует и вопрос, касающийся роли отдельных жирных кислот (ЖК), в том числе и полиненасыщенных (ПНЖК), в атерогенезе.
Показано, что холестерин (ХС), в том числе в форме соединений с ЖК, является преобладающим липидом в атеросклеротических бляшках [3, 5]. Считается, что он практически полностью поступает из кровотока в составе липопротеинов, а не образуется за счет локального синтеза [5]. Однако, изучение липидов в бляшках и липидных пятнах показало, что в бляшках содержится больше свободного ХС по отношению к эфирам холестерина (ЭХС). Этот факт входит в противоречие с концепцией о происхождении липидов атеромы из плазмы крови, так как наибольшая доля холестерина плазмы представлена ЭХС [5]. Остается неясным механизм проникновения липидов через фиброзную покрышку бляшки. Непонятно и то, почему липиды крови поступают именно в атерому, и вместе с тем имеются в незначительном количестве в неизменной интиме, прилежащей к бляшке. По одной из версий, рост бляшки происходит из-за накопления липидов, поступающих из прорастающих в нее сосудов. По другой – количество сосудов не столь велико, чтобы обусловить обильное накопление липидов [2]. Было показано, что клетки артерий синтезируют ЖК de novo, причем в атеросклеротических артериях синтезируется большее количество ЖК, чем в интактных [6].
Таким образом, несмотря на то, что изучению атеросклероза посвящены многочисленные публикации [2, 3, 5], до настоящего времени существует много вопросов, касающихся различных этапов атерогенеза, и требующих дальнейшего исследования участников этого процесса. Кроме того, современные данные о метаболизме фиброзной бляшки все еще недостаточны.
Целью работы: анализ баланса жирных кислот, фрагментов интактных сосудов и сосудов с признаками атеросклероза.
Методы и материалы. Объектом исследования явились фрагменты брюшной аорты и общей сонной артерии (2-3г.) из 9 тел мужчин (возраст 50±6,7 лет). Выбор объектов исследования связан с тем, что в стенке брюшной аорты наиболее часто локализуются атеросклеротические бляшки, а общая сонная артерия обладает резистентностью в плане образования атером.
Кроме этого, с поверхности каждой аорты делался соскоб люминальной поверхности сосуда (эндотелий и подэндотелиальный слой), а в пластиковую пробирку с антикоагулянтом (гепарин – 10 Ед/мл) отбиралось 3-4 мл крови.
Образцы сонной артерии не имели атероматозных изменений, а все образцы аорты имели атеросклеротические повреждения различной степени. Шесть из них – 4 тип (контроль), три – 5-6 тип (опытная группа). Оценка атеросклеротических поражений проводилась по классификации Х.К. Стэри [3].
Учитывая, что у крыс не удается получить адекватную модель атеросклероза, включая в их рацион избыток ХС, мы изучили состав ЖК в брюшной аорте у 4 животных.
Производные ЖК (из эфиров холестерина и глицерина с жирными кислотами) миоцитов сосудов получали после извлечения липидов этанолом из гомогенизированных образцов. Далее использовали кислотный этанолиз и экстракцию этиловых эфиров ЖК гексаном. Этанолизу также подвергались липиды соскобов эндотелия (эндотелий и подэндотелиальный слой) и плазмы крови. Затем проводился газохроматографический анализ состава ЖК. При этом разделение этиловых эфиров жирных кислот осуществлялось на капиллярной колонке с неполярной фазой SE-30 (газ-носитель – азот).
Количественная оценка содержания отдельных ЖК производилась в процентном отношении к их общей сумме. Измерения проводились на газовом хроматографе «ГХ–1000» (РФ) с пламенно-ионизационным детектором. Для идентификации окисленных активными формами кислорода жирных радикалов использовался метод вычитания, когда пики на хроматограмме, соответствующие кето-, эпокси- и гидропероксипроизводным, исчезали. Для этого к экстрактам добавляли борогидрид натрия. Количественная оценка содержания этих соединений производилась в процентном отношении к сумме неокисленных ЖК. Окончательная идентификация осуществлялась с помощью хромато-масс-спектрометра «Finnigan DSQ II» (США).
Статистический анализ проводился с использованием U-критерия Манна-Уитни, который позволяет оперировать выборками с небольшим количеством наблюдений. Изменения считались значимыми при p<0,05.
Результаты и их обсуждение. Анализ состава ЖК сонных артерий и брюшных аорт показал, что относительное содержание арахидоновой ПНЖК в стенках a. carotis communis достоверно ниже (0,37±0,17%), чем в соответствующих им по телам фрагментах брюшных аорт (0,84±0,31%) независимо от степени их поражения. Ее уровень в аортах с развитым атеросклерозом имеет тенденцию к увеличению в сравнении с аортами без серьезных дефектов (табл.). Таким образом, повышение склонных к перекисному окислению ПНЖК в сосудах с атероматозом может указывать на их более высокую восприимчивость к окислительной деградации.
Фрагменты аорт опытной группы также характеризовались низким относительным уровнем насыщенной пальмитиновой ЖК. Кроме того, в сонных артериях тех же тел уровень пальмитиновой кислоты также ниже (несмотря на отсутствие признаков атерогенеза), чем в сонных артериях группы контроля. Уровни мононенасыщенных ЖК – пальмитолеиновой и миристолеиновой в обоих случаях, наоборот, были выше (табл.).
Таблица
Состав жирных кислот брюшной аорты и общей сонной артерии
|
|
Контроль, % |
Опыт, % |
||
|
Жирные кислоты |
Сонная артерия |
Брюшная аорта |
Сонная артерия |
Брюшная аорта |
|
лауриновая |
0,34±0,14 |
0,39±0,28 |
0,36±0,08 |
0,55±0,14 |
|
миристолеиновая |
0,19±0,05 |
0,19±0,07 |
0,33±0,06* |
0,46±0,07* |
|
миристиновая |
2,72±0,53 |
2,83±0,81 |
2,85±0,57 |
3,70±0,46* |
|
пальмитолеиновая |
5,75±1,36 |
5,34±1,25 |
7,92±0,81* |
9,40±2,57* |
|
пальмитиновая |
26,55±2,11 |
27,41±2,49 |
22,40±2,35* |
23,29±2,48* |
|
линолевая |
10,27±3,75 |
10,22±1,86 |
11,44±4,52 |
12,27±4,14 |
|
олеиновая |
42,82±2,05 |
40,55±5,04 |
44,04±0,64 |
40,34±0,43 |
|
стеариновая |
6,89±1,14 |
7,96±2,17 |
5,31±0,62* |
4,76±1,78* |
|
арахидоновая |
0,24±0,19 |
0,73±0,54 |
0,63±0,28 |
1,07±0,52 |
|
арахиновая |
0,89±0,30 |
0,94±0,36 |
0,73±0,04 |
0,58±0,09* |
|
докозагексаеновая |
0,19±0,18 |
0,29±0,25 |
0,32±0,20 |
0,24±0,02 |
Примечание: различия достоверны * – p < 0,05
Образование мононенасыщенных кислот из насыщенных катализируется 9-десатуразой, участвующей в регуляции ответа на изменение условий среды путем поддержания текучести клеточных мембран. Показано, что наличие в пище достаточного количества ПНЖК подавляет экспрессию 9-десатуразы. С другой стороны, известно, что ЖК синтезируются при помощи синтазы жирных кислот, приводящей к образованию пальмитиновой кислоты. При ее нормальной активности значительная часть пальмитиновой ЖК превращается в стеариновую и арахиновую. При гиперэкспрессии фермента повышается содержание пальмитиновой кислоты относительно стеариновой. Показано, что этот процесс всегда сопутствует активной пролиферации опухолевых клеток, а ингибирование синтазы жирных кислот (например, введением ПНЖК) приводит к ее остановке [1]. Свидетельством повышенной активности синтазы ЖК клеток бляшки при осложненном атеросклерозе может являться тот факт, что в аортах при осложненном атеросклерозе уровень пальмитиновой кислоты снижен на 15,03% (p<0,05) в сравнении с контролем, а уровень стеариновой и арахиновой на 40,20% и 38,30% (p<0,05), соответственно. В сонных артериях уровень пальмитиновой, стеариновой и арахиновой кислот был снижен практически на одну величину относительно контроля. В отличие от других насыщенных ЖК уровень миристиновой кислоты в аортах опытной группы не снижается, а наоборот имеет тенденцию к росту (p=0,12) (табл.). Это может быть связано с тем, что миристиновая ЖК в основном включается в клеточные триглицериды [1] а, следовательно, отражает увеличение их содержания.
Учитывая вышесказанное, можно предположить, что выявленный нами ранее выраженный дефицит линолевой ПНЖК в плазме крови при атеросклерозе [4] может служить фактором, который на фоне высокой активности синтазы ЖК стимулирует экспрессию десатураз в гладкомышечных клетках (ГМК), что, в конечном итоге, способствует пролиферации миоцитов.
Спектр жирных кислот брюшных аорт крыс имеет существенные отличия от соответствующего спектра у человека. В основном это касается относительного уровня мононенасыщенных ЖК. Так, относительный уровень олеиновой кислоты составляет всего 32,90±1,81%. Кроме того, в брюшных аортах крыс в сравнении с брюшной аортой человека повышен (34,09±2,79%) уровень насыщенной пальмитиновой ЖК.
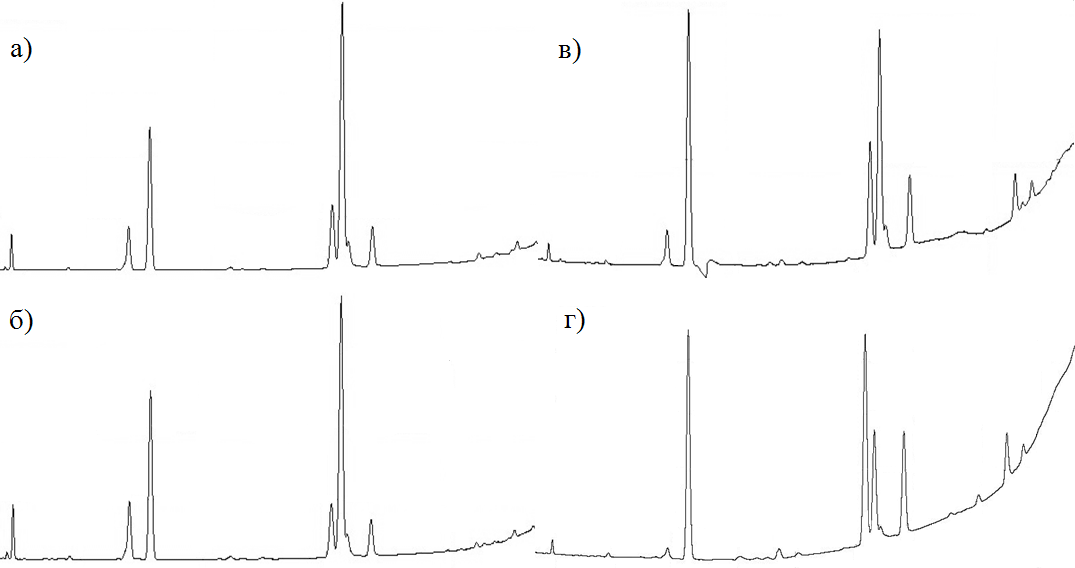
Следует отметить, что баланс ЖК в крупных атеросклеротических бляшках в значительной мере сходен с соотношением жирных кислот в тех же сосудах, но с нормальной консистенцией (рис.), и значительно отличается от спектра ЖК плазмы крови (особенно здоровых людей). Это, с одной стороны, указывает на наличие достаточно активного метаболизма клеточных элементов бляшки, направленного на поддержание гомеостазиса, а с другой – на тот факт, что основная часть жирных кислот бляшки образована в результате ферментативных процессов, протекающих в ГМК, а не в результате накопления поступивших из кровотока липидов.
Профиль жирных кислот материала, взятого при соскобе с поверхности аорты, с одной стороны, напоминал профиль ЖК плазмы крови, а с другой – состав, присущий миоцитам. Cоскобы эндотелия с поверхности сосудов с далеко зашедшим атеросклерозом имели тенденцию (p=0,10) к более высоким уровням окисленных производных жирных радикалов (1,86% против 0,53%).
Рис. Спектр жирных кислот: (a) – части брюшной аорты с нормальной консистенцией, (б) – атеросклеротической бляшки, (в) – плазмы крови с того же тела, (г) – плазмы крови здорового человека.
Выводы:
Нарушение обмена жирных кислот в гладкомышечных клетках может являться одним из триггеров атерогенеза.
Жирные кислоты в липидах атеросклеротической бляшки образованы в результате синтетических процессов, протекающих в ее клетках.
Литература:
Акимов М.Г., Безуглов В.В., Бобров М.Ю. и др. Липиды и рак. Очерки липидологии онкологического процесса. – СПб., 2009.
Бодрова О.В. Атеросклероз. – М., 2000.
Зайчик А.Ш., Чурилов Л.П. Основы общей патологии. Часть 2. Основы патохимии. – СПб., 2000.
Осипенко А.Н., Акулич Н.В., Марочков А.В., Орлов Д.А. // Молодежь в науке – 2009: прил. к журн. «Вести Национальной академии наук Беларуси». В 5 ч. Ч. 4. – 2010. – С. 414–419.
- Adams C.W. // J. Clin Pathol (Suppl). – 1973. – Vol. 26. – P. 38 – 42.
- Clair R.W, Lofland H.B., Clarkson T.B. // J. Lipid Res. – 1968. – Vol. 9. – P. 739-747.
Похожие статьи
Осложнения аневризмы аорты при атеросклерозе и синдроме...
При исследовании дуги аорты умершего мужчины в возрасте 55 лет, на уровне отхождения от нее левой общей сонной артерии в стенке аорты имеется дефект с ровными краями 1,5 см в диаметре.
Диагностика нарушения липидного обмена у пациентов...
плазма крови, кислота, относительный уровень, недостаточность, уровень, жирная кислота плазмы крови, высокое содержание, интенсивная терапия, липидный обмен, липидный состав.
Состояние эндотелия сонных артерий при артериальной...
При АГ имеет место ремоделирование сосудов головного мозга, которое выражается в первую очередь в увеличении диаметра общей сонной и внутренней сонной артерий в сравнении с контрольной группой, толщины ТИМ сонных артерий, зависящие от степени повышения АД...
Изучение показателей состояния сонных артерий и скорости...
Изучены показатели состояния сонных артерий и скорости кровотока больных артериальной гипертензией и сахарным диабетом.
Увеличение толщины комплекса интимы-медиа общей сонной артерии также сопровождалось увеличением диаметра сосуда.
Вариантная анатомия чревного ствола и печеночной артерии
Под нормальной (типичной) анатомией чревного ствола понимают его отхождение от брюшной аорты и деление на 3 ветви: левую желудочную, общую печеночную и селезеночную артерии [4].
Управляемая гемодилюция как кровосберегающий метод...
Известно, что реконструктивные вмешательства на брюшной аорте сопряжены с риском
Одной из основных причин летальных исходов в хирургии магистральных артерий — таких как аорта и ее
Для интраоперационного резервирования крови отбирались больные с уровнем...
Анатомические и ультразвуковые параллели в диагностике...
Для больных ИБС, атеросклерозом периферических и сонных артерий, аневризмой брюшного отдела аорты, а также у пациентов сахарным диабетом содержание общего холестерина не должно превышать 4,5 ммоль/л, а ЛПНП -2,5 ммоль/л.
Топографическая анатомия подвздошно-поясничных артерий
При исследовании дуги аорты умершего мужчины в возрасте 55 лет, на уровне отхождения от нее левой общей сонной артерии в стенке аорты имеется дефект с ровными... Анатомические и ультразвуковые параллели в диагностике...
Исследование факторов, влияющих на стабильность...
Состав жирных кислот брюшной аорты и общей сонной артерии.
Смесь жирных кислот с кислотным числом 200...210 мг КОН включает лауриновую (0,43 %), миристиновую (16,7 %), пальмитиновую (55,3.
Похожие статьи
Осложнения аневризмы аорты при атеросклерозе и синдроме...
При исследовании дуги аорты умершего мужчины в возрасте 55 лет, на уровне отхождения от нее левой общей сонной артерии в стенке аорты имеется дефект с ровными краями 1,5 см в диаметре.
Диагностика нарушения липидного обмена у пациентов...
плазма крови, кислота, относительный уровень, недостаточность, уровень, жирная кислота плазмы крови, высокое содержание, интенсивная терапия, липидный обмен, липидный состав.
Состояние эндотелия сонных артерий при артериальной...
При АГ имеет место ремоделирование сосудов головного мозга, которое выражается в первую очередь в увеличении диаметра общей сонной и внутренней сонной артерий в сравнении с контрольной группой, толщины ТИМ сонных артерий, зависящие от степени повышения АД...
Изучение показателей состояния сонных артерий и скорости...
Изучены показатели состояния сонных артерий и скорости кровотока больных артериальной гипертензией и сахарным диабетом.
Увеличение толщины комплекса интимы-медиа общей сонной артерии также сопровождалось увеличением диаметра сосуда.
Вариантная анатомия чревного ствола и печеночной артерии
Под нормальной (типичной) анатомией чревного ствола понимают его отхождение от брюшной аорты и деление на 3 ветви: левую желудочную, общую печеночную и селезеночную артерии [4].
Управляемая гемодилюция как кровосберегающий метод...
Известно, что реконструктивные вмешательства на брюшной аорте сопряжены с риском
Одной из основных причин летальных исходов в хирургии магистральных артерий — таких как аорта и ее
Для интраоперационного резервирования крови отбирались больные с уровнем...
Анатомические и ультразвуковые параллели в диагностике...
Для больных ИБС, атеросклерозом периферических и сонных артерий, аневризмой брюшного отдела аорты, а также у пациентов сахарным диабетом содержание общего холестерина не должно превышать 4,5 ммоль/л, а ЛПНП -2,5 ммоль/л.
Топографическая анатомия подвздошно-поясничных артерий
При исследовании дуги аорты умершего мужчины в возрасте 55 лет, на уровне отхождения от нее левой общей сонной артерии в стенке аорты имеется дефект с ровными... Анатомические и ультразвуковые параллели в диагностике...
Исследование факторов, влияющих на стабильность...
Состав жирных кислот брюшной аорты и общей сонной артерии.
Смесь жирных кислот с кислотным числом 200...210 мг КОН включает лауриновую (0,43 %), миристиновую (16,7 %), пальмитиновую (55,3.