Особенности клинической картины, современных аспектов диагностики и лечения синдрома такоцубо (стрессовой кардиомиопатии)
Авторы: Панагов Залим Григорьевич, Шериева Альбина Юрьевна, Гудиева Илона Раульевна
Рубрика: 6. Клиническая медицина
Опубликовано в
V международная научная конференция «Медицина: вызовы сегодняшнего дня» (Санкт-Петербург, июль 2018)
Дата публикации: 06.06.2018
Статья просмотрена: 4852 раза
Библиографическое описание:
Панагов, З. Г. Особенности клинической картины, современных аспектов диагностики и лечения синдрома такоцубо (стрессовой кардиомиопатии) / З. Г. Панагов, А. Ю. Шериева, И. Р. Гудиева. — Текст : непосредственный // Медицина: вызовы сегодняшнего дня : материалы V Междунар. науч. конф. (г. Санкт-Петербург, июль 2018 г.). — Санкт-Петербург : Свое издательство, 2018. — С. 5-18. — URL: https://moluch.ru/conf/med/archive/304/14362/ (дата обращения: 25.04.2024).
В 1990 г. японский кардиолог Sato H. и соавт. обнаружили, что у 22 пожилых женщин с, казалось бы, тяжёлой картиной острого коронарного синдрома (ОКС), по данным коронарографии не выявляется столь тяжёлых поражений. Более того, выраженное снижение функции левого желудочка, которое отмечалось в момент госпитализации, нивелировало и состояние больных восстанавливалось быстрее, чем при ОКС. Стало понятно, что речь идёт о ранее не изученном заболевании и в МКБ-10 появилась новая нозологическая форма — синдром такоцубо. В статье описана типичная клиническая картина данного синдрома, приведены наиболее современные диагностические критерии и методы лечения.
Ключевые слова: острый коронарный синдром, такоцубо, синдром «разбитого сердца», коронарография, кардиомиопатия.
Синдром такоцубо — транзиторное баллоноподобное расширение средней части верхушки сердца, сопровождающееся одновременной гиперкинезией базальных сегментов левого желудочка при отсутствии гемодинамически значимого стеноза венечных артерий (I51.81) [1].
Другие названия синдрома: стрессовая кардиомиопатия, кардиомиопатия такоцубо, синдром апикального баллонирования, «синдром разбитого сердца», «синдром счастливого сердца».
Своим названием синдром обязан характерным изменением формы левого желудочка на эхокардиографии, возникающим за счёт акинезии/дискинезии и напоминающим японский глиняный сосуд — такоцубо, представляющий собой ловушку для осьминогов («тако» — осьминог, «цубо» — чаша). Ловушка-такоцубо — это 15-сантиметровый сосуд, который используется японскими рыбаками для ловли осьминогов на дне моря, в который они забираются как в жилище и оставляют снаружи только щупальца. Через некоторое время рыбаки вытаскивают ловушки за привязанную к ним верёвку вместе с осьминогами. Интересен тот факт, что приспособление такоцубо используется только рыбаками Хиросимы.
Эпидемиология. Таким образом, синдром впервые описан в Японии в 1990 г. В США первый случай описан в 1998 г. Sharkey S. W. и соавт. Вскоре после первого описания стало очевидным, что заболевание встречается в разных регионах мира. В Болгарии о первых случаях данного заболевания было доложено в марте 2006 г. на эхокардиографическом курсе Европейского кардиологического общества в Софии, а в последующем — и на Европейском конгрессе по эхокардиографии. Сегодня случаи синдрома такоцубо описаны авторами России, Франции, Бельгии, Мексики, Австралии, Испании, Южной Кореи, Китая, Бразилии, Германии, Израиля, Южной Африки, Турции и Исландии.
На сегодняшний день в Международном регистре синдрома такоцубо зарегистрировано 1750 пациентов.
При этом 90 % больных — женщины после менопаузы в возрасте 66–67 лет, около 10 % — мужчины; кроме того, описаны случаи заболевания даже у детей.
Необходимо отметить, что синдром такоцубо выявляется примерно у 1–2 % среди всех госпитализированных с ОКС.
Анатомические варианты синдрома такоцубо:
- Типичный (верхушечный) вариант (75–80 %) — вовлечение апикальных и средних сегментов левого желудочка, при этом зоны нарушения кинетики миокарда не соответствуют бассейну кровоснабжения какой-либо отдельной коронарной артерии;
- Атипичный вариант («щадящий верхушку вариант») (10–15 %) — верхушка левого желудочка не затронута, а вовлекаются только его средние сегменты;
- Базальный (инвертированный) вариант — 5 %;
- Поражение двух желудочков — менее 0,5 %.
Типичный и атипичный варианты синдрома имеют схожую клиническую картину. Остаётся неясным, почему у некоторых пациентов верхушка левого желудочка не поражается.
Этиология. В первое время считалось, что ведущий этиологический фактор — эмоциональный. Однако в ходе последних наблюдений выяснилось, что более часто провоцирующими факторами являются физические.
Таблица 1
Этиологические факторы синдрома такоцубо
|
Физические факторы — 36 % |
Эмоциональные факторы — 27,7 % |
|
тяжёлая физическая работа; внезапное падение АД; тяжёлая болезнь; хирургическое вмешательство или медицинская процедура; сильная боль; приступ бронхиальной астмы; проведение химиотерапии; инсульт др. |
неожиданная потеря или болезнь близкого человека; получение плохих новостей (например, диагностика рака); несчастный случай; финансовый убыток; потеря работы; семейные конфликты; сильный страх; публичные выступления и др. |
В 28,5 % этиологический фактор остается неизвестным.
Среди 1750 пациентов учёные выделили 485 человек, которые смогли абсолютно точно сказать, какое именно событие стало «спусковым крючком» для синдрома такоцубо. Из этих 485 человек у 465 (26,5 %) приступ случился после печального или трагического события (смерть родственника, посещение похорон, болезнь или смерть любимого человека), вследствие чего синдром получил название «синдром разбитого сердца». Один случай произошёл с человеком, страдавшим от ожирения, после того как он застрял в трубе во время отдыха в аквапарке.
При этом выяснилось, что у 20 (4,1 %) человек болезнь была спровоцирована счастливым событием: празднованием дня рождения, свадьбы, победой любимой спортивной команды, рождением внука. По аналогии с «разбитым сердцем» врачи назвали новое явление «синдромом счастливого сердца».
Таким образом, положительные эмоции тоже могут привести к развитию синдрома такоцубо, т. к. они приводят к ответной реакции вегетативной нервной системы в той же степени, как и отрицательные, что обусловливает изменение ЧСС, ОПСС и уровня АД. Имеются данные о том, что частота развития осложнений сердечно-сосудистых заболеваний может быть на 27 % выше в день рождения по сравнению с другими днями года. Поразителен тот факт, что положительные эмоции вызывают чаще изменения атипичной локализации — поражение средних сегментов (рис. 1).
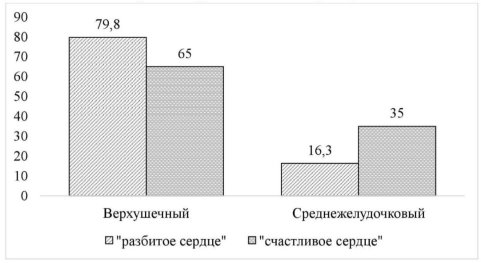
Рис. 1. Анатомические варианты синдрома такоцубо при различных этиологических факторах
Патогенез. Патогенетические механизмы развития синдрома такоцубо сложны и складываются из 3-х составляющих:
- Избыток катехоламинов;
- Спазм коронарных артерий;
- Микрососудистая дисфункция.
Выделение катехоламинов, по всей видимости, играет центральную роль в патофизиологии синдрома такоцубо как пусковой механизм при внезапном стрессе; на момент клинических проявлений отмечаются признаки симпатической активации.
Имеется 2 физиологических момента, требующих рассмотрения.
Во-первых, это когнитивные центры мозга и гипоталамо-гипофизарно-надпочечниковая (ГГН) ось и какое количество адреналина и норадреналина высвобождается в ответ на тот или иной стресс (т. е. «усиление» ГГН-оси).
Во-вторых, реакция сердечно-сосудистой и симпатической нервной системы на внезапную симпатическую активацию и резкое повышение уровня циркулирующих катехоламинов.
Сывороточные уровни катехоламинов на момент клинических проявлений синдрома такоцубо значительно выше, чем в покое, у одного и того же или у сопоставимых пациентов с острым инфарктом миокарда, что указывает на наличие потенциальной возможности избыточного усиления ГГН-оси и высвобождения адреналина.
Возможность патогенной роли катехоламинов выявлена в ряде исследований определения в плазме катехоламинов. Объединяя результаты из этих серий, плазменные уровни норадреналина были повышены в 74 % и составили следующие концентрации: адреналин — 1264 пг/мл (N — 376 пг/мл), норадреналин — 2284 пг/мл (N — 1100 пг/мл). Повышение уровня катехоламинов и обратимые изменения левого желудочка наблюдались также в крысиной модели, вызванной стрессом. Однако, высокий уровень катехоламинов в крови не является повсеместно встречаемым у обследуемых пациентов и некоторые исследования показали нормальный уровень [2].
Сообщается о ятрогенном синдроме такоцубо после введения симпатомиметических препаратов (например, добутамина при стресс-ЭхоКГ).
У некоторых пациентов с кардиомиопатией такоцубо, единственным очевидным стрессом является воздействие препаратов катехоламинов или β‐агонистов в обычных клинических дозах.
Эти патофизиологические гипотезы не могут быть взаимоисключающими, поскольку вся сердечно-сосудистая система подвергается воздействию того же самого катехоламинового шторма. Многие из этих гипотез до сих пор изучаются, поскольку в настоящее время нет доказанных патофизиологических механизмов, объясняющих синдром такоцубо.
Дальнейшая поддержка гипотезы действия катехоламинов обеспечивается наблюдениями подобной обратимой кардиомиопатии с глобальной или очаговой дисфункцией у пациентов с феохромоцитомой и в условиях острого повреждения головного мозга, которые также постулируются связанными с действием катехоламинов. По данным эндомиокардиальной биопсии в серии из 8 пациентов в период дисфункции левого желудочка обнаружены гистологические признаки катехоламиновой токсичности: отсутствие признаков миокардита, обнаружение интерстициального фиброза, внутриклеточное накопление гликогена, множество вакуолей, дезорганизованность цитоскелета миокардиоцитов, увеличение белка внеклеточного матрикса. Эти изменения нивелировались почти полностью после функционального восстановления. Предположительно, что наибольший эффект в апикальной части миокарда может быть связан с более высокой плотностью β‐адренорецепторов в этом месте.
Генетическая предрасположенность. Стрессовые пусковые механизмы синдрома такоцубо указывают на то, что его патофизиология сильно связана с факторами окружающей среды. Тем не менее можно предположить, что у некоторых людей существует генетическая предрасположенность к стресс-индуцированному синдрому такоцубо. Хотя данный синдром не рассматривается в качестве первичной генетической кардиомиопатии, в ряде исследований обнаружена возможность существования генетических факторов риска. Наличие генетической предрасположенности было предположено на основе описания нескольких семейных случаев синдрома такоцубо. Однако в этих исследованиях задействовано относительно небольшое число пациентов. Решение этих противоречий потребует высокого качества фенотипирования, идентификации генов-кандидатов, а также обмена данными высокого качества о большом количестве больных с синдромом такоцубо [3].
Несмотря на подробный анамнез, в 15 % из случаев стрессовый фактор выявить невозможно; остаётся неясным, почему в одних случаях стресс может привести к развитию кардиомиопатии такоцубо, а в других — при наличии даже более сильного стресса данное заболевание не возникает.
Клинические формы. Выделяют 2 клинических подтипа синдрома такоцубо:
Первичный синдром такоцубо — основной причиной обращения за медицинской помощью являются острые сердечные симптомы; пациенты доставляются бригадой скорой помощи или госпитализируются по направлению лечащего врача. Больные этой категории могут как иметь чётко идентифицируемые стрессовые триггеры (часто эмоциональные), так и не иметь их.
Вторичный синдром такоцубо — возникает у пациентов, госпитализированных по поводу другого медицинского состояния (хирургического, анестезиологического, акушерского или психиатрического). У этих больных внезапная активация симпатической нервной системы или повышение уровня катехоламинов приводят к возникновению острого синдрома такоцубо как осложнения первичного состояния или его лечения. При лечении необходимо сосредоточиться не только на собственно синдроме такоцубо и его сердечно-сосудистых осложнениях, но и на первичном заболевании, вызвавшем синдром.
Клиническая картина
Клинический пример
Больная А., 64 года
‒ Жгучие боли за грудиной, без иррадиации, волнообразные, в течение дня;
‒ Боли возникли остро после эмоционального стресса (выступление в суде);
‒ Одышка инспираторного характера, возникающая при умеренной физической нагрузке;
‒ Вызвана «Скорая помощь», зафиксировано АД 80/50 мм.рт.ст.;
‒ Госпитализирована в ЦРБ по месту жительства с подозрением на острый инфаркт миокарда;
‒ Болевой синдром был купирован еще на догоспитальном этапе, более не рецидивировал.
Объективное исследование при поступлении:состояние средней степени тяжести, положение активное, сознание ясное, акроцианоз, периферических отеков нет, пульс 76 в минуту, ритмичный, резкое ослабление I тона над верхушкой сердца, грубый систолический шум по левому краю грудины, над лёгкими с обеих сторон выслушивается большое количество влажных мелкопузырчатых хрипов, живот мягкий, безболезненный; ОАК и ОАМ без особенностей.
На ЭКГ: подъём сегмента ST в I, aVL, V2-V6 отведениях, патологические зубцы Q в этих же отведениях (рис. 2).
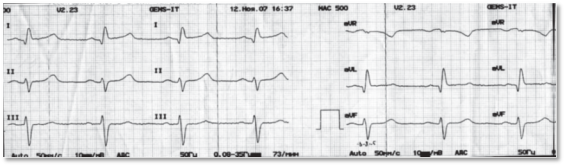
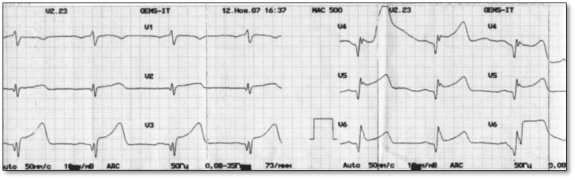
Рис. 2. ЭКГ у больной с синдромом такоцубо в первые часы от начала заболевания
Данные Эхо-КГ: ЛП — 5,1 х 5,7 см; ПП — 3,3 х 4,2 см; конечно-диастолический размер (КДР) ЛЖ — 5,6 см; МЖП — 1,0 см; ФВ — 39,8 %; акинезия всех верхушечных сегментов ЛЖ, гипокинезия средних передне-перегородного, передне-бокового и переднего сегментов; гиперкинезия базальных сегментов; систолическое давление (СД) в ЛА — 76 мм.рт.ст. (N — 30 мм.рт.ст.) (рис. 3).
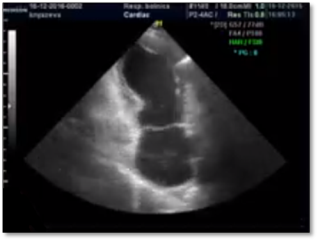
Рис. 3. Эхо-КГ у больной с синдромом такоцубо в первые часы от начала заболевания
Пациентке установлен предварительный диагноз: ИБС. Q-инфаркт миокарда c подъемом ST в переднебоковой стенке. Вечером тоже же дня был выполнен тромболизис капельно в/в 1500000 ЕД стрептокиназы (без осложнений).
В дальнейшем лечение пациентки проводилось по программе ОКС. Между тем, сократимость ЛЖ у больной стала быстро улучшаться, и через 4 дня нарушений локальной кинетики уже не выявляли.
На ЭКГ стала быстро нарастать амплитуда зубца R в отведениях V2-V4 одновременно с исчезновением патологического зубца Q в I, aVL, V2-V4 отведениях и формированием широкого и глубокого отрицательного зубца Т в этих же отведениях.
На Эхо-КГ: полости не расширены, нарушения локальной сократимости нет, ФВ ЛЖ — 69 %, СД в ЛА — 35 мм.рт.ст.
Отсутствовала динамика кардиоспецифических ферментов.
Таким образом, у пациентки с клиникой острой стадии инфаркта миокарда и поздним началом тромболизиса (через 5,5 ч от начала ангинозного приступа) не только произошла нормализация тяжёлых нарушений сократимости ЛЖ, но и зарегистрировано исчезновение (!) уже сформированного патологического зубца Q на ЭКГ при отсутствии значимой динамики кардиоспецифических ферментов. Возникло подозрение на синдром такоцубо и была выполнена коронарография.
Данные коронарографии: правый тип кровоснабжения; ствол проходим, трифуркация ствола, передняя межжелудочковая артерия, интермедиальная артерия, огибающая артерия, правая коронарная артерия — без признаков стенозирования; признаков тромбоза, спонтанных диссекций и осложнённых стенозов нет.
В течение года наблюдения самочувствие пациентки оставалось нормальным. Полное восстановление исходной картины ЭКГ произошло только через 5 месяцев после выписки из стационара.
Диагностика. Диагноз синдрома такоцубо ставится на основании:
‒ клинической картины,
‒ данных ЭКГ,
‒ данных Эхо-КГ,
‒ данных коронарографии.
Таблица 2
Диагностические критерии синдрома такоцубо, предложенные экспертами клиники Мейо
|
1. |
Преходящая гипо-, а- или дискинезия средних сегментов ЛЖ как при вовлечении верхушки, так и в его отсутствие; нарушение локальной сократимости миокарда, распространённость которых превышает зону, кровоснабжаемую какой-либо одной коронарной артерией; часто наличие провоцирующего стрессового фактора |
|
2. |
Отсутствие стенозирующего поражения коронарных артерий или ангиографических признаков острого разрыва атеросклеротической бляшки |
|
3. |
Впервые резвившиеся патологические изменения ЭКГ (либо подъём сегмента ST, либо инверсия зубца Т) или умеренное повышение уровня кардиоспецифического тропонина в крови |
|
4. |
Отсутствие феохромоцитомы и миокардита |
Диагностические критерии клиники Мейо ограничены. Здесь самым главным считается второй пункт — отсутствие поражения коронарных артерий. На сегодняшний день данный критерий не совсем правомочен, поскольку описаны случаи развития синдрома такоцубо как ответная реакция на инфаркт миокарда.
Таблица 3
Диагностические критерии синдрома такоцубо Ассоциации специалистов по сердечной недостаточности (2016)
|
1. |
Транзиторные патологические движения миокарда стенок ПЖ или ЛЖ, которым часто (но не всегда) предшествует стрессовый триггерный механизм (эмоциональный или физический) |
|
2. |
Транзиторные патологические движения миокарда обычно не соответствуют зоне кровоснабжения одной коронарной артерии |
|
3. |
Отсутствие обструкции коронарной артерии, свидетельств отрыва атеросклеротической бляшки, формирования тромба либо прочих патологических состояний, которые могли бы объяснить имеющуюся дисфункцию ЛЖ (гипертрофическая кардиомиопатия, вирусный миокардит) |
|
4. |
Появление новых обратимых ЭКГ-изменений (↑ или ↓ сегмента ST от изолинии, БЛНПГ, инверсия зубца T и/или удлинение интервала QT) во время острой фазы (3 мес) |
|
5. |
Значительное повышение уровня натрийуретического пептида (мозгового натрийуретического пептида [BNP] или его N-терминального фрагмента [NT-proBNP]) во время острой фазы заболевания |
|
6. |
Незначительное повышение уровня сердечного тропонина (т. е. несоответствие между уровнем тропонина и имеющейся кардиальной дисфункцией) |
|
7. |
Восстановление систолической функции желудочка за 3–6 мес |
Таблица 4
Критерии стратификации риска убольных ссиндромом такоцубо
|
Фактор риска |
Высокий риск |
Низкий риск |
|
Возраст |
≥ 75 лет |
˂ 70 лет |
|
Уровень САД |
< 110 мм.рт.ст. |
≥ 110 мм.рт.ст. |
|
Отек легких |
Диагностируется |
Отсутствует |
|
Необъяснимое развитие обморока, желудочковая тахикардия или фибрилляция желудочков |
Диагностируется |
Отсутствует |
|
ФВ ЛЖ |
< 35 % |
≥ 45 % |
|
Обструкция ВТ ЛЖ |
≥ 40 мм.рт.ст. |
Отсутствует или < 40 мм.рт.ст. |
|
Митральная регургитация |
Диагностируется |
Отсутствует |
|
Тромб в области верхушки |
Диагностируется |
Отсутствует |
|
Дефект МЖП или разрыв стенки ЛЖ |
Диагностируется |
Отсутствует |
Лечение. До настоящего времени отсутствуют формальные рекомендации по лечению больных с синдромом такоцубо. Считается, что в острой фазе заболевания показано применение транквилизаторов, если развитию синдрома предшествовал эмоциональный стресс, а также устранение других возможных провоцирующих факторов, например, боли.
Назначаются ингибиторы АПФ, β-дреноблокаторы, антикоагулянты, диуретики, антагонисты кальция.
Если Эхо-КГ не дает убедительных данных, говорящих об обструкции ВТ ЛЖ, можно с осторожностью пробовать лечение инотропными средствами, такими как добутамин и допамин.
Если Эхо-КГ выявит данные об обструкции ВТ ЛЖ, нельзя применять инотропные средства, потому что они могут ухудшить обструкцию. При умеренной и тяжелой обструкции уместно применение β-адреноблокаторов, несмотря на гипотонию. β-адреноблокаторы в таком случае могут улучшить гемодинамику, уменьшая степень обструкции.
В случае отсутствия значимого застоя легких нужно попробовать корригировать гипотонию путем инфузии кристаллоидных растворов.
Независимо от наличия градиента в выходном тракте левого желудочка, при отсутствии эффекта от медикаментозной терапии уместно приступить к интрааортной контрапульсации.
У больных с внутрижелудочковым тромбозом (по данным Эхо-КГ) необходимо проводить антикоагулянтную терапию в течение не менее 3-х месяцев. Продолжительность применения такой антикоагулянтной терапии можно изменить в зависимости от степени восстановления левожелудочковой функции и разрешения тромба.
У больных без тромбоза, но с тяжелой левожелудочковой дисфункцией уместна антикоагулянтная терапия до тех пор, пока не исчезнут признаки акинезии или дискинезии, или в течение 3-х месяцев, в зависимости от того, что наступит первым.
Прогноз. Обратимость синдрома такоцубо — важнейший признак, который помогает отличить его от многих других острых синдромов СН. Временные границы восстановления функции миокарда варьируются в зависимости от тяжести острого эпизода. В качестве ориентира: ФВ ЛЖ обычно восстанавливается через 12 недель. При этом восстановление изменений на ЭКГ может занять до 6–12 месяцев, а в некоторых случаях они могут оставаться патологическими постоянно, например, если возникают рубцовые изменения миокарда.
Возможны осложнения синдрома такоцубо:
‒ острая сердечная недостаточность (12–45 %);
‒ обструкция ВТ ЛЖ (10–25 %);
‒ митральная регургитация (14–25 %);
‒ кардиогенный шок (6–20 %);
‒ фибрилляция предсердий (5–15 %),
‒ желудочковые аритмии (4–9 %),
‒ брадикардия, асистолия (2–5 %);
‒ формирование тромбов (2–8 %);
‒ тампонада сердца (˂ 1 %);
‒ разрыв стенки желудочка (˂ 1 %);
‒ смертность в стационаре (1–4,5 %);
‒ рецидив (5–22 %);
‒ смертность в течение 5 лет (3–17 %).
Факторы развития осложнений:
‒ провоцирующие факторы физической природы;
‒ острое неврологическое или психическое заболевание;
‒ высокая концентрация тропонина;
‒ низкая ФВ в момент госпитализации.
Заключение. Синдром такоцубо представляет собой синдром острой СН, который всё больше привлекает внимание медицинских работников. Многие аспекты этого синдрома недостаточно понятны и не уточнены, а уровень современных знаний недостаточен для того, чтобы создать рекомендации по оптимальному ведению больных. Однако увеличение числа случаев синдрома такоцубо и высокая частота осложнений в период острой фазы заболевания указывает на необходимость усовершенствования тактики ведения больных.
Организация регистров синдрома такоцубо позволит создать инфраструктуру, необходимую для проведения исследований, в частности для разработки новых терапевтических тактик. В отдельных стационарах в год можно наблюдать примерно от 5 до 30 больных с синдромом такоцубо в год, поэтому для получения данных о большем числе больных необходимо создание специальных сетей.
Литература:
- Ватутин Н. Т., Калинкина Н. В., Кетинг Е. В. и соавт. Синдромы в кардиологии: монография. Донецк: Каштан, 2010. — 278 с.
- Гиляревский С. Р. Кардиомиопатия такоцубо. Подходы к диагностике и лечению / С. Р. Гиляревский. — М.: МЕДпресс-информ, 2013. — 184 с.: ил.
- Lyon A. R., Bossone E., Schneider B. et al. Current state of knowledge on Takotsubo syndrome: a Position Statement from the Taskforce on Takotsubo Syndrome of the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail. 2016 Jan; 18 (1): 8–27.
- Ghadri J. R., Cammann V. L., Napp L. et al. Differences in the Clinical Profile and Outcomes of Typical and Atypical Takotsubo Syndrome: Data From the International Takotsubo Registry. JAMA Cardiol. April 13, 2016.
- Ватутин Н. Т., Калинкина Н. В., Савченко Е. А. и соавт. Магнитно-резонансная визуализация в диагностике острого инфаркта миокарда // Український кардіологічний журнал. — 2014. — № 3. — С. 95–102.
- Sheppard M. N. Takotsubo Syndrome — Stress-induced Heart Failure Syndrome. European Cardiology Review. 2015; 10 (2): 83–8.
Ключевые слова
кардиомиопатия, острый коронарный синдром, такоцубо, синдром «разбитого сердца», коронарографияПохожие статьи
Особенности повышенного риска развития хронического...
Так же, у данной категории больных, по мере прогрессирования заболевания установлена выраженность нарушений кардио-респираторной системы.
Есть ли генетическая предрасположенность?
Коронарографиястенозирующихпоражений коронарных артерий.
Влияние остаточных гемодинамически значимых стенозов на...
ACS, больной, подъем сегмента, группа, TCAS, ASE, острый коронарный синдром, острый инфаркт миокарда, коронарная артерия, контрольная группа. Характеристика вариабельности ритма сердца у больных с острым...
Эффективность комплексной терапии Милдроната у больных...
Лечение больных перечисленными способами должно быть начато незамедлительно, как только по клиническим данным и результатам ЭКГ-исследования в покое складывается впечатление о наличии острого коронарного синдрома с и без стойкого подъема сегмента...
Изменения структурно-функционального состояния левого...
больной, ребенок, сердечно-сосудистая система, заболевание почек, патология почек, пациент, группа пациентов
Особенности геометрии левого желудочка у пациентов с метаболическим синдромом и диастолической дисфункцией по типу нарушения релаксации.
Характерные особенности показателей центральной гемодинамики...
ACS, больной, подъем сегмента, группа, TCAS, ASE, острый коронарный синдром, острый инфаркт миокарда, коронарная артерия, контрольная группа. Характеристика вариабельности ритма сердца у больных... SDNN, больной, подъем сегмента, III, HRV...
Состояние центральной и внутрисердечной гемодинамики при...
ACS, больной, подъем сегмента, группа, TCAS, ASE, острый коронарный синдром, острый инфаркт миокарда, коронарная артерия, контрольная группа.
Анатомические и ультразвуковые параллели в диагностике...
Заболевания аорты делятся на дилатации, аневризмы аорты, атеросклеротические и воспалительные поражения, генетические заболевания (например, синдром Марфана), врожденные аномалии, в том числе коарктация аорты, острый аортальный синдром, включая...
Характеристика вариабельности ритма сердца у больных...
Основные термины (генерируются автоматически): SDNN, больной, подъем сегмента, III, HRV, суточное мониторирование, острый
Изучение структурно-функциональных параметров левого желудочка у больных с артериальной гипертензией и синдромом обструктивного...
Похожие статьи
Особенности повышенного риска развития хронического...
Так же, у данной категории больных, по мере прогрессирования заболевания установлена выраженность нарушений кардио-респираторной системы.
Есть ли генетическая предрасположенность?
Коронарографиястенозирующихпоражений коронарных артерий.
Влияние остаточных гемодинамически значимых стенозов на...
ACS, больной, подъем сегмента, группа, TCAS, ASE, острый коронарный синдром, острый инфаркт миокарда, коронарная артерия, контрольная группа. Характеристика вариабельности ритма сердца у больных с острым...
Эффективность комплексной терапии Милдроната у больных...
Лечение больных перечисленными способами должно быть начато незамедлительно, как только по клиническим данным и результатам ЭКГ-исследования в покое складывается впечатление о наличии острого коронарного синдрома с и без стойкого подъема сегмента...
Изменения структурно-функционального состояния левого...
больной, ребенок, сердечно-сосудистая система, заболевание почек, патология почек, пациент, группа пациентов
Особенности геометрии левого желудочка у пациентов с метаболическим синдромом и диастолической дисфункцией по типу нарушения релаксации.
Характерные особенности показателей центральной гемодинамики...
ACS, больной, подъем сегмента, группа, TCAS, ASE, острый коронарный синдром, острый инфаркт миокарда, коронарная артерия, контрольная группа. Характеристика вариабельности ритма сердца у больных... SDNN, больной, подъем сегмента, III, HRV...
Состояние центральной и внутрисердечной гемодинамики при...
ACS, больной, подъем сегмента, группа, TCAS, ASE, острый коронарный синдром, острый инфаркт миокарда, коронарная артерия, контрольная группа.
Анатомические и ультразвуковые параллели в диагностике...
Заболевания аорты делятся на дилатации, аневризмы аорты, атеросклеротические и воспалительные поражения, генетические заболевания (например, синдром Марфана), врожденные аномалии, в том числе коарктация аорты, острый аортальный синдром, включая...
Характеристика вариабельности ритма сердца у больных...
Основные термины (генерируются автоматически): SDNN, больной, подъем сегмента, III, HRV, суточное мониторирование, острый
Изучение структурно-функциональных параметров левого желудочка у больных с артериальной гипертензией и синдромом обструктивного...











