Гетерополисоединения (ГПС) — это класс необычных координационных соединений, в которых оксометаллатная сфера выступает как единый лиганд по отношению к одному или нескольким элементам-комплексообразователям, образуя гетерополианионы (ГПА). Исходя из этого гетерополисоединения бывают одноядерными или многоядерными. Обширные исследования в химии гетерополисоединений велись около 180 лет, за это время накопилась большая экспериментальная справка. Тем не менее не все вопросы являются хорошо освещенными. Существуют несколько типов ГПС. Структуры типа Кеггина- это структуры 12 ряда, то есть имеют 12 атомов молибдена внутри сферы. Структуры Перлоффа (также носят имя Андерсона) — 6 атомов молибдена или вольфрама, которые участвуют в образовании сферы. Также есть гибридные типы, которые можно исследовать с помощью различных физико-химических методов, и устанавливать точный химический и кристаллизационный состав. Уникальность ГПС заключается в том, что они обладают окислительно-восстановительными свойствами. Из них можно получить необычные кислоты — гетерополикислоты, которые образуют гетерополисини. Применение соединений данного вида разнообразно. Их в основном используют в качестве гомогенных и гетерогенных катализаторов. Гетерополисоединения находят место также в синтезе органических веществ. Интерес представляет исследование каталитической активности ГПС в зависимости от состава и структуры [1]. ГПС применяют в аналитической химии для определения фосфора, кремния и германия. В биохимии гетерополисоединения используются в качестве осадителей протеинов, алкалоидов и пуринов. Например, анион [P 2 M 18 O 62 ] 6- применяют для колориметрического определения мочевой кислоты и холестирола.
Применение в качестве красителей и осадителей почти полностью основано на кулоновских взаимодействиях полианионов и катионных групп в биомолекулах.
В производстве красок гетерополимолибдаты и вольфраматы используются для создания цветных лаков, в фотосинтезе они используются в качестве акцепторов электронов. Большие гетерополивольфрамат анионы, например [As 2 W 18 O 68 ] 6- и особенно [NaSb 9 W 21 O 86 ] 18- обнаруживают антивирусные и антиопухолевые свойства.
Гетерокислоты и их соли используются как гетерогенные катализаторы [1] для различных реакций — окисление пропилена и изобутилена в акриловую и метакриловую кислоты, окисление ароматических углеводородов, полимеризации олефинов, гидродесульфирование и др.
Наши ученые большое внимание уделяют гомогенным каталитическим процессам с участием гетерополианионов в растворах. В частности, смешанные полианионы [PV x Mo 12-x O 40 ] n- совместно с солями Pd(II) использовались для каталитического окисления олефинов кислородом воздуха, например этилена в ацетальдегид и др.
Нерастворимые соли гетерополианионов, особенно молибдофосфат аммония, давно используются как дешевые ионообменные материалы, их применяют в хромотографии, для изготовления ион-селективных мембран.
Кристаллические 12-вольфрамофосфорные и 12-молибофосфорные кислоты применяются как протонные проводники.
Области применения гетерополикомплексов все расширяются. Уже опубликованы данные о применении их в качестве ингибиторов пламени, коррозии и для защитных покрытий стали и алюминия. Так как спектр полученных соединений обширен, важно для научной работы выбрать менее изученное, но перспективное для практического дальнейшего применения, например, в качестве катализатора или установить их биологические свойства. Поэтому авторы выбрали ранее неизученный гетерополиникелат натрия. Ранее был синтезирован гексамолибденоникелат аммония, который является гомогенным аналогом по ГПА, но разным по катиону. Синтез ГПС осуществляли по модифицированной методике. Авторы предложили следующий способ гексамолибденоникелата натрия состава Nа 4 [NiMo 6 O 18 (OH) 6 ]·6H 2 O [2]: раствор молибдата натрия, нагревали до 80 С 0 , а раствор нитрата никеля — до 45С 0 . Раствор молибдата натрия подкисляли концентрированной азотной кислотой до рН=3. Данные растворы смешивали, по каплям добавляя перекись водорода 10 %, после чего нагревали на водяной бане в течении двух часов. Затем охлаждали в эксикаторе около недели. Спустя пять дней обнаруживали выпадение зеленых кристаллов, которые промывали водой и высушивали при комнатной температуре. Фото представлено на рис 1.
![Микрофотография Nа4 [NiMo6O18(OH)6]·6H2O](https://articles-static-cdn.moluch.org/articles/j/88378/images/88378.001.jpg)
Рис.1. Микрофотография Nа 4 [NiMo 6 O 18 (OH) 6 ]·6H 2 O
Для детализирования состава был произведен масс-спектральный анализ соединения, результаты которого приведены в табл. 1.
Таблица 1
Данные масс-спектрального анализа Nа 4 [NiMo 6 O 18 (OH) 6 ]·6H 2 O
|
Гетерополисоединение |
Nа |
Ni |
Mo |
O |
|
Найдено, % Для Nа 4 [NiMo 6 O 18 (OH) 6 ]·6H 2 O Вычислено, % |
5.57 5.61 |
4.76 4.85 |
46.52 47.05 |
41.35 41.98 |
Авторами был осуществлен рентгенофазовый анализ (РФА). Благодаря РФА можно узнать сингонию, параметры элементарной ячейки кристалла. Было установлена что гексамолибденоникелат натрия относится к триклинной сингонии, пространственная группа Р1 (таблица 2). Указаны параметры элементарной ячейки, углы, объем элементарной ячейки. Также мы рассчитали по методу Сыромятникова пикнометрическая плотность (таблица 2–3, рис. 2).
Таблица 2
Результаты РФА Nа 4 [NiMo 6 O 18 (OH) 6 ]·6H 2 O
|
a, Å |
b, Å |
c, Å |
α º |
β,º |
γ º |
Z |
V, Å 3 |
ρ,г/см 3 |
|
8,05 |
10,51 |
12,13 |
69,55 |
70,61 |
84,12 |
1 |
911,23 |
2,65 |
![Штрихрентгенограмма Nа4 [NiMo6O18(OH)6]·6H2O](https://articles-static-cdn.moluch.org/articles/j/88378/images/88378.002.png)
Рис.2. Штрихрентгенограмма Nа 4 [NiMo 6 O 18 (OH) 6 ]·6H 2 O
Таблица 3
Данные рентгенофазового анализа
|
№ |
2θ, град |
D, Ǻ |
I, % |
№ |
2θ, град |
D, Ǻ |
I, % |
|
1. |
9,01 |
10,90 |
7 |
9. |
20,03 |
4,46 |
12 |
|
2. |
9,25 |
9,51 |
18 |
10. |
21,93 |
4,07 |
15 |
|
3. |
9,95 |
8,81 |
10 |
11. |
22,53 |
3,98 |
3 |
|
4. |
10,97 |
8,01 |
41 |
12. |
24,64 |
3,69 |
10 |
|
5. |
14,67 |
6,12 |
21 |
13. |
25,45 |
3,46 |
15 |
|
6. |
17,57 |
5,13 |
100 |
14. |
31,06 |
2,89 |
2 |
|
7. |
18,54 |
4,74 |
11 |
15. |
32,47 |
2,79 |
4 |
|
8. |
19,52 |
4,55 |
6 |
16. |
36,39 |
2,44 |
5 |
|
17. |
39,98 |
2,22 |
9 | ||||
Авторами был проведен термогравиметрический анализ, с помощью чего обнаружено 4 эндотермических эффектов. Первый эндоэффект (115ºС) — соответствует удалению шести молекул кристаллизационной воды; второй (при 250ºС) — выделению гидроксильных групп в виде трех молекул воды; при эндотермическом эффекте (при 375ºС) происходит перекристаллизация, при заключительном эндоэффекте (770ºС) — удаление 4 молекул оксида молибдена. При сравнении рентгенограммы образца, прокаленного после 375С, установлено, что в продуктах термолиза находятся молибдат натрия, ортомолибдат никеля и оксид молибдена. Сравнение рентгенограммы после 770C указывает на отсутствие оксида молибдена.
Авторы сформировали схему термолиза ГПС.
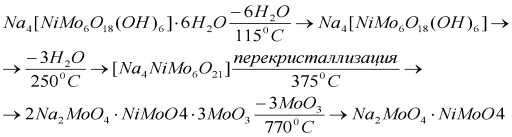
Литература:
- Поп М. С. Гетерополи- и изополиоксометаллаты. Новосибирск: Наука, 1990. 232 c.
- Орешкина А. В., Казиев Г. З. Глазунова Т. Ю. Синтез и исследование кислых гексамолибденометаллатов с никель-аммиачным катионом// Журн.неорган.химии. 2008. Т.53. № 10. С.1662–1666.

