На территории плотной застройки крупных городов единственными объектами живой или искусственно созданной природной среды остаются парки. За внешним видом и состоянием персонал следит ежедневно, а наблюдение за экологическим и биогеохимическим состоянием требует специальных приборов, квалификации кадров, лабораторных опытов и т.д. В лабораторных условиях мы провели исследование отобранных образцов воды Большого Ангарского пруда с целью определить значения электропроводности воды и содержания таких химических веществ, как азот, фосфор и фосфаты, аммиак и органические вещества.
Ключевые слова : исследование, парк, водный объект, пробы воды, электропроводность, содержание химических веществ.
Объектом отбора проб воды является Большой Ангарский пруд, находящийся в парке «Ангарские пруды» на севере г. Москвы между Коровинским шоссе, Ангарской ул., ул. Софьи Ковалевской, ул. Восьмисотлетия Москвы и Проектируемым проездом № 4599. Большой Ангарский пруд занимает площадь 3,6 га, расположен между Ангарской ул. и ул. Софьи Ковалевской. Пробы были отобраны в трех точках, на визуальной середине пруда и по краям, месту впадения водотока и упора в насыпь. Отобранные образцы воды из каждой точки мало отличаются друг от друга. Вода чистая, не мутная, без запаха.
Электропроводность обусловлена наличием в веществе подвижных электрических зарядов — носителей тока. Видом носителя тока определяется электронная, ионная, электронно-ионная и дырочная. В зависимости от удельной электрической проводимости все тела делят на проводники, полупроводники и диэлектрики, физ. величина, обратная электрическому сопротивлению. В СИ единицей электрической проводимости является сименс, 1 См = 1 Ом-1 [1]. Значение электропроводности воды не является константой, а зависит от наличия в ней солей и иных примесей. Так, например, электропроводность дистиллированной воды будет минимальна. Величину электропроводности измеряем с помощью кондуктометра HM Digital COM-80. Для каждого образца значение выражается в µS (микросименс). Полученные результаты определения электропроводности проб воды представлены в Таблице 1.
Таблица 1
Результаты измерения электропроводности проб воды
|
Исследуемый объект |
№ пробы по порядку |
Значение электропроводности, µS |
|
Большой Ангарский пруд |
1 |
190 |
|
2 |
280 |
|
|
3 |
255 |
|
|
Водопроводная вода |
- |
460 |
Значения электропроводности проб Большого Ангарского пруда различаются между собой, а также намного меньше значения водопроводной воды. Различия в показателях могут быть связаны с различной минерализацией воды, а также с геологией области расположения исследуемого водного объекта.
Для определения наличия азота в исследуемых пробах выполнено следующее. В пробирки с пробами было добавлено одинаковое количество NH 4 Cl. Затем, полученный раствор был пропущен через Цинк. Для определения наличия азота в пробах, в каждую из них добавлен реактив Грисса. При наличии азота в пробе окрас образца сменится на красный, или его оттенки, в зависимости от содержания искомого вещества. Также для сравнения в одной пробирке был концентрированный раствор с азотом. Уравнение реакции выглядит как:
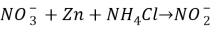
Все отобранные пробы дали отрицательный результат на наличие азота. Проверочная проба дала положительный результат.
Принцип определения аммиака в воде основан на его способности вступать в химическую реакцию с реактивом Несслера, который окрашивает раствор в красно-бурый цвет. О наличии и ориентировочном содержании аммиака в воде можно судить по интенсивности этой окраски.
Реакция идет по уравнению:
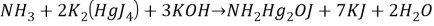
Так же, как и в опыте по определению азота, добавляем одну пробирку с раствором, содержащим аммиак.
Все пробы, кроме контрольной дали отрицательный результат, потому что окрас не сменился. Значит, все исследуемые пробы не содержат аммиак.
В водах соединения фосфора, как минеральные, так и органические могут присутствовать в растворенном, коллоидном и взвешенном состоянии. Переход соединений фосфора из одной формы в другую осуществляется довольно легко, что создает сложности при определении тех или иных его форм. В том случае, когда анализируют фильтрованную пробу, говорят о растворенных формах, в противном случае о суммарном содержании.
Определение растворенных фосфатов (ортофосфатов) осуществляется по реакции с молибдатом аммония и аскорбиновой кислотой с образованием молибденовой сини в исходной водной пробе. При определении фосфатов из-за кислой реакции среды может гидролизоваться некоторая часть полифосфатов или лабильных органических соединений фосфора, но доля таких соединений невелика и на практике этим пренебрегают [2].
Предельно допустимая концентрация фосфатов (в пересчете на фосфор) в воде водных объектов рыбохозяйственного назначения составляет:
— для олиготрофных водных объектов 0,05 мг/дм3;
— для мезотрофных — 0,15 мг/дм3;
— для эвтрофных — 0,20 мг/дм3.
Предельно допустимая концентрация фосфатов для водных объектов хозяйственно-питьевого и культурно-бытового назначения не установлена, в них нормируется только содержание полифосфатов. Предельно допустимая концентрация полифосфатов составляет 3,5 мг/дм 3 в пересчете на фосфат-ион и 1,1 мг/дм 3 в пересчете на фосфор [3].
Для проверки была добавлена пробирка с пробой, содержащей фосфаты. При добавлении реактива в каждую пробу, окрас исследуемых проб не изменился, в отличие от проверочной. Следовательно, в пробах воды фосфаты отсутствуют.
В воде всегда присутствуют органические вещества в виде взвесей, коллоидных или молекулярных соединений. В настоящее время нет достаточно надежного способа, позволяющего полностью выделить органическое вещество из воды и оценить его количественно, поэтому чаще пользуются косвенными методами для того, чтобы судить о содержании этого вещества в природных водах. Наиболее распространена оценка количества органического вещества по окисляемости воды.
Окисляемость — это величина, показывающая общее содержание в воде органических веществ, окисляемых одним из сильных химических окислителей. Этот показатель отражает общую концентрацию органики в воде [4].
Происхождение и содержание органических веществ, находящихся в природных водах, весьма разнообразны. Различны и их химические свойства по отношению к кислороду: одни вещества устойчивы к окислению, другие, наоборот, легко окисляются. Прямое определение органических веществ в природных водах является сложной и трудоемкой задачей. Поэтому пользуются более простыми косвенными методами. Один из них — это метод перманганатной окисляемости, дающий представление о содержании в воде легко окисляющихся органических веществ.
В ходе проведения опыта на определение содержания в пробах органических веществ, в щелочной раствор (25 %) добавляли пробу воды, затем добавляли перманганат калия. В результате реакции пробы, не содержащие органические вещества, приобретали темно красный цвет. Пробы, содержащие органические вещества, меняли цвет на зеленый или его оттенки. В ходе опыта только 2 пробы поменяли окрас на зеленый. Это значит, что в них присутствуют органические вещества.
Литература:
- Большая политехническая энциклопедия. — М.: Мир и образование. Рязанцев В. Д. 2011
- Е. В. Веницианов. Экологический мониторинг: шаг за шагом. 2003
- ГОСТ 18309–2014 Вода. Методы определения фосфорсодержащих веществ.
- ГОСТ Р 55684–2013 (ИСО 8467:1993) Вода питьевая. Метод определения перманганатной окисляемости.







