В работе описана оптимизация анализа аспирина методом высокоэффективной жидкостной хроматографии. Был подобран оптимальный состав подвижной фазы, приготовлен соответствующий фосфатный буфер, подобрана оптимальная скорость потока. Получены хроматограммы растворов аспирина с различными концентрациями. Анализ проводился в изократическом режиме.
Ключевые слова: высокоэффективная жидкостная хроматография, аспирин, отработка метода .
Высокоэффективная жидкостная хроматография (ВЭЖХ) — метод анализа веществ, основанный на различной скорости прохождения веществ через колонку, заполненную адсорбентом. ВЭЖХ позволяет проводить одновременное разделение сложных проб на составляющие соединения, детектирование большинства компонентов, измерение концентрации одного или нескольких соединений.
В настоящее время ВЭЖХ широко используется в анализе лекарственных веществ — количественном определении действующих веществ и примесей. Для повышения качества и безопасности продукции в фармацевтической индустрии используются современные методы
анализа, чаще всего это хроматографические методы, имеющие множество преимуществ, таких как: быстрота определения, эффективное разделение, высокая чувствительность.
В результате комбинации ограниченного числа сорбентов и неограниченного числа различных по составу подвижных фаз возможно решение множества встречающихся на практике задач. Подвижная фаза в ВЭЖХ выполняет двоякую функцию:
1) обеспечивает перенос десорбированных молекул по колонке (подобно подвижной фазе в газовой хроматографии);
2) регулирует константы равновесия, а, следовательно, и степень удерживания исследуемого вещества.
Метод жидкостной хроматографии (ЖХ) применим для разделения значительно более широкого круга веществ, чем метод газовой хроматографии. Это связано с тем, что большая часть веществ не обладает летучестью и многие вещества неустойчивы при высоких температурах. В ЖХ разделение обычно происходит при температуре, близкой к комнатной.
В ряде случаев преимущества непосредственного сочетания высокочувствительного обнаружения с процессом разделения нескольких веществ теряются вследствие того, например, что при фотометрическом обнаружении в УФ-области или в видимой области спектра 1) элюируемые вещества могут обладать различными максимумами поглощения, в то время как большинство детекторов допускает измерение лишь при одной длине волны, и 2) требуемая (в УФ-области) прозрачность подвижной фазы ограничивает область применения как детектора, так и собственно хроматографов. В то же время в отдельных случаях эти ограничения могут способствовать высокой селективности анализа [1].
Материалы и методы исследования
Оборудование:
- Высокоэффективный жидкостный хроматограф Agilent 1100 c хроматографической колонкой с18 и диодно-матричным детектором
- Дополнительное оборудование: аналитические весы, спектрофотометр, pH-метр, пипет-дозаторы, ареометр
Компоненты подвижной фазы:
Ацетонитрил, дигидрофосфат калия, дистиллированная вода, фосфорная кислота
Объект исследования — Аспирин «Кардио» (Bayer)
Определение аспирина методом ВЭЖХ проводилось в следующих условиях: скорость потока 1,0 мл/мин, аналитическая длина волны 272 нм. Были проведены анализы и с другими скоростями потока (от 0,5 до 1,5), но наилучшие результаты разделения были достигнуты именно при этих значениях. При 272 нм наблюдается максимум поглощения аспирина.
Для пробоподготовки лекарственного вещества брали точные навески с помощью аналитических весов и разбавляли рассчитанным и отобранным с помощью пипет-дозатора объемом раствора ацетонитрила.
В качестве элюента была подобрана смесь ацетонитрил-вода-фосфатный буфер с pH 2.3, в соотношении 70:28:2. Анализ проводился в изократическом режиме. Изократический режим-режим, при котором на протяжении всего эксперимента состав подвижной фазы остается неизменным.
Фосфатный буфер потребовался в связи с необходимостью перевести в одну форму ацетилсалициловую кислоту, которая может присутствовать в двух формах — протонированной и ионной.
Фосфатный буфер с pH 2.3 был приготовлен по методике, описанной у F. Pragst — UV Spectra of Toxic Compounds [2]. Для точного определения концентрации имевшейся фосфорной кислоты была измерена ее плотность с помощью ареометра. Она оказалась равна 1.64 г/мл, что соответствует 82.5 %. Растворением в 245 мл дистиллированной воды навески 1.62 г дигидрофасфата калия, а также 739 мкл фосфорной кислоты (82.5 %), отобранных с помощью пипет-дозатора, было приготовлено 250 мл фосфатного буфера. С помощью pH-метра был определен pH полученного раствора. Он оказался 2.7. После добавления еще 250 мкл фосфорной кислоты pH достиг необходимого значения — 2.3.
В ходе данного исследования была выявлена проблема, связанная с перепадами давления внутри колонки, которая не позволяла обнаружить вещество, так как было много побочных шумовых пиков, сигналы размывались. Было принято решение увеличить скорость потока до 2 мл/мин, обеспечив возрастание давления настолько, чтобы можно было обнаружить место неполадки. Благодаря этому была выявлена проблема с колонкой: растворители стали вытекать с одного из концов колонки — выявлена и устранена негерметичность.
Для сравнения была взята хроматограмма, полученная на колонке с октадецилсиликагелем (C18) (4.6×100мм) [3]. Лекарственное вещество — аспирин. Элюентом служила смесь ацетонитрил-вода в соотношении 2:8. Сигнал ацетилсалициловой кислоты острый, хорошо выраженный (Рис. 1.)

Рис. 1. Хроматограмма-образец
После устранения неполадок полуено несколько хроматограмм в различных условиях. На Рис. 2 показана хроматограмма, полученная нами на колонке с октадецилсиликагелем (C18) (4.6×100мм). Для анализа был приготовлен раствор концентрацией 200 мг/л. Элюентом служила смесь ацетонитрил-вода-фосфатный буфер в соотношении 70:28:2.
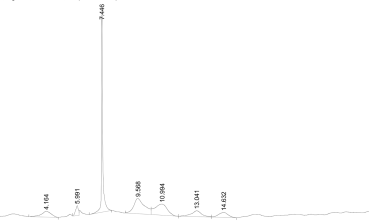
Рис. 2. Хроматограмма аспирина, сигнал ацетилсалициловой кислоты (концентрация 200 мг/л)
На Рис. 3 показана хроматограмма, полученная нами на колонке с октадецилсиликагелем (C18) (4.6×100мм). Для анализа был приготовлен раствор в ацетонитриле концентрацией 100 мг/л. Элюентом служила смесь ацетонитрил-вода-фосфатный буфер в соотношении 70:28:2.

Рис. 3. Хроматограмма аспирина, сигнал ацетилсалициловой кислоты (концентрация 100 мг/л)
Результаты
В результате исследования аспирина методом высокоэффективной жидкостной хроматографии нами были установлены оптимальные условия для анализа аспирина методом ВЭЖХ: подобран оптимальный состав элюента, подобрана оптимальная скорость потока, при которой вещество выходит из колонки за разумное время и при этом не происходит повышения давления выше нормы, решена проблема перепадов давления внутри колонки, получены хроматограммы растворов аспирина концентрациями 200 мг/л и 100 мг/л с острыми выраженными сигналами от ацетилсалициловой кислоты.
Авторы выражают благодарность за помощь в проведении работ Алабушевой В., компании BIOCAD за предоставление высокоэффективного жидкостного хроматографа, университету ИТМО за предоставление хроматографической колонки C18 и ацетонитрила высокой степени чистоты.
Литература:
- Шаповалова, Е. Н. Хроматографические методы анализа. Методическое пособие для специального курса / Е. Н. Шаповалова, А. В. Пирогов. — Москва: Изд-во МГУ, 2016. — 230 c.
- UV Spectra of Toxic Compounds / F. Pragst, M. Herzler, S. Herre [и др.]. — 2. — Heppenheim:, 2001. — 133 c.
- Фролова, Т. А. Возможности гидрофильной хроматографии в анализе фармацевтических препаратов, содержащих ионогенные вещества. / Т. А. Фролова, О. Б. Григорьева, Е. Ю. Аношина. // Хроматография Agilent. — Москва:, 2010. — С. 12–15.
- Анализ фармацевтических препаратов ВЭЖХ и СВЭЖХ как методы определения лекарственных веществ в крови / Ю. В. Медведев, Г. В. Раменская, И. Е. Шохин, Т. А. Ярушок. // Аналитические решения Аджилент. — 2011. — № 1. — С. 3–6.

