Проведены сопоставительные исследования превращений н-С 4 Н 10 (С 4 ), н-С 7 Н 16 (С 7 )и их смеси (1:1мол)при атмосферном давлении, в интервале 140–200 0 ,Н 2 /С=3 и о. с. 2,5ч -1 в присутствии композиционных катализаторов 0,5 %Со /Al 2 O 3 (А)или0,5 %Со /HZSM-5(М)/10 % SZ (где SZ-ZrO 2 -SO 4– 2 (2 %)). Найдено, что в отличии от преимущественно изомеризационного превращения н-алканов на А/SZ, для превращения С 4 :С 7 смеси характерно низкое вовлечение в процесс С 4 , образование С 5 -С 6 алканов и низкая стабильность катализаторов. В отличии от А/SZ, превращение С 4 :С 7 смеси на М/SZ реализуется с высокой конверсией С 4 , стабильным функционированием катализатора и повышенными выходами С 5 -С 6 алканов. При 180 0 конверсия С 4 и С 7 составляет соответственно 43,4–36,7 %, а селективность по С 5 –С 6 36,6 %. Сделано предположение о первичной активации образования [С 4 +С 7 ] интермедиата и его изомеризации на SZ, и последующим гидродиспропорционированием промежуточных веществ с участием бренстедовских кислотных центров HZSM-5.
Ключевые слова: н-бутан, н-гептан, смесь, композиционный катализатор, цеолит, бимолекулярный механизм.
В производстве автомобильных бензинов наблюдается постоянная тенденция к ограничению в них содержания ароматических углеводородов, особенно бензола и непредельных углеводородов при сохранении высокооктановых характеристик топлива. Эффективное решение данной проблемы связано развитием процесса изомеризации н-парафинов. В современных технологических схемах производства бензинов качестве сырья используется лёгкая нафта. Эффективность процесса изомеризации, направленное на получение высокооктановых компонентов бензина (изопентана и диметилбутанов), зависит от рецикла низкооктановых н-пентана и гексанов, т. е. сводится к индивидуализации изомеризации отдельных С 5 и С 6 компонентов лёгкой нафты [1].
Промышленно предпочитаемыми катализаторами изомеризации С 4 -С 6 парафинов являются среднетемпературные (280–300 0 ) цеолитные и относительно низкотемпературный (180–210 0 ) диоксид циркония [2]. Эти катализаторы, как правило, промотированы платиной и функционируют при давлениях 1,5–3,0 МПа. Содержание в сырье С 7 парафинов оказывает отрицательное воздействие на стабильность функционирования отмеченных катализаторов и, поэтому, их содержание в сырье должно быть ограничено в пределах 2–5 % масс [3].
Отмеченные особенности процесса изомеризации лёгкой нафты и ограниченность её содержания в ископаемом сырье являются факторами, ограничивающими широкомасштабное производство не содержащих высокооктановых бензинов без ароматических компонентов.
Известно, что изомеризация н-бутана реализуется по бимолекулярному механизму с образованием и последующим гидрорасщеплением интермедиата С 8 в целевой продукт изобутан и побочные С 3 -С 5 -алканы, т. е. продукты диспропорционирования [4]. В отличии отн-бутана , С 5 -С 7 н-алканы, в основном изомеризуются мономолекулярно [5], путём перехода вторичного карбокатиона в третичный, через промежуточный циклопропильный ион и миграцию гидрида иона. Вместе с тем нельзя исключать роль и бимолекулярного протекания процесса с участием образующихся продуктов гидрораспада.
Образование подобных соединений и их накопление на поверхности SZ, может быть причиной быстрой дезактивации катализатора. Необходимость промотирования катализатора типа SZ платиной и высокое давление водорода, по-видимому, эффективно блокирует образование бимолекулярных интермедиатов и тем самым, повышает стабильность процесса изомеризации н-парафинов.
Ранее было показано, что контактирование смеси н-парафинов С 6 и С 4 , с катализатором М/Н-цеолит/ SZ, при 140–200 0 и атмосферном давлении водорода, бимолекулярное протекание процесса, приводит к образованию С 4- и С 6+ алканов [6]. Применение гидрокрекирующего цеолитного компонента способствует не только стабилизация превращения н-С 6 , но также повышает активность катализатора по преращению н-С 4 . Таким образом, наблюдается рост изомеризационно-диспропорционирующей активности М/Н-цеолит/ SZ композиционного катализатора. Вовлечение в процесс изомеризационного диспропорционирования н-гептана и н-бутановой смеси на SZ –цеолитной каталитической системе может снизить позволить снизить отрицательное влияние С 7 - парафинов на изомеризацию лёгкой нафты и повысить ресурс С 5 -С 6 алканов, необходимых для производства современных бензинов. Поэтому настоящее сообщение посвящено сопоставительному изучению превращений н-С 4 , н-С 7 парафинов и их смеси(1:1,мол) на композиционном катализаторе 0,4 % Со / НZSM-5 / SO 2– 4 (2 %) ZrO 2 и на его компонентах при атмосферном давлении, в интервале температур 140–200 0 .
Экспериментальная часть
Объектом исследования служили композиционные катализаторы (КК) состава Со/HZSM-5 или Аl 2 O 3 /SO 4– 2 /ZrO 2 , или их компоненты приготовленные по методике [7]. В качестве источника активных компонентов использовали соли циркония ZrO(N0 3 ) 2 ∙2H 2 0 и кобальта. КК системы готовили путем выдержки декатионированного HZSM-5 (Si/Al = 23) в растворе нитрата кобальта заданной концентрации в течение 24ч с последующей фильтрацией, сушкой при 120 и 350°С (3 ч), прокалкой при 550°С (5 ч) и обработкой в токе водорода (40 мл·мин–3 ч) при 380°С. При синтезе SZ компонента КК предварительно получали гель диоксида циркония, путём гидролиза ZrO(N0 3 ) 2 , взятого в заданном количестве, 25 %-ным раствором аммиака при рН 8–9 [8]. С этой целью в раствор, содержащий 10 г ZrO(N0 3 ) 2 ∙2H 2 0 в 300 мл Н 2 О, нагретой до 80°, по каплям при перемешивании добавляли раствор аммиака. Образовавшийся гель 2ч выдерживали в растворе при указанной выше температуре, затем фильтровали, промывали дистиллированной водой и сушили при 100° (24ч). Полученный гидрогель Zr(ОН) 4 сульфатировали раствором (NH 4 )2SO 2– 4 (с перемешиванием 2 ч), а затем водную часть выпаривали до визуально влажного состояния.
Превращение н-бутана и н-гептана и их смеси изучали на лабораторной каталитической установке проточного типа, снабженной кварцевым реактором. Объем катализатора, загружаемого в реактор, варьировали в пределах 1–5 см 3 при поддержании постоянства приведённых ниже условий процесса.
Перед опытом проводили восстановление КК системы водородом при 380° (2 ч). Превращение н-бутана и н-гептана и их смеси на КК системах изучали варьированием температуры (Т) в интервале 140–220
0
, с объемной скоростью подачи бутана (275ч
-1
) и гептана (WHSV-2,5ч) при атмосферном давлении и линейной скоростью водорода 2л/час. Сопоставительный анализ реактантов и продуктов реакции осуществляли отбором проб непосредственно на входе и на выходе из реактора (on-line режим) и их анализом методом ГЖХ с использованием хромотографа Auto-Sistem XL (Perkin Elmer) с капиллярной колонкой metilfenilsilksan (100м 0.25мм
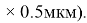
Применяемый азот, с чистотой 99,6 %, дополнительно подвергали очистке от примесей кислорода и паров воды, а водород, получаемый электролизом, проходил через осушитель.
Исходным сырьём служили: сжиженный н-бутан чистотой не менее 96,6 мас. %, н-гептан (ХЧ) и их смесь в мольном соотношении 1:1.
Первичную характеристику реализации процесса осуществляли сопоставительным анализом углеводородного состава на входе и выходе из реактора. Учитывая стабилизацию функционирования КК к 20 минуте эксперимента, каталитические данные, приведённые ниже, для определённости, соответствует 30 минуте опыта.
Перед проведением опытов образцы КК подвергали стандартной (регенерационной) обработке азотом (чистота 99,6 %), а затем воздухом при 500
0
С (2 ч) и электролизным водородом при 380
0
С (2 ч) с линейной скоростью 2 л/ч. Превращение бутана, гептана и их смеси проводили при атмосферном давлении, в интервале температур 140–200
0
. Подачу реактантов осуществляли в среде водорода при мольном соотношении Н
2
/СН=2. Сопоставительный анализ реактантов и продуктов реакции осуществляли отбором проб непосредственно на входе и на выходе из реактора (on-line режим) и их анализом методом ГЖХ с использованием хромотографа Auto-Sistem XL (Perkin Elmer) с капиллярной колонкой metilfenilsilksan (100м 0.25мм
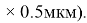
Первичную характеристику реализации процесса осуществляли сопоставительным анализом углеводородного состава на входе и выходе из реактора. Учитывая стабилизацию функционирования КК к 20 минуте эксперимента, каталитические данные, приведённые ниже, для определённости, соответствует 30 минуте опыта.
Исходя из первичных данных, для оценки вовлечённости смеси бутана и гептана в процесс образования продуктов превращения (С 5 — С 6 и С 7 ), конверсии компонентов С 4- и С 8+ рассчитаны раздельно
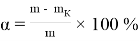
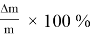
Где:
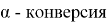
m –исходное количество в реактанте;
m k –остаточное количество в катализате.
Селективность определяли по формуле:
Sel =

где
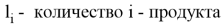
Для характеристики превращения смеси алканов, суммарную конверсию рассчитывали по формуле:
∑ конв. = 0,37× α 1 +0,63× α 2 (3)
α 1 — конверсия C 4 Н 10 0,37 и 0,63 — весовое соотношение молей
α 2 — конверсия C 7 Н 16
Рентгенографический анализ образцов катализаторов осуществляли на дифрактометре ДРОН-ЗМ. Съёмку проводили при CuК α -излучении с Ni фильтром на воздухе при комнатной температуре.
Определение количеств углеродистых отложений, накапливающихся на катализаторах, проводили окислительной обработкой катализатора. Перед проведением опытов установку продували инертным газом (Не) 1ч. Затем катализатор обрабатывали воздухом со скоростью подачи 4л ч -1 при 500 0 С. Количества выделившихся Н 2 О и СО 2 определяли как гравиметрически (путём их поглощения ангидроном и аскаридом, помещённые в соответствующие капсулы, с последующим взвешиванием этих ампул), так и непосредственно, анализом образовавшихся углеродистых отложений с применением элементного анализатора фирмы TruSpec Micro. Во избежание ошибок воздух, входящий в реактор, также пропускали через трубки, заполненные ангидроном и аскаридом.
Для установления структурных особенностей использованного композиционного катализатора, его компонентов и их взаимодействия использовали ИКС диффузного отражения. Перед проведением этих исследований образцы предварительно подвергали стандартной обработке в токе воздуха (20мл/мин;1ч) при 500 0 водородом и при 380 0 гелием. ИКС — спектры образцов регистрировали на ИК-Фурье спектрометре ALPHA (фирма BRUKER Германия) в диапазоне волновых чисел 400–4000см -1 .
Результаты и обсуждение
Сопоставительные превращения н-бутана и н-гептана на Со /Al 2 O 3 /SZ представлены, соответственно, в табл.1 и табл.2. Полученные данные показывают высокую активность SZ катализатора в превращении этих молекул. В интервале температур 160–200 0 н-бутан подвергается интенсивным превращениям с образованием изо-бутана и эквимолярной смеси С 3 , С 5 алканов. С ростом температуры селективность образования изо-бутана снижается, а С 3 , С 5 алканов возрастает (табл.1).
Таблица 1
Превращение н-бутана на SZ — содержащих композиционных катализаторах
|
t , 0 С |
Со / Al 2 O 3 / SZ |
Со/ HZSM-5 / SZ |
||||
|
конверсия, % |
Селективность, %мас . |
Конверсия, % |
Селективность, %мас . |
|||
|
Изо –С 4 |
С 3 +С 5 |
Изо –С 4 |
С 3 +С 5 |
|||
|
160 |
30,5 |
95,1 |
4,9 |
34 |
94,1 |
5,9 |
|
180 |
34,5 |
90,8 |
9,2 |
- |
- |
- |
|
200 |
41,0 |
73,9 |
26,1 |
46 |
51,5 |
48,5 |
Подобное превращение н-С 4 Н 10 может происходить вследствие первичной активации образования бимолекулярного интермедиата С 8 , его изомеризации и последующего гидрорасщепления [9], т. е. образующие продукты являются результатом изомеризационно-диспропорционного (ИД) процесса. С повышением температуры выход С 3 , С 5 продуктов возрастает, что указывает на диспропорционирующее возрастание SZ.
Превращение н-гептана на Со /Al 2 O 3 /SZ, существенно зависит от температуры опыта (табл.2). При температурах 140–160 0 основными продуктами реакции является изо-гексаны, а побочными С 6- парафины. С ростом температуры снижение выхода изо-С 7 сопровождается монотонным ростом С 3 -С 4 алканов, по составу близкому в интервале температур140–160 0 практически не изменяется, а далее с ростом температуры монотонно снижается. Из данных представленных в табл.2, следует, что образование С 3 -С 4 является следствием β-гидрорасщепления по отношению к третичному атому в молекуле изо-С 7 Н 16 , а активация н-С 7 Н 16 протекает с образованием С 7 + интермедиата, изомеризацией через соответствующий циклоалькильный переход и миграцией гидрид иона, т. е. по мономолекулярному механизму изомеризации [5,12].
Таблица 2
Влияние температуры на превращение н-гептана.
|
t, 0 С |
Со / Al 2 O 3 / SZ |
Со/ HZSM-5 / SZ |
||||||
|
конверсия, % |
выход, %мас |
конверсия, % |
выход, %мас |
|||||
|
С 3 –С 4 * |
С 5 –С 6 |
изо-С 7 |
С 1 -С 4 |
С 5 -С 6 |
изо-С 7 |
|||
|
140 |
56 |
7,5 |
2,1 |
46,4 |
43 |
4,5 |
5,3 |
33,2 |
|
160 |
78 |
35,8 |
2,1 |
40,1 |
64 |
29,2 |
6,5 |
28,3 |
|
180 |
84 |
53,8 |
1,8 |
28,4 |
72 |
36,7 |
7,3 |
28,0 |
|
200 |
95 |
83,2 |
1,6 |
10,2 |
93 |
80,5 |
2,5 |
10,0 |
*содержание С 1 -С 2 не превышает 1 %.
Превращение смеси н-С 4 Н 10 : н-С 7 Н 16 отличается от индивидуального превращения этих веществ. Из данных представленных в табл.3, следует, что на Со /Al 2 O 3 /SZ в результате взаимовлияния компонентов смеси происходит резкое снижение конверсии н-С 4 Н 10 и почти двукратное н-С 7 Н 16 по сравнению с индивидуальными превращениями этих веществ.
Таблица 3
Превращение н-С 7 Н 16 : н-С 4 Н 10 (1:1 мол) на Со / Al 2 O 3 / S О 2– 4 — ZrO 2
|
Температура, 0 С |
Распределение продуктов |
|||||||
|
конверсия, % |
селективность, %мас |
|||||||
|
н-С 4 Н 10 |
н-С 7 Н 16 |
С 7 +С 4 |
С 3 |
С 4 |
С 5 –С 6 |
Изо-С 7 |
||
|
140 |
2,7 |
27,1 |
25,0 |
2,2 |
- |
56,2 |
41,6 |
|
|
160 |
4,6 |
40,3 |
30,0 |
8,2 |
- |
44,9 |
46,9 |
|
|
180 |
7,5 |
45,4 |
55,0 |
13,6 |
- |
36,8 |
49,6 |
|
|
200 |
- |
57,6 |
57,6 |
28,3 |
30,2 |
23,6 |
17,9 |
|
Введение в реакцию н-С 4 Н 10 оказывает существенное воздействие на распределение продуктов превращения н-С 7 Н 16 на этом катализаторе, в результате которого, в катализате, значительно повышается содержание С 5 -С 6 алканов. Повышение температуры от 140 до 180 0 приводит к монотонному снижению выхода С 5 -С 6 и повышению выхода изо-С 7 алканов (табл.3).
Выхода С 3 в этом температурном интервале значительно ниже по сравнению с выходами превращения чистого н-С 7 Н 16 . Здесь следует учесть, что вклад диспропорционирования н-С 4 Н 10 в образование С 3 и С 5 алканов незначителен, т. е. С 3 является продуктом распада С 7 , а конверсия н-С 4 Н 10 являются суммарным отражением образования и вовлечения С 4 в процесс превращения смеси н-С 4 Н 10 : н-С 7 Н 16 на Со /Al 2 O 3 /SZ. Принимая во внимание отсутствие в продуктах реакции С 1 -С 2 углеводородов и вовлечение в процесс от 2,7 до 7,5 % исходного С 4 Н 10 , можно предположить, что наличие в продуктах превращения С 5 -С 6 алканов является результатом образования бимолекулярного интермедиата [С 4 +С 7 ] и его гидрораспада. С повышением температуры до 200 0 происходит резкое снижение образования С 5 -С 6 и изо- С 7 продуктов реакции. В этом случае процесс приобретает характер близкий к характеру превращения чистого н-С 7 Н 16 . Отсутствие конверсии н-С 4 Н 10 и резкое снижение выхода С 5 -С 6 алканов указывает на снижение вклада в процесс бимолекулярной составляющей превращения н-С 7 Н 16 посредством образования [С 4 +С 7 ] интермедиата. С другой стороны снижение конверсий н- С 7 Н 16 от 95 (табл.2) до 57,6 % в присутствии н-С 4 Н 10 (табл.3) показывает, что н-бутан блокирует гидрорасщепление С 7 промежуточных веществ благодаря конкуренции за центры участвующие в активации водорода.
Следует также отметить влияние наличия С 4 Н 10 в исходной реакционной смеси на стабильность функционирования Со /Al 2 O 3 /SZ.Из данных представленных на рис 1. видно, что если при превращении н-С 7 Н 16 , катализатор в условиях эксперимента сохраняет стабильность в течении практически 120 минут, то, как при превращении н-С 4 Н 10 :н-С 7 Н 16 к 30 минуте эксперимента катализатор заметно снижает свою активность.
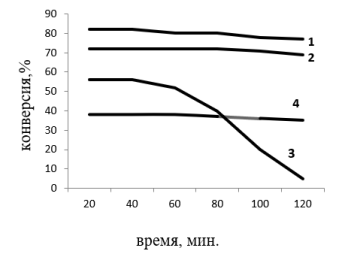
Рис. 1. Влияние продолжительности процесса на стабильность катализатора при Т=180 0
1.н-С 7 Н 16 на Со /Al 2 O 3 /SZ
2.н-С 7 Н 16 на Со / HZSM
3. н-С 4 Н 10 : н-С 7 Н 16 на Со /Al 2 O 3 /SZ
4. н-С 4 Н 10 : н-С 7 Н 16 на Со / HZSM
Замена Со/Al 2 O 3 компонента композиционного катализатора на цеолитный Со/HZSM-5, обладающий высокими кислотными свойствами, не оказывает существенного воздействия на конверсию н — С 4 Н 1О , но повышает выход продуктов диспропорционирования С 3 и С 5 (табл.1). Возможно это связано с вкладом α-расщепления изомеризованного интермедиата С 8 . Повышение гидрокрекирующей активности Со/HZSM-5/SZ приводит к селективности β-расщепления и тем самым понижает выход изо-С 4 Н 10 и повышает выход продуктов диспропорционирования.
Конверсия н-С 7 Н 16 в присутствии Со/HZSM-5/SZ в интервале 140–180 0 заметно ниже (~12 %) по сравнению Со /Al 2 O 3 /SZ.Однако особое внимание вызывает состав образующихся продуктов. Замена Со /Al 2 O 3 на Со/HZSM-5, как следует из данных табл.2, приводит к снижению выхода С 3 -С 4 и повышению выхода С 5 -С 6 алканов. Повышение температуры до 200 0 практически устраняет отмеченные особенности превращения н-С 7 Н 16 в присутствии Со/HZSM-5/SZ.Следовательно замена Со /Al 2 O 3 компонента на Со/HZSM-5 оказывает на механизм превращения н-гептана.
Продукты превращения н-С 7 Н 16 в смеси с н-С 4 Н 10 на Со/HZSM-5/SZ мало отличаются от продуктов аналогичного превращения Со /Al 2 O 3 /SZ. Особый интерес представляет то, что в результате использования цеолитного компонента резко возрастает вовлечённость в процесс н-С 4 Н 10 , конверсия которого превышает конверсию индивидуального н-С 4 Н 10 на обоих SZ содержащих катализаторах. С другой стороны, под воздействием н-С 4 Н 10 конверсия н-С 7 Н 16 на Со/HZSM-5/ SZ также, как на Со /Al 2 O 3 /SZ снижается. Причём зависимость конверсии н-С 7 Н 16 от температуры приобретает более сложный характер, заключающийся в снижении этого параметра с повышением температуры выше 160 0 (табл.4). Аналогичная зависимость от температуры наблюдается выход С 5 -С 6 продуктов превращения смеси н-С 4 Н 10 : н-С 7 Н 16 .
С повышением температуры, при прочих равных условиях, выходу С 3 возрастает, но, как следует из данных представленных в табл.4, при этом в интервале 140–180 0 не только возрастают выхода изо-С 7 продуктов, а также дополнительно фиксируются более высокомолекулярные С 8 парафины.
Таблица 4
Превращение н-С 7 Н 16 : н-С 4 Н 10 (1:1 мол; 0,63:0,37мас) на композиционном катализаторе Со/ HZSM-5 / SZ
|
Температура 0 С |
Распределение продуктов |
|||||||
|
конверсия, % |
селективность, % мас |
|||||||
|
н-С 4 Н 10 |
н-С 7 Н 16 |
н-С 4 Н 10 + нС 7 Н 16 |
С 3 |
С 5 -С 6 |
Изо-С 7 |
С 8 |
||
|
140 |
21,5 |
28,2 |
26,0 |
21,0 |
54,2 |
24,8 |
- |
|
|
160 |
30,6 |
41,0 |
37,2 |
28,2 |
40,6 |
28,6 |
2,6 |
|
|
180 |
43,4 |
36,7 |
39,2 |
19,0 |
36,6 |
39,9 |
4,5 |
|
|
200 |
5,0 |
23,5 |
16,6 |
46,9 |
30,3 |
22,8 |
- |
|
Принимая во внимание высокие значения выходов С 3 на Со/HZSM-5/ SZ по сравнению с Со /Al 2 O 3 /SZ можно с большой вероятностью предположить, что С 3 и С 8 продукты реакции являются результатом гидрорасщепления бимолекулярных интермедиатов [С 4 +С 7 ]. Отсутствие С 8 в продуктах реакции при 140 0 и низкие выхода в интервале температур 160–180 0 могут являться следствием их, как более высокой температуры кипения, так и более высокой реакционной способности. Результатом этих эффектов является монотонный рост конверсии н-С 4 Н 10 в интервале 140–180 0 несмотря на понижение конверсии н-С 7 Н 16 в интервале температур от 160 до 180 0 . Здесь следует отметить, что повышение температуры до 200 0 изменяет характер взаимодействия н-С 4 Н 10 и н-С 7 Н 16 .Резкое снижение конверсии н-С 4 Н 10 при превращении смеси с ростом температуры до 200 0 может быть следствием уменьшения вероятности образования бимолекулярных интермедиатов [С 4 +С 7 ]. Понижение конверсии н-С 7 Н 16 при 200 0 в присутствии н-С 4 Н 10 указывает на сохранение последним способности блокировать гидрорасщепления первого с участием SZ компонента катализатора.
Воздействие н-С 4 Н 10 на превращение н-С 7 Н 16 наиболее сильно проявляется на стабильности функционирования катализатора. Из данных представленных на рис.1 видно, что если превращение н-С 7 Н 16 при 180 0 на Со /Al 2 O 3 /SZ достаточно стабильно в течении 120 мин., то при превращении смеси н-С 4 Н 10 : н-С 7 Н 16 при этих же условиях, катализатор начинает терять активность уже после 30 минуты работы. Использование в составе катализатора цеолитного компонента, как показано на рис.1, приводит к стабилизации превращения н-С 4 Н 10 : н-С 7 Н 16. Причиной дезактивации катализатора является блокирование его активной поверхности углеводородистыми отложениями (УВО). В табл.5 представлены данные, характеризующие накопление УВО на поверхности использованных композиционных каталитических систем при превращении углеводородной смеси н-С 4 Н 10 : н-С 7 Н 16 . Из сопоставления данных, характеризующих стабильность функционирования катализатора (рис.1) с данными табл.5 можно отметить интенсивное накопление УВО при превращении смеси на Со/Al 2 O 3 /SZ уже в первые 30минут функционирования (1,31 %), что соответствует началу ингибирования процесса. Дополнительное накопление УВО (1,51 %) приводит к резкому снижению активности катализатора. В результате замены алюмооксидного компонента на цеолитный, накопление УВО резко сокращается: за 120мин. достигает 1,05 %. Как следует из данных рис.1, образец Со/HZSM-5/ SZ стабилен на протяжении этого времени. Таким образом, наличие кислотного компонента в составе SZ содержащего катализатора, способствует значительному снижению накопления УВО.
Таблица 5
Накопление углеводородистых отложений (УВО)на SZ –содержащих катализаторах при превращении смеси н-С 4 Н 10 : н-С 7 Н 16 (1:1) Т=180 0
|
Катализатор Со/ Al 2 O 3 / SZ |
Время, мин |
УВО |
С |
Н 2 |
|
|
г/г кат |
% |
г/г кат |
г/г кат |
||
|
Со/HZSM-5/ SZ (гептан) |
120 |
0,026 |
0,65 |
0,022 |
0,0035 |
|
Со/Al 2 O 3 /SZ |
30 |
0,052 |
1,31 |
0,045 |
0,007 |
|
60 |
0,060 |
1,51 |
0,051 |
0,009 |
|
|
Со/HZSM-5/ SZ |
30 |
0,020 |
0,50 |
0,017 |
0,0033 |
|
60 |
0,029 |
0,71 |
0,024 |
0,0042 |
|
|
120 |
0,042 |
1,05 |
0,036 |
0,0063 |
|
Для превращения н-С 7 Н 16 на Со/HZSM-5/ SZ характерна высокая стабильность (рис.1) и, соответственно, низкое накопление УВО (табл.5). Из сопоставления данных элементного анализа, представленных в табл.5, следует, что соотношение Н/С содержится в пределах 0,16 -0,18. В пределах ошибки опыта это соотношение может соответствовать формуле (-СН2-) n . Принимая во внимание водородную среду и низкие температуры реакции можно предположить, что УВО представляет собой насыщенные углеводороды, температуры, кипения которых превышают температуру опытов. Следовательно, накопление УВО является следствием образования более высокомолекулярных продуктов в результате взаимодействия н-С 4 Н 10 с С 7+. Поэтому повышение гидрокрекирующей активности катализатора цеолитным компонентом, способствует эффективному расщеплению [С 4 +С 7 ] интермедиата в С 7- продукты и, тем самым стабилизирует процесс, уменьшая накопление УВО.
Таким образом, И-Д превращение смеси н-С 4 Н 10 : н-С 7 Н 16, является следствием синергизма каталитических свойств SZ и Со/HZSM-5 компонентов композиционного катализатора, возникающего в интервале температур 140–180 0 . Для характеристики состояния компонентов Со/HZSM-5/SZ, последний был подвергнут РФ и ИКС анализу.
В табл.6 представлены максимумы интенсивных полос поглощения (п.п.) ИКС композиционных катализаторов и Со/HZSM-5. Как видно из этих данных активный композиционный катализатор содержит набор п. п., входящих в Со/HZSM-5 и SZ. Принимая во внимание, удовлетворительное соответствие п. п., представленных в табл.4, описанным в [13,14] для ИКС ZSM-5 и SZ, можно также предположить отсутствие непосредственного взаимодействия между компонентами Со/HZSM-5/SZ.
Таблица 6
Максимумы полос поглощения ИКС Со/ HZSM-5 / SZ и его компонентов
|
Со/ HZSM-5 / SZ |
3740 |
3660 |
3610 |
1394 |
1061 |
904 |
|
Со/HZSM-5 |
3740 |
3660 |
3610 |
- |
- |
- |
|
Со/Al 2 O 3 /SZ |
- |
- |
1394 |
1061 |
904 |
Из рентгеновской дифрактограммы образца, представленного на рис.2, видно, что образец содержит цеолитную фазу, характерную для структуры ZSM-5 и тетрагональную и моноклинную фазы диоксида циркония.
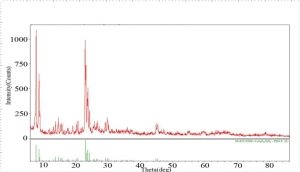
Рис. 2. Рентгеновская дифрактограмма КК С o / Al 2 O 3 / SO 4 - 2 — ZrO 2
Принимая во внимание полученные результаты ИК спектрального анализа, по-видимому, композиционно-каталитическую систему можно рассматривать как псевдо твёрдый раствор HZSM-5-SZ. Такое фазовое состояние было установлено для системы Pt/SZ-Al 2 O 3 [15].
Из представленных выше данных и их интерпретации следует, что исходная активация И-Д превращения н-С 4 Н 10 , н-С 7 Н 16 и их смеси происходит при участии льюисовских кислотных [5,16] или ред-окс [4,6] центров, локализованных на SZ. С другой стороны благодаря цеолитному компоненту, носителю бренстедовских кислотных центров, резко возрастает выход продуктов диспропорционирования промежуточных веществ превращения н-С 4 Н 10 , н-С 7 Н 16 и их смеси. Изменение селективности композиционного катализатора в результате замены Со/Al 2 O 3 на Со/HZSM-5 показывает, что благодаря фазовому состоянию, близкому к состоянию твёрдого раствора, происходит сопряжение центров, расположенных на его различных компонентах. Таким образом эффект сопряжения центров. расположенных на различных носителях предопределяет последующее экспериментальное поведение композиционного катализатора.
Заключение
Совмещение каталитических свойств композиционных катализаторов, компонентами которых являются модифицированный кобальтом цеолит Со/HZSM и SO 4– 2 (2 %) -ZrO 2 приводит к синергетическому эффекту в результате которого превращение смеси н-С 4 Н 10 : н-С 7 Н 16 в отличии от превращения отдельных компонентов протекает преимущественно с образованием С 5 -С 6 алканов.
На композиционном катализаторе Со/HZSM-5/SZ переработка смеси н-С 4 Н 10 : н-С 7 Н 16 при температуре 140–180 0 позволяет конвертировать смесь на уровне 26,0–39,0 %, а также обеспечить конверсию н-С 4 Н 10 от 21,5–43,4 %, н-С 7 Н 16 от 28,2 -36,7 %, где селективность С 5 -С 6 составляет 54,2 и 36,3 %.
Образование С 5 -С 6 является следствием протекания процесса через стадию формирования и изомеризацией промежуточных веществ [С 4 +С 7 ], и их последующим гидрорасщеплением в конечные продукты.
Дальнейшие исследования в этом направлении могут быть основой для разработки технологии, направленное на повышения ресурса С 5 -С 6 алканов, являющихся компонентами современных высокооктановых бензинов.
Литература:
- Ясакова Е. А., Ситдикова А. В., Ахметов А. Ф. Тенденции развития процесса изомеризации в Р оссии и за рубежом // Нефтегазовое дело. 2010. № 1.С.1–19.
- Турукалов М. Полная изомеризация // Нефтегазовая вертикаль. — 2008. –. № 16. — c. 22–28.
- Кузнецов П. Н., Твердохлебов В. П., Кузнецова Л. И., Казбанова А. В., Мельчаков Д. А., Довженко Н. Н. Новые катализаторы на основе диоксида циркония для изомеризации алканов нефтяных фракций.//Journal of Siberian Federal University Engineering and Technologies 4(2011 4).438–452.
- Y.Ono «Asurvey of the mechanism in catalytic izomerization of alkanes. Catalysis Today,2003,81,p-3–16
- Wakayama T., Matsuhashi H. Reaction of linear, branched, and cyclic alkanes catalyzed by Brönsted and Lewis acids on H-mordenite, H-beta, and sulfated zirconia // Journal of Molekular catalysis A: Сhemical. 2005. V. 239. P.32–40
- Абасов С. И., Агаева С. Б., Мамедова М. Т., Тагиев Д. Б., Искендерова А. А., Исаева Е. С., Иманова А. А. Совместная конверсия н-гексана и н-бутана на цирконий — цеолитных катализаторах //Катализ в промышленности. 2015. Т.15. № 4. С. 73–78.
- Абасов С. И., Агаева С. Б., Мамедова М. Т., Исаева Е. С., Иманова А. А., Искендерова А. А., Алиева А. А., Зарбалиев Р. Р., Тагиев Д. Б. Превращение н-гептана, н-бутана и их смеси на каталитических системах Al2O3/WO42-/ZrO2 и HMOR/WO42-/ZrO2 //Журнал прикладной химии. 2018. Т.91. Вып.6. С.838–845.
- Tatsumi T., Matsuhashi H., Arata K. Superacids Based on Zirconium Dioxide // Bull. Chem.Soc. Japan. 1996. V. 69. P. 1191–1194.
- V. Adeeva, G. D. Lei,W. M. H. Sachtler Competitive mechanisms of n-butane isomerization on sulfated zirconia catalysts. Catal.Lett. 1995.33.135
- Suzaki T., Okuhara T. Catal.Lett. Direct evidence of intramolecular rearrangement in skeletal isomerization of n-butane over bifunctional catalysts 2001.72.111
- G.Caeiro., R. H. Carvalho., X.Wang., M. A. N. D. A. Lemos Activation of C2-C4 alkanes over acid and bifunctional zeolite catalysts //Journal of Molekular catalysis A:Chemical. 2006. V. 255. P.131–158.
- Miyaji A, Okuhara T. Skeletal isomerization of n-heptane and hydroisomerization of benzene over bifunctional heteropoly compounds. Catalysis Today 81 (2003) 43–49.
- Kotrel, S., Lunsford, J.H., Knozinger, H. Characterizing Zeolite Acidity by Spectroscopic and Catalytic Means. J. Phys. Chem. B, 105 (2001), 3917–3921.
- Adeeva V, Dehaan JW, Janchen J, Lei GD, Schunemann V, Vandeven LJM, Sachtler WMH, Van Santen RA. Acid sites in sulfated and metal promoted zirconium dioxide catalysts. J Catal, 151 (1995), pp. 364–372
- Казаков М. О., Лавренов А. В., Данилова И. Г., Бельская О. Б., Дуплякин В. К. Гидроизомеризация бензолсодержащих бензиновых фракций на катализаторе Pt/ SO42-/ZrO2-Al2O3. II. Влияние химического состава на кислотные свойства и протекание модельных реакций изомеризации //Кинетика и катализ. 2011. Т 52. № 4. C.583–588.
- Katada N, Endo J, Notsu K, Yasunobu N, Naito N, Niwa M. Superacidity and catalytic activity of sulfated zirconia. Journal of Physical Chemistry. B. Vol.104, No.44, 10321–10328, 2000.







