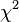Цель работы: изучить фенотипические особенности больных артериальной гипертензией в зависимости от генотипов полиморфного локуса гена ACE (ангиотензин-превращающего фермента) Ins/Del I/D (rs4646994).
Ключевые слова: артериальная гипертония, заболевания сосудов, полиморфизм, генотип.
Введение. Неуклонный рост сердечно-сосудистых заболеваний выдвинул в число важных задач исследование факторов, играющих ведущую роль в развитии и прогрессировании артериальной гипертензии. Рядом авторов особенное внимание среди факторов риска АГ уделяется генетической предрасположенности [Markus ea 2015, Nakata ea 2019].
Ведущим механизмом развития и прогрессирования кардиоваскулярных заболеваний является эндотелиальная дисфункция. Изменения и повреждения сосудистой стенки при артериальной гипертензии возникают значительно раньше клинических проявлений, что вызывает трудности ранней диагностики и оценке прогноза поражения органов-мишеней. Доказано, что в процессах ремоделирования сосудов при артериальной гипертензии важная роль принадлежит нарушению структуры и функции эндотелия, ассоциированным с повышением концентрации окисленных атерогенных липидов, дефицитом оксида азота, повышением эндотелина-1, экспрессией васкулоэндотелиального и трансформирующего факторов роста, высокой степенью выраженности процессов воспаления, гормональными и метаболическими нарушениями. В генезе ангиопатий лежит воздействие многочисленных факторов в том числе: изменения гормонального статуса, оксидативный стресс, нарушение микроциркуляции, гипоксия [Измеров Н. Ф., 2011; Бабанов С. А., 2013]. Многими исследователями подтверждено, что в возникновении и степени поражения органов-мишеней при артериальной гипертензии важную роль играют генетические факторы.
В числе генетических факторов, определяющих развитие и течение АГ, как правило, выступают аллельные варианты генов, кодирующих белки ренин-ангиотензинальдостероновой системы (РААС). Данные гены могут быть ассоциированы с развитием острых цереброваскулярных состояний у больных с артериальной гипертензией.
Наиболее изученным полиморфизмом, играющим важную роль в развитии сосудистых нарушений, в том числе, развитии инфаркта миокарда, является полиморфизм гена ACE, заключающийся в наличии (инсерция, обозначается буквой I) или отсутствии (делеции, обозначается буквой D) Alu-вставки длиной 287 пар оснований в интроне 16. Этот полиморфизм обычно обозначается кодом Alu I/D. Таким образом, возможны три варианта генотипа: II, ID и DD. Носители аллеля D имеют более высокие уровни активности ACE плазмы, в сердечной мышце и в тканях и таким образом, имеют более высокие уровни ангиотензина II. Генотип DD обнаруживается у 28–31 % людей, попадающих в группу риска развития ишемической болезни сердца, инфаркта миокарда, постинфарктных осложнений, инсулинорезистентности и сахарного диабета, артериальной гипертензии и других. Исследование полиморфизма Alu Ins/Del I->D гена ангиотензин-конвертирующего фермента (ACE) имеет прогностическое значение, позволяющее определить риск развития заболеваний сердечно-сосудистой системы.
Ген ACE кодирует аминокислотную последовательность ангиотензин-превращающего фермента (АПФ), который является важным физиологическим регулятором артериального давления и водно-солевого обмена. АПФ превращает циркулирующий в крови неактивный ангиотензин I в ангиотензин II, обладающий мощным гипертензивным действием за счёт влияния на водно-солевой обмен, сердечно-сосудистую и другие системы организма.
Полиморфизм Alu Ins/Del I->D гена ACE имеет два варианта, отличающихся наличием (insertion, I) или отсутствием (deletion, D) Alu-последовательности в интроне гена ACE. С данным полиморфизмом связана различная степень экспрессии гена АСЕ. Суммарная активность АПФ у носителей сочетания D/D аллеля на 30 % выше, чем у лиц с вариантом I/I, что является фактором риска артериальной гипертонии (АГ) и других сердечно-сосудистых заболеваний, в частности ишемической болезни сердца (ИБС).
Данные о связи вариантов полиморфизма Alu Ins/Del I->D гена ACE с риском сердечно-сосудистых заболеваний, полученные в пилотных научных исследованиях. Большое количество работ посвящено изучению риска развития ишемического инсульта у лиц с DD генотипом. В ряде работ [Markus ea 2015, Nakata ea 2019] были найдены ассоциации между DD генотипом и высоким риском развития лакунарных инсультов. В тоже время, многие исследования не установили связи полиморфизма гена АПФ с ишемическим инсультом. В гене АПФ был выявлен инсерционно-делеционный полиморфизм, связанный с инсерцией (I) или делецией (D) Alu повтора размером 287 п.н. в интроне 16 гена АСЕ [Rigat B. et al., 2009]. Данный полиморфизм оказался ассоциирован с уровнем АПФ в плазме крови и наиболее высоким этот уровень оказался у гомозигот по аллелю D [ Tiret L. et al., ]. Было описано 10 новых полиморфных участков в гене АПФ и установлено, что кроме инсерционно-делеционного полиморфизма по крайней мере еще один полиморфный участок ассоциирован с изменениями уровня АПФ в плазме крови. Второй полиморфный сайт, влияющий на уровень АПФ, отвечает за 38 % вариабельности уровня АПФ в плазме крови, до сих пор точно не идентифицирован. Однако установлено, что он расположен в 5' концевой области гена АПФ [ Villard Er. et al., 1996]. Анализ этого сайта мог бы позволить лучше понять вклад гена АПФ в развитие сердечно-сосудистых заболеваний.
Полиморфизм в гене ангиотензинконвертирующего фермента (ACE), связанный с делецией Alu последовательности в интроне 16, встречается у 30 % населения и рассматривается как генетический фактор предрасположенности к инфаркту миокарда.
Впервые положительная статистически значимая ассоциация I/D полиморфизма гена АПФ с ИМ была найдена Cambien F. et al. в исследовании типа случай-контроль [ Cambien ea 2012]. Относительный риск (ОР) развития ИМ для лиц с DD генотипом в общей выборке больных составил 1,34, а в группе лиц с низким числом средовых факторов риска заболевания — 3,2 [ Cambien ea 2015]. Согласно результатам работы, выполненной в рамках программы ECTIM (Etude Cas- Temoin de Infarctus du Myocarde), риск ИМ у пациентов с генотипом DD, имеющих родителей, перенесших ИМ, увеличен в 3 раза по сравнению с таковым у пациентов, у родителей которых не было ИМ [ Tiret ea 2013]. Высокая частота генотипа DD найдена в выборке детей, у которых двое или больше из числа бабушек и дедушек перенесли ИМ, либо умерли от него. Было показано, что у больных ИБС при наличии аллеля D в генотипе риск возникновения ИМ и внезапной смерти от него повышен (в 2,2 раза — для DD генотипа; в 1,8 раза — для ID генотипа) [Evans ea 2014]. В некоторых работах, в частности Zee R. et al. [Zee ea 2014], показано, что распространенность гомозиготности по аллелю D с возрастом значительно уменьшается. На этом основании делается вывод, что DD генотип увеличивает риск преждевременной смерти, поэтому меньшая частота аллеля D в популяциях с высокой продолжительностью жизни и в старших возрастных группах является косвенным подтверждением влияния этого аллеля на риск фатальных сердечно сосудистых заболеваний.
В исследовании Nakai K. et al. была найдена ассоциация между повышенной частотой аллеля D и увеличением числа пораженных сосудов у больных ИБС из Японии [Nakai ea 2010]. При изучении ангиограмм больных ИМ или нестабильной стенокардией отмечена тенденция к увеличению числа стенозов сосудов у пациентов с генотипом DD. Установлена прямая зависимость между DD генотипом и развитием рестенозов после коронарной ангиопластики [Amant ea 2017]. Выявлена ассоциация генотипа II гена АПФ у больных АГ с суточным профилем АД типа нон-диппер, а генотипа DD гена ангиотензинпревращающего фермента (АПФ) — с суточным профилем АД типа диппер. При этом генотип DD ассоциирован с высоким уровнем атерогенных липидов и риском развития атеросклероза. В последних исследованиях показана важная роль ренин ангиотензин альдостероновой системы (РААС) в процессах атерогенеза. Вазоконстрикция и задержка в организме натрия и воды, обусловленная действием ангиотензина II (AT II) и альдостерона, активируют атерогенез. В настоящее время, согласно данным экспериментальных и клинических исследований, AT II рассматривается как медиатор воспаления, который непосредственно активирует рост атеросклеротической бляшки и ремоделирование сердца. Кроме того, AT II отрицательно влияет на функцию эндотелия, стимулируя секрецию цитокинов и хемокинов. Доказано, что наличие у больного АГ с суточным профилем типа диппер генотипа DD гена АПФ сочеталось с нормальной вегетативной реактивностью, носительство генотипа II гена АПФ у больных ГБ с суточным профилем АД типа нон-диппер — с гиперсимпатикотоническим типом вегетативной реактивности. Гипертоническая болезнь (ГБ) является одним из главных факторов риска развития мозгового инсульта, ишемической болезни сердца (ИБС), с которыми связано около 50 % всех летальных исходов. По литературным данным, частота полиморфного локуса Ins/Del I/D (rs4646994) гена ACE (ангиотензинпревращаюшего фермента) в общей популяции составляет 15–20 %, у больных АГ от 30 % до 40 %.
Вышеизложенные положения определили цель и задачи настоящего исследования.
Задачи исследования:
1. Изучить клинические особенности АГ в зависимости от варианта носительства аллеля гена ACE (ангиотензин-превращающего фермента).
2. Исследовать частоту вариантов СПАД у различных генотипов полиморфного локуса Ins/Del I/D (rs4646994) гена ACE (ангиотензин-превращающего фермента) у больных АГ
3. Оценить частоту генотипов полиморфного локуса Ins/Del I/D (rs4646994) гена ACE (ангиотензин-превращающего фермента) у больных АГ в сочетании с ишемической болезнью сердца и условно здоровых лиц.
4. Исследовать показатели окислительного метаболизма липидов, маркеров ишемии и ремоделирования миокарда при различных генотипах полиморфного локуса Ins/Del I/D (rs4646994) гена ACE у больных АГ
5. Разработать дополнительные критерии риска раннего развития поражения органов-мишеней и оптимизировать лечение различных фенотипов больных АГ в зависимости от генотипа полиморфного локуса гена ACE (ангиотензин-превращающего фермента) Ins/Del I/D (rs4646994)
Специальные методы исследования
Всем пациентам проводилось комплексное обследование.
Суточное мониторирование артериального давления с использованием портативных мониторов системы АВРМ-02 (Венгрия).
Оценивались следующие показатели:
— суточные индексы времени АД;
— среднее систолическое (САД) и среднее диастолическое АД (ДАД);
— вариабельность САД;
— вариабельность ДАД;
— индекс времени САД и индекс времени ДАД;
— суточный индекс САД и ДАД;
— величина и скорость утреннего подъема САД и ДАД.
Метод исследования однонуклеотидных полиморфизмов генов
Определение однонуклеотидных полиморфизмов проводилось на приборе для ПЦР (полимеразной цепной реакции) в реальном времени «АНК-32М» (Россия).Наборы реагентов для определения полиморфного локуса Ins/Del I/D (rs4646994) гена ACE (ангиотензинпревращаюшего фермента), компании Синтол (Россия). Метод: ПЦР в реальном времени.
Для исследования однонуклеотидных полиморфизмовиспользовали венозную кровь. Забор крови проводился в утренние часы (8:00).
Исследование содержания атерогенных липидов, биомаркера дисфункции миокарда натрийуретического пептида NT pro BNP в образцах сыворотки проведено на иммуноферментном 8-канальном планшетном фотометре «Eхреrt Рlus» фирмы «ASYS HITECH» (Австрия), стандартная длина волны измерения 450 н. м. Иммуноферментный анализ «сэндвич» — типа, наборами фирм производителей. Забор крови проводился в утренние часы (8:00).
Методы статистического анализа
Статистическая обработка полученного материала осуществлялась на персональном компьютере с использованием пакета статистических программ Stat Soft Statistica 6.0, 2000. С помощью метода вариационной статистики определялась средняя арифметическая (M), ее ошибка (±m), критерий Стьюдента (t) при различных уровнях значимости (p). Достоверными считались результаты при p<0,01, p<0,05. Анализ данных проводился с помощью статистического пакета программ SPSS 15.0.
Результаты исследования
Результаты исследования свидетельствуют, что обследуемые группы достоверно не различались по полу, возрасту и длительности артериальной гипертензии (в первой группе — 6,9±1,9 года, во второй — 7,1±1,7 года, в третьей — 7,2±1,5 года, четвертой —6,8±2,1). Имели место различия в группах больных в зависимости от генотипа полиморфного локуса Ins/Del I/D (rs4646994) гена ACE (ангиотензин-превращающего фермента) (табл. 1).
Таблица 1
Частота генотипов полиморфного локуса Ins/Del I/D (rs4646994) гена ACE (ангиотензин-превращающего фермента) у больных АГ в сочетании с ишемической болезнью сердца и условно здоровых лиц
|
Исследуемые группы |
Генотипы |
|||||
|
I\I |
I\ D |
D\D |
||||
|
N =39 |
% |
N = 42 |
% |
N = 47 |
% |
|
|
АГ |
8 |
20,5** |
12 |
28,5 |
18 |
38,3** |
|
Ишемическая болезнь сердца |
5 |
12,8** |
8 |
19,0 |
13 |
27,6** |
|
АГ+ ИБС |
4 |
10,2** |
7 |
16,6 |
11 |
23,5** |
|
Условно здоровые лица |
22 |
56,5** |
15 |
35,9 |
5 |
10,6** |
Примечание: **различия достоверны между группами р1 — АГ р2 —ИБС, р3 — АГ + ИБС, р4 — условно здоровые лица, p<0,01, p<0,05
Изучение частоты случаев артериальной гипертензии у лиц с различными генотипами позволило выявить преобладание данного показателя в группах, обследуемых с генотипами I\ D и D\D (табл.1). При этом ишемическая болезнь сердца и сочетание артериальной гипертензией и ИБС, в группе с генотипом D\D встречалась статистически достоверно чаще, чем при генотипах I\I и I\ D (табл. 1). По данным проведенного исследования, среди условно здоровых лиц преобладал генотип I\I (табл. 1).
Исследование встречаемости вариантов суточного профиля артериального давления (СПАД) у больных АГ различных генотипов позволило выявить преобладание неблагоприятных профилей АД «non-dippers» и «night-pickers» у пациентов с генотипом D\D (табл.2). При этом благоприятный суточный профиль АД «dippers» имел место статистически достоверно чаще у обследуемых с генотипом I\I (табл.2).
Таблица 2
Частота вариантов СПАД у различных генотипов полиморфного локуса Ins/Del I/D (rs4646994) гена ACE (ангиотензин-превращающего фермента) у больных АГ
|
Вариант СПАД |
Генотипы |
|||||
|
I\I |
I\ D |
D\D |
||||
|
N = 39 |
% |
N = 42 |
% |
N = 47 |
% |
|
|
«dippers» |
33 |
84,6** |
17 |
40,5 |
18 |
38,3** |
|
«non-dippers» |
3 |
7,6** |
20 |
47,6 |
25 |
53,2** |
|
«over-dippers» |
2 |
5,2** |
4 |
9,5 |
1 |
2,1** |
|
«night-pickers» |
1 |
2,6** |
1 |
2,4 |
3 |
6,4** |
**различия достоверны между генотипами р1 — I\I, р2 — I\ D, р3 — D\D, p<0,01, p<0,05
У всех обследуемых были изучены показатели гемодинамики (систолическое, диастолическое и среднее гемодинамическое артериальное давление). Результаты представлены в таблице 3.
Таблица 3
Средние уровни АД при суточном мониторировании у больных АГ в зависимости от генотипа полиморфного локуса Ins/Del I/D гена ACE (ангиотензин-превращающего фермента)
|
Показатель |
Пациенты с генотипом I \D ( n = 42) |
Пациенты с генотипом D\D ( n =47) |
Пациенты с генотипом I\I ( n = 39) |
p |
|
Систолическое АД, мм. рт. ст. |
151,2 ± 4,2 |
155,3 ± 4,5** |
145,2 ± 2,8 |
p < 0,01 |
|
Диастолическое АД, мм. рт. ст. |
95,3 ± 3,9 |
97,6 ±3,8** |
90,3 ± 2,1 |
p < 0,01 |
|
Среднее гемодинамическое, мм. рт. ст. |
108,4 ± 4,5 |
109,6± 4,8** |
103,2 ± 3,2 |
p < 0,05 |
Примечание: **различия достоверны между группами р1 — I \D р2 — D\D, р3 — I\I, p<0,01, p<0,05
Исследование уровней артериального давления у больных с различными генотипами полиморфного локуса Ins/Del I/D гена ACE позволило выявить следующие особенности. Так, во всех группах больных АГ имело место изменение параметров центральной гемодинамики. Показано статистически достоверное (p<0,01, p<0,05) повышение систолического, диастолического, среднего гемодинамического давления, особенно у пациентов с генотипом D\D и больных АГ, являющихся носителем генотипа I\D. При этом данные величины статистически (p<0,01, p<0,05) достоверно отличались от значений группы с генотипом I\I, где имели место наиболее низкие показатели систолического, диастолического, среднего гемодинамического давления.
Изучение окислительного метаболизма липидов маркеров и ишемии миокарда у пациентов с АГ и различными генотипами полиморфного локуса Ins/Del I/D (rs4646994) гена ACE выявило статистически достоверные различия, представленные в таблице 4.
Таблица 4
Характеристика показателей окислительного метаболизма липидов, маркеров ишемии миокарда при различных генотипах полиморфного локуса Ins/Del I/D (rs4646994) гена ACE у больных АГ
|
Показатели |
Генотипы |
I\I — D\D |
|||
|
I\I |
I\ D |
D\D |
p |
|
|
|
ЛПНП-ХС, ммоль\л |
3,25 ±01** |
3,51 ± 0,3 |
3,92 ± 0,2** |
0,032 |
7,649 |
|
ЛПОНП-ХС, ммоль\л |
0,57 ± 0,06** |
0,69±0,05 |
0,96±0,04** |
0,016 |
8,854 |
|
Натрийуретический пептид NT pro BNP, нг / мл |
0,075 ± 0,03** |
0,096± 0,05 |
0,119± 0,03** |
0,002 |
9,327 |
**различия достоверны между генотипами р1 — I\I, р2 — I\ D, р3 — D\D, p<0,01, p<0,05
Так, наиболее высокий уровень атерогенных липидов имел место у носителей генотипа D\D (табл.4), кроме того, у пациентов данной группы были статистически достоверно более высокие показатели маркера ишемии миокарда натрийуретического пептида NT pro BNP (табл. 4). У больных АГ, имеющих генотип I\ D, значения окислительного метаболизма липидов были статистически достоверно выше данных пациентов, имеющих генотип I\I (табл. 4).
Выводы:
- Артериальная гипертензия у пациентов, являющимися носителями генотипа D\D полиморфного локуса Ins/Del I/D гена ангиотензин-превращающего фермента характеризуется преобладанием суточного профиля АД «non-dipper» и «night-pickers»;
- Для пациентов с артериальной гипертензией и генотипом D\D полиморфного локуса Ins/Del I/D гена ангиотензин-превращающего фермента характерно повышение показателей окислительного метаболизма липидов и маркеров ишемии миокарда;
- Установлена прямая зависимость между DD генотипом полиморфного локуса Ins/Del I/D гена ангиотензин-превращающего фермента и частотой развития артериальной гипертензии и ишемической болезни сердца.
Практические рекомендации
- В целях ранней диагностики риска артериальной гипертензии важное клиническое значение имеет определение генотипа полиморфного локуса Ins/Del I/D гена ангиотензин-превращающего фермента;
- С целью ранней диагностики поражения органов-мишеней при артериальной гипертензии у пациентов с генотипами D\D и I\ D полиморфного локуса Ins/Del I/D гена ангиотензин-превращающего фермента, практическое значение имеет определение показателей окислительного метаболизма липидов и маркеров ишемии миокарда;
- Исследование генотипов полиморфного локуса Ins/Del I/D гена ангиотензин-превращающего фермента может иметь значение для ранней коррекции выявленных изменений центральной гемодинамики у носителей генотипов D\D и I\ D и снижения риска развития ишемической болезни сердца.
Литература :
- Адельшина, Г. А. Генетика в задачах. Учебное пособие / Г. А. Адельшина, Ф. К. Адельшин. — М.: Планета, 2015. — 176 c.;
- Ауэрбах, Ш. Генетика / Ш. Ауэрбах. — М.: Атомиздат, 2012. — 320 c.
- Ефремова, В. В. Генетика / В. В. Ефремова, Ю. Т. Аистова. — М.: Феникс, 2010. — 256 c.;
- Лильин, Е. Т. Генетика для врачей / Е. Т. Лильин, Е. А. Богомазов, П. Б. Гофман-Кадошников. — М.: СПб: Питер,2002. — 256 c.
- Эфроимсон, В. П. Введение в медицинскую генетику: моногр. / В. П. Эфроимсон. — М.: Государственное издательство медицинской литературы, 1990 . — 492 c.;
- Wang T. J. Impact of obesity on plasma natriuretic peptide levels / T. J. Wang, M. G. Larson, D. Levy [et al.]. — Circulation. — 2011. — Vol. 109. — P. 594–600.;
- Whaley-Connell A. Mineralocorticoid Receptor Antagonism Attenuates glomerular Filtration barrier Remodeling in the transgenic Ren2 rat / A. Whaley-Connell, J. Habibi, Y. Wei [et al.]. — Am. J. Physiol. Renal Physiol. — 2009. — Vol. 296 (5). — P. F1013–F1022.;
- Windhausen F. Invasive versus Conservative Treatment in Unstable coronary Syndromes investigators. N-terminal pro-brain natriuretic peptide for additional risk stratification in patients with non-ST-elevation acute coronary syndrome and elevated troponin T: an invasive versus conservative treatment in unstable coronary syndromes (ICTUS) sub-study / F. Windhausen, A. Hirsch, G. T. Sanders [et al.]. — Am. Heart. J. — 2007. — Vol. 153. — P. 485–492.;
- Witt B. J. The incidence of ischemic stroke in chronic heart failure: a meta-analysis / B. J. Witt, A. S. Gami, K. V. Ballman [et al.] // J. Card. Fail. —2007. — Vol. 13, № 6. — P. 489–496.;
- Wood P. An appreciation of mitral stenosis. Part 2. Investigations and results / P. Wood. — Br. Med. J. — 2011. — Vol. 1, № 4871. — P. 1113–1024.;
- World Health Organization. Global status report on noncommunicable diseases 2010. — Geneva: World Health Organization, 2011;
- Yanes L. L. Testosterone-dependent hypertension and upregulation of intrarenal angiotensinogen in Dahl salt-sensitive rats / L. L. Yanes, J. C. Sartori-Valinotti, R. Iliescu [et al.]. — Am. J. Physiol. Renal Physiol. — 2009. — Vol. 296. — P. F771–F779.