Одним из главных факторов интенсификации агрохимического комплекса является его химизация, в первую очередь, широкое применение и эффективность использования минеральных удобрений.
Основной ассортимент азотных удобрений, производимых в нашей Республике, составляют аммиачная селитра, карбамид и сульфат аммония. Эти удобрения относятся к физиологически кислым и многолетнее их применение привело к искусственному закислению миллионов гектар сельскохозяйственных площадей, что отрицательно влияет на повышение урожайности сельскохозяйственных культур.
На основе многолетних физиологических и биохимических исследований установлено, что возникаемая при засолении почв физиологическая недостаточность кальция является одним из важнейших факторов, лимитирующих солеустойчивость хлопчатника. Поэтому развитие производств минеральных удобрений на базе собственных сырьевых ресурсов, особенно кальцийсодержащих и щелочных видов, как цианамид кальция и другие, приобретает важное значение для выращивания хлопчатника в условиях засоленных почв и ограниченности водных ресурсов.
Азот из цианамида кальция более эффективно усваивается растениями, т. к. он является медленнодействующим удобрением. Так, например, растворимость цианамида кальция в воде в 70 раз меньше, чем аммиачной селитры. При внесении под зяблевую вспашку, он предпочтительнее всех других форм азотных туков. Помимо удобрительного эффекта, выявлено его стерилизующее действие на вредную микрофлору почвы.
Цианамид кальция и его производные являются дефолиантами мягкого действия. В отличие от других дефолиантов, он относительно быстро теряет свои токсические свойства, разлагаясь в течение 48–72 часов.
Промышленная переработка цианамида кальция дает ряд ценных продуктов для различных отраслей промышленности, в том числе и для золотодобывающей.
Однако производство подобных удобрений, как цианамид кальция, у нас в Республике не создано, и этот вопрос сохраняет свою актуальность до настоящего времени. В процессе синтеза цианамида кальция воздействием газовой смесью аммиака и диоксида углерода на оксид кальция важное значение имеет изучение вопроса о потери относительно дорогостоящего исходного компонента — аммиака за счет термического разложения и побочной реакции взаимодействия аммиака и диоксида углерода.
В связи с этим был выполнен ряд термодинамических расчетов на основе относительно новых физико-химических констант для следующих химических реакций:
2NH3=N2+3H2(1)
СО2+2NH3=CH4+H2O+N2+0,5O2(2)
CO2+2NH3 =C+N2+2H2O+H2(3)
Тепловой эффект реакции (1) в интервале температур 373–1473 К оказался эндотермичным и эндотермичность системы с повышением температуры возрастала, а абсолютное значение теплового эффекта, наоборот, уменьшалось и при 1073 К величина теплового эффекта реакции была равна — 56598,10 Дж/моль.
Значение десятичного логарифма константы равновесия при температуре 373 К было отрицательно по знаку, а при температуре 458 К (+1850С) — равно нулю. С повышением температуры наблюдался небольшой рост величины десятичного логарифма константы равновесия, а при 1073 К она составляет +3,4285.
Величина изменения энергии Гиббса при 373 К имеет положительный знак и в дальнейшем с ростом температуры абсолютное значение этой величины уменьшается. Начиная с температуры 458 К (+1850С), величина изменения энергии Гиббса приобретает отрицательный знак. Это означает, что начиная с данной температуры процесс термического разложения аммиака термодинамически осуществим, хотя на практике это зависит от ряда технологических и кинетических факторов.
Величина изменения энергии Гиббса при температуре 1073 К, являющаяся оптимальной в процессе синтеза цианамида кальция из извести, аммиака и диоксида углерода, составляла 70433,87 Дж/моль.
Сравнение результатов термодинамических расчетов по старым и новым константам показало, что абсолютные значения теплового эффекта и логарифма константы равновесия, рассчитанные по новым константам, оказались меньшими, а изменения энергии Гиббса — большими, нежели при использовании старых констант. Термодинамические параметры, рассчитанные по новым и старым константам различались на 1 %. Температура начала разложения аммиака по старым физико-химическим константам оказалась 456 К (+1830С), а по новым — 458 К (+1850С).
Тепловой эффект реакции (2) между аммиаком и диоксидом углерода в температурном интервале 873–1473 К был эндотермичным. С повышением температуры эндотермичность системы незначительно уменьшается. При 1073 К тепловой эффект реакции равен — 168395,67 Дж/моль.
Значения десятичного логарифма константы равновесия реакции в интервале температур 873–1473 К имели отрицательные знаки, причем эта отрицательность с повышением температуры уменьшается, а абсолютные значения логарифма константы равновесия увеличивались и при 1073 К достигают величины — 9,851.
Величины изменения энергии Гиббса в изученном интервале температур оказались положительными по знаку, что означает термодинамическую невероятность осуществления реакции. С повышением температуры величина изменения энергии Гиббса увеличивается незначительно и при 1073 К становится равной +202383,94 Дж/моль.
Выполненные термодинамические расчеты показывают, что протекание исследуемой реакции (2) термодинамически маловероятно.
При получении цианамида кальция бескарбидным методом, образование в его составе свободного углерода или сажи имеет отрицательные последствия при его применении и получении из него производных. Поэтому нами были проведены термодинамические расчеты вероятности образования свободного углерода по реакции (3) из исходной газовой смеси со стехиометрическим соотношением в температурном интервале 873–1373 К с шагом 100 К.
Значения теплового эффекта для реакции вычисляли в соответствии с законом Гесса при постоянном давлении для стандартных условий. В результате проведенных расчетов установлено, что энтальпия ΔН0298 = 9444,12 Дж/моль. Это указывает на эндотермичность исследуемой реакции в стандартных условиях.
Изменение энтропии (ΔS0298) вышеприведенной реакции составляло 444,68 Дж/моль* град. Следовательно, исследуемая реакция является обратимой.
Расчет изменения энергии Гиббса (ΔG0298) показал, что оно равно 123064,00 Дж/моль. Полученный результат показывает термодинамическую вероятность реакции. Однако, проведенные нами в стандартных условиях экспериментальные исследования не подтвердили данный вывод и в связи с этим было решено в последующих термодинамических расчетах изучать реакцию при высоких температурах. Для этого, пользуясь уравнением Кирхгоффа, выводили зависимость теплоемкости от температуры. На основании этой зависимости были произведены расчеты термодинамических параметров реакции в зависимости от температуры.
Во всем изученном температурном интервале (873–1373 К) тепловые эффекты реакции оказались эндотермичными. С увеличением температуры до 1173 К тепловые эффекты реакции уменьшались, а выше указанной температуры — несколько увеличивались.
В дальнейших расчетах были определены значения изменения энергии Гиббса. Полученные данные показывают, что абсолютные значения изменения энергии Гиббса с повышением температуры уменьшаются. Из этого следует, что в температурном интервале 873–1373 К с термодинамической точки зрения протекание исследуемой реакции невозможно.
Принципиальная технологическая схема, результаты опытных испытаний и расчет себестоимости производства цианамида кальция из извести, аммиака и экспанзерного газа.
На рис. 1. представлена разработанная принципиальная технологическая схема получения цианамида кальция.
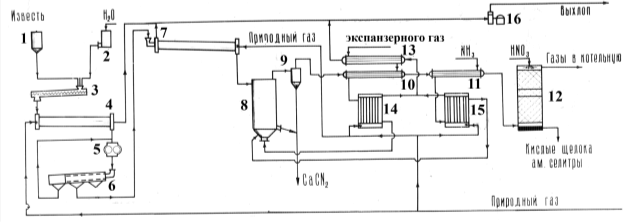
Рис. 1. Принципиальная технологическая схема производства цианамида кальция
Исходная известь, измельченная до фракции меньше 0,25 мм, из бункера (1) в необходимом количестве поступает в гранулятор-затворитель (3), куда одновременно поступает вода из сборника (2) с получением массы с соотношением Т:Ж=1:1,5. Далее затворенная шихта подвергается сушке в сушилке (4) топочными газами и поступает в дробилку (5). После измельчения шихта подается в цилиндрические грохоты (6). Здесь исходная шихта разделяется на три фракции. Мелкая фракция поступает в бункер (1) извести и далее в гранулятор-затворитель (3); крупная фракция вновь возвращается на дробление (5), а фракция размером 1–3 мм, поступает в подогреватель шихты (7), где она подогревается до оптимальной температуры синтеза цианамида кальция. После этого подогретая шихта поступает в реактор синтеза цианамида кальция (8).
В реакторе шихта при температуре 800 oC вступает в химическое взаимодействие с подогретыми экспанзерным газом и аммиаком с образованием цианамида кальция.
Заданная температура в реакторе (8) поддерживается за счет тепла, вносимого экспанзерным газом и аммиаком, предварительно нагреваемых в теплообменниках (9),(10) и подогревателе (12), а затем в нагревателях (13) и (14) за счет сжигания в них природного газа. Нагрев шихты в сушилке (4) производится прямым сжиганием природного газа.
При достижении необходимой степени использования аммиака отходящие газы из реактора (8) получения цианамида кальция с содержанием избытков аммиака, диоксида углерода, а также незначительных количеств азота, водорода, оксида углерода и метана после рекуперации тепла в теплообменниках (9) и (10) поступают в абсорбер (11), где азотной кислотой из них абсорбируется аммиак. Полученный таким образом кислый раствор аммиачной селитры направляется в цех производства аммиачной селитры для донейтрализации газообразным аммиаком.
Избыток азотной кислоты в растворе аммиачной селитры до нейтрализации поддерживается с целью предотвращения поглощения диоксида углерода.
Температура отходящих газов перед абсорбером (11) не должна быть ниже 110 oC, чтобы не образовались солевые отложения в результате кристаллизации карбонатов аммония и не происходила конденсация водяных паров в трубопроводах.
Оставшиеся в газовой фазе азот, водород, метан, а также оксид углерода могут направляться в котельную.
Литература:
- Беглов Б. М. Состояние и перспективы производства и применения минеральных удобрений в Узбекистане// Kimyo va kimyo texnologiyasi.-2003- № 1.- с.8–16.
- Якубов Ш. А., Панжиев О. Х. Синтез цианамида кальция на базе местного сырья и отходов промышленности// Материалы второй Всероссийской научно — технической конференции. Уфа: 2000. — с.128–129.
- Топор Н. Д., Огородова Л. П., Мельчакова Л. В. Термический анализ минералов и неорганических соединений. М.: МГУ. 1987.-270 с.
- Цианамид кальция: тенденции и перспектива международной торговли // Harg Copy Mail Delivery. 2007. — 90 с.







