Большинство клеток высших растений и животных в процессе эволюции не приобрели естественных механизмов адаптации к холоду. В связи с чем, при воздействии низких температур нуждаются в наличии средств «искусственной» защиты. Для сохранения клеток крови, в том числе лейкоцитов, используют большой спектр криофилактиков, которые делят на проникающие и непроникающие. В их число входят вещества различной химической природы. К проникающим в клетку относятся глицерин, диметилсульфоксид – ДМСО, диметилацетамид – ДМАЦ, 1,2-пропандиол – 1,2-ПД. Непроникающие – это поливинилпирролидон – ПВП, полиэтиленоксид – ПЭО-1500 и более высоких молекулярных масс, гидроксиэтилкрахмал – ГЭК. Защитное действие внутриклеточных криофилактиков выражается в том, что, обладая низкой молекулярной массой, эти вещества легко проникают в клетку, связывают воду, способствуют переохлаждению клеток, изменяют кристаллообразование, стимулируя образование преимущественно мелких кристаллов льда при замораживании. Кроме того, являясь хорошими растворителями, они снижают концентрацию солей внутри и вне клеток, этим самым, предохраняя их от обезвоживания и уменьшая повреждение белковых структур клеток. Также эти вещества образуют связи со структурными компонентами мембраны клеток, что ведет к снижению степени ее повреждения при замораживании [1, 2, 6]. Механизм действия непроникающих криопротекторов основан на их способности образовывать прочные связи с внеклеточной водой, замедлять скорость образования кристаллов и изменять их структуру, взаимодействовать с мембраной клеток, следствием чего является повышение ее устойчивости к повреждающему действию кристаллов [2, 5].
На сегодняшний день состав криоконсервирующих растворов весьма вариабелен, так как различные по своей природе клетки по-разному переносят замораживание. Как показывают исследования [9, 10, 11, 14], наилучшие результаты получают при использовании комбинированных, т.е. растворов, содержащих как проникающие, так и непроникающие криопротекторы.
В рамках данной работы изучалась эффективность применения новых хладоограждающих растворов для сохранности морфофункциональных показателей ядерных клеток крови человека, замороженных по экспоненциальной программе и хранившихся при температуре –80°С в течение одних суток.
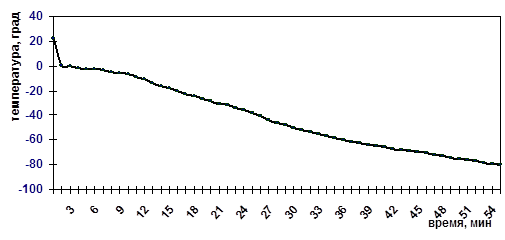 |
Объектом исследования служил концентрат лейкоцитов, выделенный из цельной крови доноров-добровольцев путем цитафереза («Sorvall», США). Для введения ядерных клеток крови в состояние холодового анабиоза –80°С были использованы два хладоограждающих раствора. Ингредиентами первого раствора явились: криопротектор смешанного действия – гексаметиленбистетрагидроксиэтилмочевина, криопротектор проникающего действия – ДМСО и антиоксидант – сукцинат гидроксиметилэтилпиридина. В состав второго раствора вошли следующие ингредиенты: криопротектор проникающего действия – 1,2-ПД, криопротектор непроникающего действия – ГЭК, «реставрирующая» добавка с антигипоксическим действием – «Реамберин». Проведено более 500 тестирований. Среднее количество биообъекта составляло 22,7±6,1 мл. Лейкоциты смешивали в соотношении 1:1 с одним из хладоограждающих растворов в пластикатном контейнере «Компопласт 300» и выдерживали в течение 20 мин при комнатной температуре. Замораживание клеток производили по двухступенчатой экспоненциальной программе (на 1-м этапе со скоростью 10°/мин до точки эвтектики (–4,8°С), на 2-м – 1-2°/мин до температуры –80°С). (Рис. 1)
Рис.1. Экспоненциальная программа замораживания лейкоцитов до –80ºС.
После замораживания объекта до названной температуры контейнеры с клетками переносили в электроморозильник на –80°С («Sanyo», Япония) для хранения. Быстрый отогрев биообъекта производили через одни сутки при замораживании с первым раствором и через одни сутки – со вторым в 20-литровой водяной ванне, нагретой до +38°С, в течение 30-45 сек (в зависимости от объема биообъекта) при интенсивном покачивании контейнера (3-4 раза в секунду) до температуры биообъекта +2 ÷ +4°С.
До замораживания и в первые минуты после отогрева проводили оценку функциональных свойств лейкоцитов. Определяли целостность клеточных мембран по методу Шрека с использованием суправитального красителя эозина [13]; морфологический состав лейкоконцентрата по данным лейкоформулы; степень активации мембраносвязанной NADPН-оксидазы нейтрофилов с помощью регистрации супероксидного анион-радикала в НСТ-тесте [4]; содержание соединений, обеспечивающих микробицидность нейтрофилов без участия кислорода (дефензины, серпроцидины, кателицидин), в гранулах нейтрофилов, с помощью лизосомально-катионного теста (ЛКБ-тест) по методике А.А. Славинского и Г.В. Никитиной [8], содержание Т- и В-лимфоцитов с помощью моноклональных антител; фагоцитарную активность нейтрофилов с использованием инертных частиц латекса [7], а также с помощью регистрации кинетической кривой спонтанной люминолзависимой хемилюминесценции (ЛХЛ) с определением на ней максимальных интенсивностей основных пиков и времени их наступления в секундах. Измерения проводились на биохемилюминометре БХЛ-07 (ЦНИЛ НГМА; «ИМБИО», Россия);
Полученные данные обрабатывали статистически: вычисляли среднее арифметическое значение, среднее квадратичное отклонение. Достоверность различия между показателями оценивали по критерию Уилкоксона. Результаты считали достоверными при p < 0,05 [3].
При замораживании биообъекта с хладоограждающим раствором I (n=12) установлено, что сохранность общего количества лейкоцитов составила 96,8±4,3% (от исходного уровня), жизнеспособность – 90,9±7,1%, количество гранулоцитов – 94,5±6,9%. Сохранность лимфоцитов и моноцитов во всех опытах была равнозначно высокой, что обусловлено хорошей устойчивостью данных видов лейкоцитов к процессам замораживания-отогрева [12]. Количество лизосомально-катионных белков достоверно (p<0,05) не отличалось от исходного уровня. По данным НСТ-теста наблюдалось достоверное (p<0,05) увеличение процента активированных нейтрофилов после отогрева в 4 раза. При изучении субпопуляций лимфоцитов установлено, что количество Т- и В-лимфоцитов в размороженных образцах через одни сутки хранения при –80°С достоверно не изменялось по сравнению с данными до замораживания.
При замораживании биообъекта до –80°С с хладоограждающим раствором II (n=11) установлено, что через одни сутки холодового анабиоза сохранность общего количества лейкоцитов составила 93,7±4,8% (от исходного уровня) с жизнеспособностью 87,0±7,6%. Количество гранулоцитов достоверно снизилось до 68,2±12,7%. Сохранность лимфоцитов и моноцитов во всех опытах была также равнозначно высокой. Кислородзависимая микробицидность нейтрофилов (НСТ-тест) после отогрева увеличивается в 3 раза, а количество лизосомально-катионных белков в нейтрофилах остается на прежнем уровне.
При оценке начальной стадии фагоцитарной активности нейтрофилов (ФАН) показано, что у нативных лейкоцитов первый пик ЛХЛ регистрируется в среднем на 300 сек с максимальной интенсивностью 163,2±51,3 мВ (адгезия клеток), второй пик – в среднем на 500 сек с максимальной интенсивностью 360,5±50,4 мВ (ответ, вызванный опсонизацией, сопровождается повышением уровня метаболической активности). Следующий этап фагоцитоза исследовали по поглощению нейтрофилами инертных частиц латекса. Установлено, что фагоцитарная активность нативных нейтрофилов составляла 62,3±9,7%.
После смешивания и экспонирования лейкоцитов с любым вариантом хладоограждающего раствора регистрируется в большинстве случаев только один пик ЛХЛ, по интенсивности уступающий в 15 раз нативным клеткам.
Через 1 сутки холодового анабиоза при –80°С c применением обоих растворов ЛХЛ лейкоцитов регистрируется в виде одного пика и составляет 3,5±1,1 мВ, что достоверно ниже в сравнении с уровнем до замораживания. Такое резкое падение интенсивности хемилюминесценции обусловлено особенностями компонентов, входящих в состав растворов, в частности, криопротекторов, которые выступают в роли ингибиторов свечения и нарушают цепь реакций активных кислородных метаболитов с люминолом. При оценке ФАН после отогрева наблюдается сохранность 78,1±5,9% (от исходного уровня) клеток с поглощёнными частицами латекса при использовании раствора I, что достоверно (p>0,05) выше данного показателя при использовании раствора II, где их количество составляет 57,3±5,9%.
Таким образом, из двух представленных хладоограждающих растворов лучшими криозащитными свойствами обладает раствор I, позволяющий сохранить на высоком уровне морфофункциональные показатели ядерных клеток крови человека, замороженных по экспоненциальной программе и хранившихся при температуре –80°С в течение одних суток.
Работа выполнена при финансовой поддержке РФФИ, грант 08-04-01423.
Библиографический список:
1. Белоус А.М., Бондаренко В.А. Структурные изменения биологических мембран при охлаждении. Киев: Наукова думка, 1982. – 256 с.
2. Белоус А. М., Грищенко В.И. Криобиология. Киев: Наукова думка, 1994. – 430 с.
3. Гланц С. Медико-биологическая статистика. М.: Практика, 1998. – 459 с.
4. Гольдберг Е.Д., Дыгай А.М., Шахов В.П. Методы культуры ткани в гематологии. Томск: Изд-во Томского гос. ун-та, 1992. – С. 224-226.
5. Гордиенко Е.А., Пушкарь Н.С. Физические основы низкотемпературного консервирования клеточных суспензий. Киев: Наукова думка, 1994. – 143 с.
6. Левин С.В. Структурные изменения клеточных мембран. Л.: Наука, 1976. – 197 с.
7. Потапова С.Г., Хрустиков В.С., Демидова Н.В. и др. Изучение поглотительной способности нейтрофилов крови с использованием инертных частиц латекса // Пробл. гематологии и переливания крови, 1977. – №9. – С. 58-59.
8. Славинский А.А., Никитина Г.В. Цитохимическое выявление катионных белков в гранулоцитах крови амидо-черным 10Б для визуальной оценки и компьютерного анализа изображения // Клиническая лабораторная диагностика, 1999. – №2. – С. 35-37.
9. Celluzzi C.M. Welbon C. A simple cryopreservation method for dendritic cells and cells used in their derivation and functional assessment // Transfusion, 2003. – Apr. 43, №4. – P. 488-494.
10. Crowley J.P., Rene A., Valeri C.R. The recovery, structure, and function of human blood leukocytes after freeze-preservation // Cryobiology, 1974. – Vol. 11. – Р. 395-409.
11. Feldmann C. Einfluß von Kühlrate und Kryoprotektivzusammensetzung auf die durchflußzytometrische Analyse fon Oberflächenantigenen kryokonservierterperipherer hämatopoetischer Progenitorzellen // Hämotology, 2002. – № 28. – S. 90-115.
12. Simon J.D. Recovery of human T- and B-lymphocytes frozen at –80°C / J.D. Simon, M.M. Albala, L.J. Flinton // Cryobiology. – 1975. – Vol. 12., № 6. – P. 536–542.
13. Shreck R. A method for counting the viable cells in normal and malignant cell suspension // Ann. J. Cancer, 1936. – Vol.28 – P.389-391.
14. Stiff P.J., Murgo J.A., Zarolus C.G. Unfractionated human marrow cells cryopreservation using dimethylsulfoxide and hydroxyethyl starch // Cryobiology, 1987. – Vol. 20. – P. 17-24.







