Коррозионное поведение сплава ЛС59–1 в растворе карбоната натрия
Авторы: Харина Галина Валерьяновна, Алешина Людмила Викторовна, Ведерников Алексей Сергеевич
Рубрика: Металлургия
Опубликовано в Техника. Технологии. Инженерия №2 (4) апрель 2017 г.
Дата публикации: 15.03.2017
Статья просмотрена: 484 раза
Библиографическое описание:
Харина, Г. В. Коррозионное поведение сплава ЛС59–1 в растворе карбоната натрия / Г. В. Харина, Л. В. Алешина, А. С. Ведерников. — Текст : непосредственный // Техника. Технологии. Инженерия. — 2017. — № 2 (4). — С. 61-65. — URL: https://moluch.ru/th/8/archive/57/2096/ (дата обращения: 20.04.2024).
Работа посвящена изучению кинетики и механизма коррозионного поведения латуни марки ЛС59–1 в растворе Na2CO3 разной концентрации. Актуальность исследования вызвана необходимостью повышения коррозионной стойкости сплава в реальных условиях. Показано защитное действие цистеина по отношению к сплаву ЛС59–1 в щелочной среде. Приведены результаты инверсионно-вольтамперометрического анализа продуктов коррозии сплава в индивидуальных растворах карбоната натрия и в присутствии цистеина. Особое внимание уделяется рассмотрению селективного механизма коррозионного поведения сплава.
Ключевые слова: латунь, цистеин, селективное растворение, скорость коррозии, коррозионная стойкость, продукты коррозии
Литейный сплав ЛС59–1 представляет собой многокомпонентную систему, содержащую кроме меди (57–60 мас. %) и цинка (37,05–42,2 мас. %) свинец (0,8–1,9 мас. %). Введение свинца в медно-цинковый сплав способствует улучшению некоторых физических и химических свойств последнего. Известно [1], что свинцовые латуни относятся к числу довольно хороших конструкционных материалов в связи с присущими им такими свойствами, как низкая ударная вязкость, пластичность, высокая твердость и стойкость к истиранию, низкая прочность на изгиб, хорошая обработка резанием и др. Установлено [2], что латунь ЛС59–1 обладает достаточно высокой коррозионной стойкостью в различных средах: морская и пресная вода, атмосфера сухих газов-окислителей, органические растворители. Вместе с тем анализ литературных данных показал, что влияние щелочной среды на характер коррозионного разрушения латуни изучен недостаточно полно. В этой связи цель настоящей работы заключалась в изучении кинетики и механизма коррозии сплава ЛС59–1 в растворе карбоната натрия и определение ингибирующего эффекта цистеина в указанном растворе.
Реактивы, материалы, оборудование. Образцы латуни ЛС59–1 были получены литьем под давлением в индукционной тигельной печи с графитовой футеровкой. После тщательной шлифовки и полировки образцы сплава были взвешены на аналитических весах CY-124C и погружены в растворы объемом 100 см3 следующего состава: 1) Na2CO3 5 мас. %, 2) Na2CO3 10 мас. %, 3) 5 %-ный раствор Na2CO3, содержащий 0,2 мас. % цистеина.
По рассчитанным значениям массового показателя коррозии К (![]() , г/см2*ч), были построены кинетические зависимости коррозионного процесса К = f(). Для анализа продуктов коррозии сплава ЛС59–1 был выбран инверсионно-вольтамперометрический метод, основанный на предварительном концентрировании ионов металла из раствора с последующей регистрацией тока анодного растворения на анализаторе ИВА-5 (по ТУ 4215–001–05828695–95). При этом величина тока растворения находится в прямо пропорциональной зависимости от содержания ионов металла в анализируемом растворе. При работе на анализаторе ИВА-5 процедуры обработки вольтамперограмм и вычисления результатов анализа предусмотрены программным обеспечением и проводятся автоматически.
, г/см2*ч), были построены кинетические зависимости коррозионного процесса К = f(). Для анализа продуктов коррозии сплава ЛС59–1 был выбран инверсионно-вольтамперометрический метод, основанный на предварительном концентрировании ионов металла из раствора с последующей регистрацией тока анодного растворения на анализаторе ИВА-5 (по ТУ 4215–001–05828695–95). При этом величина тока растворения находится в прямо пропорциональной зависимости от содержания ионов металла в анализируемом растворе. При работе на анализаторе ИВА-5 процедуры обработки вольтамперограмм и вычисления результатов анализа предусмотрены программным обеспечением и проводятся автоматически.
Результаты иобсуждение. Сплав ЛС59–1 содержит, как было сказано выше, от 37,05 до 42,2 мас. % цинка, что соответствует образованию в системе двух фаз: -фазы — твердого раствора замещения цинка в меди, и -фазы — твердого раствора на основе электронного соединения Cu-Zn [3, с.303]. Присутствие в системе такого электроотрицательного элемента, как цинк (Е0Zn(2+)/Zn(0) = — 0,76В), обусловливает его избирательное растворение в агрессивной среде:
Zn — 2e– Zn2+ (1)
При этом медь, как электроположительный компонент сплава, накапливается на поверхности, образуя стабильную, обогащенную этим элементом зону. Согласно [4, с. 34] одним из механизмов селективного растворения сплавов, обогащенных электроположительным компонентом, является нестационарная объемная диффузия обоих элементов в твердой фазе: электроотрицательного — из объема к поверхности сплава; электроположительного — от поверхности вглубь сплава. В связи с ионизацией активного компонента — цинка — в соответствии со схемой (1) поверхностный слой представляет собой мелкопористую фазу, обогащенную труднорастворимым компонентом — медью.
Поскольку раствор карбоната натрия вследствие гидролиза приобретает щелочную среду, функцию деполяризатора в коррозионном процессе выполняет растворенный в такой среде кислород, который будет восстанавливаться на катодных участках сплава:
О2 + 2Н2О + 4е– 4ОН–(2)
Продуктом избирательной коррозии будет гидроксид цинка:
2Zn2+ + О2 + 2Н2О 2Zn(OH)2(3)
В сильно щелочной среде образующийся Zn(OH)2 вследствие амфотерного характера переходит в комплексное соединение:
Zn(OH)2 + 2ОН– [Zn(OH)4]2–(4)
Кинетические зависимости коррозионного процесса сплава ЛС59–1 в растворе Na2CO3 представлены на рис. 1.
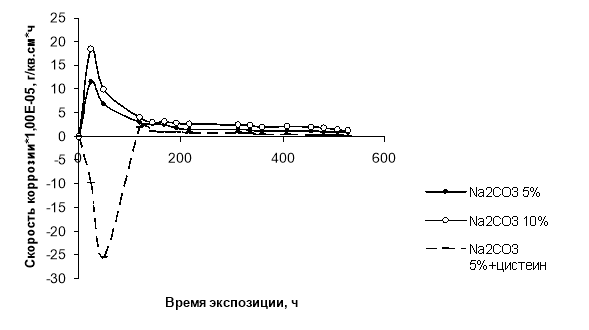
Рис. 1. Скорость коррозии сплава ЛС59–1 в растворах Na2CO3 (5, 10 мас. %) и в 5 %-ном растворе Na2CO3 в присутствии цистеина (0,2 мас. %)
Как видно из рис. 1, скорость коррозии латуни в начальный период времени резко возрастает, что обусловлено преимущественно ионизацией электроактивного компонента; после 120 часов выдержки образцов коррозионный процесс замедляется, и скорость коррозии приобретает постоянные значения. Авторами [5, с. 258] установлено, что в начальный период в поверхностном слое сплава благодаря высокой скорости селективного растворения цинка возникает значительный избыток вакансий по сравнению с объемом сплава. Однако со временем этот избыток уменьшается вследствие диффузии вакансий вглубь сплава, а поверхностных атомов меди — к поверхности сплава.
Молекулярный кислород — довольно сильный окислитель, способный ионизировать некоторый электроположительные металлы, в частности, медь (Е0О2/2Н2О = +1,23 Е0Cu(2+)/Cu(0) = +0,34 В):
Cu0 –2e– Cu2+(5)
Кроме того, переход в раствор меди возможен также и в результате равномерной коррозии сплава, следующей за селективным выщелачиванием более активного компонента при наличии обогащенной электроположительным компонентом зоны на поверхности сплава. В этом случае имеет место процесс послойного стравливания сплава, лимитирующей стадией которого является скорость выхода атомов электроотрицательного компонента на поверхность сплава [4. c. 38]
Из рис. 1 также видно, что с увеличением концентрации Na2CO3 скорость коррозии латуни в области активного растворения возрастает, однако в области пассивации значения массового показателя коррозии не зависят от концентрации ОН–-ионов в коррозионной среде.
С целью повышения коррозионной стойкости сплава ЛС59–1 нами было исследовано ингибирующего действие цистеина, относящегося к группе серосодержащих аминокислот и образующего по аналогии с сульфидами с ионами тяжелых металлов труднорастворимые соединения — цистеинаты:
2R-SH + Zn2+ R-S–Zn–S-R + 2H+(6)
Введение в раствор карбоната натрия цистеина (0,2 мас. %) способствует понижению скорости коррозии как в области активного растворения, более того значения массового показателя коррозии приобретают отрицательные значения. Последнее обусловлено, как было сказано выше, образованием цистеинатов цинка и меди, выполняющих функцию экранирования поверхности образца от агрессивного воздействия коррозионной среды:
2R-SH + Cu2+ R-S–Cu–S-R + 2H+(7)
Для определения содержания ионов цинка и меди в продуктах коррозии был использован инверсионно-вольтамперометрический метод. Массовую концентрацию меди и цинка в растворе определяли методом добавки аттестованного раствора соответствующего металла.
Параметры определения цинка: потенциал предварительного концентрирования –1,4 В; время накопления 60 с. Аналитический сигнал, соответствующий току электрорастворения на анодной вольтамперограмме, регистрировали при потенциале (–1,0) (0,1) B. Параметры определения меди: потенциал предварительного концентрирования –0,8 В; время накопления 180 с; аналитический сигнал регистрировали при — 0,2 (0,1) B [6, с. 40].
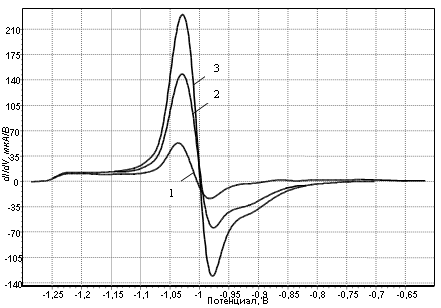
Рис. 2. АИВА цинка: 1 — фон объемом 9,0 мл: 0.1 моль/дм3 СH3COONa + 0.35 моль/дм3 NaCl; 2 — исследуемая проба объемом 1,0 мл (продукты коррозии сплава ЛС59–1 в 5 %-ном растворе Na2CO3); 3 — стандартная добавка ионов цинка 50 мкг/л.
На рис. 2 представлены дифференциальные анодные инверсионные вольтамперограммы (АИВА) цинка. Как видно из рис. 2, на АИВА введение аликвоты пробы в раствор фонового электролита (кривая 1) приводит к росту аналитического сигнала при потенциале –1,03 В (кривая 2). В присутствии добавки стандартного раствора ионов цинка отмечается дальнейший прирост АС (кривая 3), что свидетельствует о наличии в растворе ионов цинка.
Оценка степени селективности коррозионного разрушения сплава была проведена по коэффициенту селективного растворения [4, с.28]:
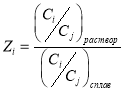 (8)
(8)
Ci — концентрация i-компонента; Cj — концентрация j-компонента.
Результаты инверсионно-вольтамперометрического анализа продуктов коррозии латуни, а также коэффициенты селективного растворения сплава приведены в таблице 1.
Таблица 1
Содержание цинка имеди впродуктах коррозии сплава ЛС59–1 икоэффициенты селективного растворения компонентов сплава
|
Коррозионная среда |
Содержание, мг/л |
Отношение содержания компонентов всплаве |
Коэффициент селективности растворения цинка |
Коэффициент селективности растворения меди |
||
|
Zn2+ |
Cu2+ |
Zn/Cu |
Cu/Zn |
ZZn |
ZCu |
|
|
5 %-ный раствор Na2CO3 |
10,28 |
3,69 |
0.69 |
1.44 |
4,01 |
0,25 |
|
10 %-ный раствор Na2CO3 |
17,81 |
5,36 |
4,78 |
0,21 |
||
|
5 %-ный раствор Na2CO3 + цистеин 0,2мас. % |
6,15 |
2,12 |
4,17 |
0,24 |
||
Из таблицы 1 следует, что значения коэффициента селективности цинка для всех использованных коррозионных сред многократно превышает таковой для меди, что свидетельствует о преимущественном растворении цинка. Несколько большее значение коэффициента селективности цинка найдено для сплава в 10 %-ном растворе Na2CO3, что обусловлено более активным его выщелачиванием из сплава.
Таким образом, литейный сплав ЛС59–1 в растворе карбоната натрия корродирует по селективному механизму с преимущественным выщелачиванием цинка, как более электроотрицательного металла. Обнаружено, что цистеин обладает достаточно высоким ингибирующим эффектом по отношению к латуни ЛС59–1 в щелочной среде за счет экранирования поверхности сплава образующимися труднорастворимыми цистеинатами цинка и меди. Результаты кинетических исследований коррозионных процессов латуни ЛС59–1 хорошо согласуются с полученными данными инверсионно-вольтамперометрического анализа.
Литература:
- Латунь ЛС59–1. [Электронный ресурс] Режим доступа: http://cu-prum.ru/latun/ls59–1.html. (Дата обращения 24.02.2017).
- Латунь — обработка, свойства, коррозия. [Электронный ресурс] Режим доступа: http://ls59.ru/publ/1–1-0–3. (Дата обращения 24.02.2017).
- Власов В. С. Металловедение. Учебное пособие. М.: Альфа-М. Инфра-М. 2015. 332 с.
- Маршаков И. К., Введенский А. В., Кондрашин В. Ю., Боков Г. А. Анодное растворение и селективная коррозия сплавов. В.: Воронежский университет, 1988. 208 с.
- Ситников А. Д., Пчельников А. П., Маршаков И. К., Лосев В. В. Закономерности обесцинкования латуней при анодной поляризации в хлоридных растворах. Защита металлов, 1978. № 14. С. 258–262.
- Белышева Г. М., Малахова Н. А., Алешина Л. В., Стенина Л. Э. Инверсионный вольтамперометрический анализатор «ИВА-ЗАК». Аналитика и контроль.1996. № 3–4. С.40–45.
Ключевые слова
латунь, скорость коррозии, коррозионная стойкость, цистеин, селективное растворение, продукты коррозииПохожие статьи
Исследование возможности использования солей нафтеновых...
щелочная среда, R-S, S-R, поверхность сплава, раствор карбоната натрия, раствор, аналитический сигнал... Защитные свойства консервационных масел и ингибиторов...
Получение и исследование свойств новых полупроводниковых...
Коррозионное поведение сплава ЛС59–1 в растворе карбоната...
Основные термины (генерируются автоматически): щелочная среда, R-S, S-R, поверхность сплава, раствор карбоната натрия, раствор...
Ингибирование коррозии стали 20Л в хлоридсодержащих средах
Коррозионное поведение сплава ЛС59–1 в растворе карбоната... Показано защитное действие цистеина по отношению к сплаву ЛС59–1 в щелочной среде. Ключевые слова: латунь, цистеин, селективное растворение, скорость коррозии, коррозионная стойкость, продукты коррозии.
Утилизация отхода производства каустической соды с получением...
Поскольку раствор карбоната натрия вследствие гидролиза приобретает щелочную среду, функцию деполяризатора в. Продуктом избирательной коррозии будет гидроксид цинка.
Коррозионное поведение сплава ЛС59–1 в растворе карбоната...
Технология получения ферратов, предусматривающая...
Согласно модифицированному варианту [10], к щелочному раствору гипохлорита натрия просто добавляли твердый нитрат железа(Ш), процесс проводили при 25–30°С с добавлением твердого гидроксида калия.
Научные основы определения рН консервов для разработки...
Важна также его презумпция о недопустимости количественной интерпретации измеренных значений рН, если только среда не является разбавленным водным раствором простых веществ [7, с. 42].
Коррозия углеродистой стали в 30-процентном растворе...
коррозионный процесс, скорость коррозии, продукт коррозии, металл, результат коррозии, поверхность металла, окружающая среда, коррозия, коррозионная среда, корродирующий металл. Коррозионное поведение сплава ЛС59–1 в растворе карбоната...
Химия варки древних стекол на зольной шихте | Статья в журнале...
Коррозионное поведение сплава ЛС59–1 в растворе карбоната... Введение в раствор карбоната натрия цистеина (0,2 мас. %) способствует понижению скорости коррозии как в области активного растворения...
Разновидности соды
Определение среды (рН) растворов карбоната, гидрокарбоната и гидроксида натрия. На универсальный индикатор наносим растворы карбоната, гидрокарбоната и гидроксида натрия.
Похожие статьи
Исследование возможности использования солей нафтеновых...
щелочная среда, R-S, S-R, поверхность сплава, раствор карбоната натрия, раствор, аналитический сигнал... Защитные свойства консервационных масел и ингибиторов...
Получение и исследование свойств новых полупроводниковых...
Коррозионное поведение сплава ЛС59–1 в растворе карбоната...
Основные термины (генерируются автоматически): щелочная среда, R-S, S-R, поверхность сплава, раствор карбоната натрия, раствор...
Ингибирование коррозии стали 20Л в хлоридсодержащих средах
Коррозионное поведение сплава ЛС59–1 в растворе карбоната... Показано защитное действие цистеина по отношению к сплаву ЛС59–1 в щелочной среде. Ключевые слова: латунь, цистеин, селективное растворение, скорость коррозии, коррозионная стойкость, продукты коррозии.
Утилизация отхода производства каустической соды с получением...
Поскольку раствор карбоната натрия вследствие гидролиза приобретает щелочную среду, функцию деполяризатора в. Продуктом избирательной коррозии будет гидроксид цинка.
Коррозионное поведение сплава ЛС59–1 в растворе карбоната...
Технология получения ферратов, предусматривающая...
Согласно модифицированному варианту [10], к щелочному раствору гипохлорита натрия просто добавляли твердый нитрат железа(Ш), процесс проводили при 25–30°С с добавлением твердого гидроксида калия.
Научные основы определения рН консервов для разработки...
Важна также его презумпция о недопустимости количественной интерпретации измеренных значений рН, если только среда не является разбавленным водным раствором простых веществ [7, с. 42].
Коррозия углеродистой стали в 30-процентном растворе...
коррозионный процесс, скорость коррозии, продукт коррозии, металл, результат коррозии, поверхность металла, окружающая среда, коррозия, коррозионная среда, корродирующий металл. Коррозионное поведение сплава ЛС59–1 в растворе карбоната...
Химия варки древних стекол на зольной шихте | Статья в журнале...
Коррозионное поведение сплава ЛС59–1 в растворе карбоната... Введение в раствор карбоната натрия цистеина (0,2 мас. %) способствует понижению скорости коррозии как в области активного растворения...
Разновидности соды
Определение среды (рН) растворов карбоната, гидрокарбоната и гидроксида натрия. На универсальный индикатор наносим растворы карбоната, гидрокарбоната и гидроксида натрия.







