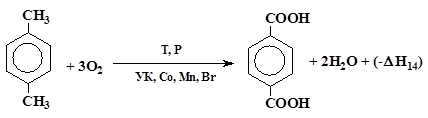Значение и получение терефталевой кислоты
Автор: Хатмуллина Диана Данисовна
Рубрика: 14. Общие вопросы технических наук
Опубликовано в
Дата публикации: 19.09.2013
Статья просмотрена: 13630 раз
Библиографическое описание:
Хатмуллина, Д. Д. Значение и получение терефталевой кислоты / Д. Д. Хатмуллина. — Текст : непосредственный // Технические науки: традиции и инновации : материалы II Междунар. науч. конф. (г. Челябинск, октябрь 2013 г.). — Т. 0. — Челябинск : Два комсомольца, 2013. — С. 86-88. — URL: https://moluch.ru/conf/tech/archive/87/3632/ (дата обращения: 25.04.2024).
Полимерные материалы и среди них химические волокна настоятельно входят в быт человека. До начала XX столетия применялись только те из них, которые являлись продуктами растительного и животного происхождения (хлопок, шерсть, лубяные волокна и т. д.). С появлением синтетических волокон последние стали быстро вытеснять натуральные волокна.
Важнейшими мономерами для производства полиэфирных волокон являются терефталевая кислота (ТФК) и диметилтерефталат (ДМТ).
Терефталевая кислота является одним из важнейших химических продуктов, используемых для производства полиэфирных волокон, полиоксадиазолов, полибензимидазолов, алкидных смол. Терефталевая кислота обладает большой прочностью, относительно высокой термостойкостью, а также высокие диэлектрические характеристики,которые позволяют применять полиэфирные материалы для производства шинного корда, транспортерных лент, приводных ремней, парусов, пожарных рукавов, электроизоляционных и других материалов. Из полиэфирных волокон (лавсан, терилен, дакрон) можно получать разнообразные материалы — длинный ворс, напоминающий мех, подходит для пошива пальто, курток, ковриков для ванной или мягких игрушек, а грубое прочное волокно пригодно для изготовления клиновых ремней, пожарных рукавов и ковровых покрытий.
Благодаря высокой устойчивости к сминанию и способности сохранять форму, хорошему внешнему виду и достаточно низкой стоимости полиэфирные волокна в чистом виде или в смеси с другими волокнами используют для изготовления широкого ассортимента товаров народного потребления: платяной и костюмной тканей, верхнего трикотажа, занавесей, постельного белья, изделий из искусственной замши и искусственного меха.
Приведенные выше свойства полиэфирных волокон обусловили наиболее крупнотоннажное производство по сравнению с производством волокон других видов.
Терефталевая кислота (1,4-бензолдикарбоновая кислота, п-фталевая кислота) является основным исходным продуктом для получения полиэтилентерефталата (ПЭТФ), гранулят которого в свою очередь используется для производства искусственного волокна, пластиковых бутылок, пленки, пластмассы.
Сырьем для производства терефталевой кислоты могут служить разные п-диалкилбензолы: п-ксилол, п-цимол, п-диэтил- и п-диизопропилбензол, а в последнее время применяется также толуол. Из окислителей наибольшее значение имеют азотная кислота и молекулярный кислород.
Из n-диалкилбензолов лучшим сырьем для окисления в терефталевую кислоту является п-ксилол. Он более доступен и, кроме того, при жидкофазном окислении п-ксилола молекулярным кислородом образуется преимущественно п-толуиловая кислота, для дальнейшего окисления которой требуется менее жесткие условия, чем для окисления промежуточных продуктов, образуемых другими n-диалкилбензолами.
В связи с развитием нефтехимической промышленности и значительным увеличением производства п-ксилола в известной степени утратили свое практическое значение способы получения диметилтерефталат (ДМТ) из толуола и п-цимола. Все большее значение приобретают процессы, позволяющие получать ТФК методом жидкофазного каталитического окисления п-ксилола с последующей ее этерификацией метанолом до ДМТ.
Процесс получения органической кислоты (терефталевой), далее технической терефталевой кислоты (ТФК) основан на реакции жидкофазного окисления параксилола (PX) кислородом воздуха в среде реакционного растворителя (RQ). В качестве катализатора используется раствор смеси кобальта (II) уксуснокислого 4‑водный и марганца (II) уксуснокислого 4-водный с добавлением промотора в виде тетрабромэтана (ТБЭ).
Брутто-реакция образования ТФК описывается схемой (1):
|
|
(1)
Тепловой эффект реакции Qp = (-∆Hр) = 326 ккал/г-моль.
Процесс проводят при температуре 185÷195°С под давлением 0,9÷1,1 МПа. Теплосъем — за счет испарения реакционного растворителя (уксусной кислоты) и реакционной воды, то есть процесс осуществляется «на кипу» при температуре, определяемой давлением (упругостью паров воды и уксусной кислоты с учетом наличия в паровой фазе инертов).
Механизм реакции — радикально-цепной с короткой цепью. Упрощенно реакцию можно рассматривать как последовательно-параллельную:
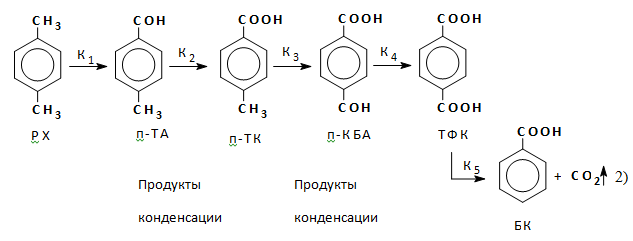
где РХ — параксилол, С6Н4 (СН3)2,
п-ТА — пара-толуиловый альдегид, п-С6Н4(CH3)СОН,
п-ТК — пара-толуиловая кислота, п-С6Н4(CH3)СООН,
п-КБА — пара-карбоксибензальдегид, п-С6Н4(СОН)СООН,
ТФК — терефталевая кислота, п-С6Н4(СООН)2,
БК — бензойная кислота, С6Н5СООН,
Кi — константа скорости I стадии реакций окисления.
Кроме образования бензойной кислоты и продуктов конденсации, основной побочной реакцией является деструктивное окисление уксусной кислоты и образование метилацетата (МА):
|
СН3СООН + 2О2 |
® |
2СО2 + 2Н2O |
(3) |
|
2СН3СООН + 3О2 |
® |
2СО2 + 2СО + 4Н2O |
(4) |
|
2СН3СООН + ½О2 |
® |
СН3СООСН3 + Н2O +СО2 |
(5) |
|
2Со(СН3СОО)3 |
® |
2Со(СН3СОО)2 + СН3СООСН3 + СО2 |
(6) |
Значение констант скоростей последовательных реакций по схеме (2), при равных значениях концентраций реагирующих компонентов, располагаются в следующей последовательности:
К2>К4>>K1>>К3 (7)
Как видно из зависимости (7), лимитирующей стадией реакции является окисление п-ТК в п-КБА, поэтому процедура оптимизации процесса окисления, в конечном итоге, должна быть направлена на обеспечение благоприятных условий для увеличения скорости реакции К3.
На процесс окисления параксилола оказывают влияние различные факторы:
1. Влияние катализатора
Увеличение концентрации катализатора и промотора существенно повышает общую скорость процесса.
Оптимальная комбинация кобальта (II) уксуснокислого 4-водного, марганца (II) уксуснокислого4-водного, тетрабромэтан ускоряет лимитирующую стадию процесса, позволяя уменьшить температуру реакции и улучшить качество ТФК, особенно по цвету.
2. Влияние температуры и давления
Температура процесса поддерживается посредством регулирования давления в реакторе окисления сбросом абгазов в систему очистки. Повышение температуры в области 180÷230°С ускоряет процесс окисления, повышая конверсию параксилола, что уменьшает содержание примесей в ТФК. Но с ускорением скорости основного процесса повышение температуры увеличивает скорость побочных процессов деструкции уксусной кислоты, параксилола и промежуточных продуктов окисления с образованием СО2 + СО. При высоких температурах (200÷230°С) повышение температуры на 10°С увеличивает содержание СО2 + СО в абгазах почти в два раза. В области низких температур (менее 200°С) образование СО2 + СО идет, в основном, за счет разложения уксусной кислоты. При более высокой температуре возрастает доля СО2 + СО, образующихся за счет деструкции параксилола и продуктов его окисления.
3. Влияние концентрации воды в реакционной массе
При высоких концентрациях вода оказывает дезактивирующее влияние на катализатор. Наличие ионов марганца повышает устойчивость каталитической системы к действию воды. Концентрация воды влияет на концентрацию кислорода в паро-газовой фазе и на образование СО2 + СО. Область оптимальных концентраций Н2О, в которой образуется минимальное количество СО2 + СО, лежит в пределах 6÷10,5 % (предпочтительно 8÷10 %), низкое значение Н2О заметно повышает содержание
СО2 + СО.
4. Влияние среднего времени пребывания жидких реагентов (удельной нагрузки по параксилолу)
При увеличении удельной нагрузки по параксилолу среднее время пребывания жидких реагентов τср уменьшается, что приводит к уменьшению конверсии параксилола. При этом в реакционной массе концентрация промежуточных продуктов окисления, в том числе и пара-карбоксибензальдегид, увеличивается, кристаллизация идет при повышенном концентрационном фоне по пара-карбоксибензальдегиду, что приводит к повышению содержания пара-карбоксибензальдегида в ТФК.
Так как τср, или удельная нагрузка по параксилолу, определяет съем ТФК с единицы реакционного объема, то определение оптимального τср является, в основном, экономической задачей — в промышленных условиях τср≈30÷120 минут в зависимости от температуры реакции.
На основании вышеизложенного приводятся оптимальные параметры процесса:
|
– давление в реакторе 1TD‑201, МПа |
0,9÷1,1 (оптимальное — 1,02) |
|
|
– температура в реакторе 1TD‑201, °С |
185÷195 (оптимальное — 186) |
|
|
– соотношение уксусной кислоты к параксилолу |
5÷6/1 (оптимальное — 5,4/1) |
|
|
– время пребывания в реакторе 1TD‑201, минут |
60 |
|
|
– концентрация в исходной реакционной смеси: — катализатора (кобальт (II) уксуснокислого и марганец (II) уксуснокислого), % масс, в пределах |
0,30÷0,40 |
|
|
– тетрабромэтана, % масс, в пределах |
0,08÷0,10 |
|
|
– силиконового масла, ppm, в пределах |
8÷10 |
|
|
– воды, % масс, в пределах |
5÷6 |
|
Похожие статьи
уксусная кислота, кислота, удельная нагрузка, повышение...
Значение и получение терефталевой кислоты | Статья в сборнике... уксусная кислота, кислота, удельная нагрузка, повышение температуры, волокно, реакционный растворитель, реакционная масса, молекулярный кислород, бензойная кислота, время...
Методы улучшения микробиологической безопасности...
уксусная кислота, кислота, удельная нагрузка, повышение температуры, волокно, реакционный растворитель, реакционная масса, молекулярный кислород, бензойная кислота, время пребывания.
Методы получения терефталоилхлорида и пути...
Теплосъем — за счет испарения реакционного растворителя (уксусной кислоты) и реакционной воды, то есть процесс осуществляется «на кипу» при температуре, определяемой давлением...
Изучение коррозии железа в уксусной кислоте в присутствии...
уксусная кислота, комнатная температура, время, мольное соотношение, эффективность коррозии, коррозия, исходная масса, растворившееся железо, железо, экстракт корня чистотела.
Синтез ионных жидкостей с аминосодержащей боковой цепью
После достижения постоянной концентрации уксусной кислоты (о чём свидетельствует
Реакционную смесь фильтруют, упаривают досуха, остаток экстрагируют 3 раза этилацетатом, после чего высушивают в вакууме водоструйного насоса при 70оС, получая ионные жидкости
Синтез пирозолинкарбоксилата, потенциально обладающего...
Малоновую кислоту нужно хорошо растворить с повышением температуры.
Выход кислоты несколько увеличивается, если вместо кипячения нагревать реакционную смесь в течение 2х часов на кипящей водяной бане, и только затем на краткое время (10 мин) довести...
Гомофазная сополимеризация n-фталимидометилметакрилата...
Для оценки изменения реакционной способности мономеров ФИММА и БА в зависимости от природы
стирол, состав сополимера, кислота, эфир, реакция сополимеризации, полярный эффект, состав сополимеров, исходное соотношение мономеров, удельная активность, звено.
«Зеленая химия» в органическом синтезе | Статья в сборнике...
После достижения постоянной концентрации уксусной кислоты (о чём свидетельствует
Реакционную смесь фильтруют, упаривают досуха, остаток экстрагируют 3 раза этилацетатом, после чего высушивают в вакууме водоструйного насоса при 70оС, получая ионные жидкости
Способ переработки биомассы с использованием солнечной энергии
Уксусная кислота.
2. Начальная стадия свето–термораспада гуза – паи, протекающая при температуре от 150 до 270°С. В этот период начинается свето–терморазложение менее термостойких компонентов гуза – паи с выделением реакционной воды, углекислоты, окиси...
Похожие статьи
уксусная кислота, кислота, удельная нагрузка, повышение...
Значение и получение терефталевой кислоты | Статья в сборнике... уксусная кислота, кислота, удельная нагрузка, повышение температуры, волокно, реакционный растворитель, реакционная масса, молекулярный кислород, бензойная кислота, время...
Методы улучшения микробиологической безопасности...
уксусная кислота, кислота, удельная нагрузка, повышение температуры, волокно, реакционный растворитель, реакционная масса, молекулярный кислород, бензойная кислота, время пребывания.
Методы получения терефталоилхлорида и пути...
Теплосъем — за счет испарения реакционного растворителя (уксусной кислоты) и реакционной воды, то есть процесс осуществляется «на кипу» при температуре, определяемой давлением...
Изучение коррозии железа в уксусной кислоте в присутствии...
уксусная кислота, комнатная температура, время, мольное соотношение, эффективность коррозии, коррозия, исходная масса, растворившееся железо, железо, экстракт корня чистотела.
Синтез ионных жидкостей с аминосодержащей боковой цепью
После достижения постоянной концентрации уксусной кислоты (о чём свидетельствует
Реакционную смесь фильтруют, упаривают досуха, остаток экстрагируют 3 раза этилацетатом, после чего высушивают в вакууме водоструйного насоса при 70оС, получая ионные жидкости
Синтез пирозолинкарбоксилата, потенциально обладающего...
Малоновую кислоту нужно хорошо растворить с повышением температуры.
Выход кислоты несколько увеличивается, если вместо кипячения нагревать реакционную смесь в течение 2х часов на кипящей водяной бане, и только затем на краткое время (10 мин) довести...
Гомофазная сополимеризация n-фталимидометилметакрилата...
Для оценки изменения реакционной способности мономеров ФИММА и БА в зависимости от природы
стирол, состав сополимера, кислота, эфир, реакция сополимеризации, полярный эффект, состав сополимеров, исходное соотношение мономеров, удельная активность, звено.
«Зеленая химия» в органическом синтезе | Статья в сборнике...
После достижения постоянной концентрации уксусной кислоты (о чём свидетельствует
Реакционную смесь фильтруют, упаривают досуха, остаток экстрагируют 3 раза этилацетатом, после чего высушивают в вакууме водоструйного насоса при 70оС, получая ионные жидкости
Способ переработки биомассы с использованием солнечной энергии
Уксусная кислота.
2. Начальная стадия свето–термораспада гуза – паи, протекающая при температуре от 150 до 270°С. В этот период начинается свето–терморазложение менее термостойких компонентов гуза – паи с выделением реакционной воды, углекислоты, окиси...