Использование природной железомарганцевой руды в качестве катализатора для получения нанотрубчатого углеродного материала
Авторы: Крылов Игорь Олегович, Юшина Татьяна Ивановна, Дунаева Вера Николаевна, Епихин Андрей Николаевич
Рубрика: 14. Общие вопросы технических наук
Опубликовано в
Дата публикации: 09.10.2014
Статья просмотрена: 158 раз
Библиографическое описание:
Крылов, И. О. Использование природной железомарганцевой руды в качестве катализатора для получения нанотрубчатого углеродного материала / И. О. Крылов, Т. И. Юшина, В. Н. Дунаева, А. Н. Епихин. — Текст : непосредственный // Современные тенденции технических наук : материалы III Междунар. науч. конф. (г. Казань, октябрь 2014 г.). — Казань : Бук, 2014. — С. 84-87. — URL: https://moluch.ru/conf/tech/archive/123/6244/ (дата обращения: 16.04.2024).
В процессе исследования очистки синтез-газа от сероводорода высокотемпературным методом с помощью железомарганцевых руд-сорбентов [1] было установлено, что не все природные руды, содержащие в своем составе соединения железа и марганца, пригодны для целей сероочистки с точки зрения сохранения теплосодержания газов. Причиной этого является протекание побочных реакций взаимодействия восстановительных компонентов синтез-газа с оксидами металлов, содержащихся в руде. Некоторые из этих реакций (например, разложение метана), недопустимые для процесса сероочистки топливных газов, получаемых газификацией угля для использования в парогазовых установках с внутрицикловой газификацией угля (ПГУ с ВЦГ), могут успешно применяться при синтезе метанола и жидких моторных топлив (ЖМТ). Для технологий химического синтеза необходимым условием является объемное соотношение в исходном газе Н2/СО=2, а метан является балластным газом. Процесс разложения метана на углерод и водород с использованием природной железомарганцевой руды марки «П» [1] позволит увеличить процентное содержание в газе водорода, тем самым увеличив выход целевого продукта.
После проведения исследования устойчивости природных сорбентов сероводорода в среде синтез-газа [1] был проведен элементный анализ сорбента «П», проявившего наибольшее влияние на изменение состава синтез-газа. Анализ показал наличие в пробе большого количества углерода (более 30 % масс.), образовавшегося в результате разложения углеродсодержащих соединений газа (СО, СН4). Присутствие углерода в пробах позволили предположить, что при наличии в руде железа и при определенных условиях возможно получение наноструктурного углерода — нанотрубок и нановолокон, а руда, содержащая соединения железа и марганца, может являться катализатором процесса химического осаждения углерода из газовой фазы с образованием такого углерода. Такой метод имеет еще одно название — пиролиз углеродсодержащих газов на синтетических катализаторах, содержащих металлы группы железа [2,3].
Для проверки этой гипотезы были проведены опыты по каталитическому пиролизу метана на руде марки «П» из газовой смеси следующего состава (% об.): СО (25,75); Н2 (15,83); СН4 (31,55); N2 (26,87).
Эксперименты проводились на установке, ранее использовавшейся для изучения протекания побочных реакций в плотном слое сорбента сероочистки, модернизированной системой генерации водорода для предварительного восстановления руды катализатора. После проведения предварительного восстановления водородом газовая смесь, имитирующая синтез-газ, из баллона через редуктор подавалась в реактор, заполненный исследуемым материалом, который разогревался до заданной температуры электропечью. Выходящий из реактора газ проходил через фильтр и направлялся на хроматографический анализ, для определения концентраций Н2, СН4, СО. Расход газа перед реактором определялся с помощью электронного газового расходомера, а расход газа на выходе после измерения состава — газовыми часами ГСБ-400. Отходящий синтез-газ сбрасывался в вытяжную систему.
Перед загрузкой в реактор на аналитических весах взвешивался исследуемый материал и мелкодробленый кварц для организации подложки в реакторе и для распределения газа.
Восстановление материала водородом осуществлялось при повышении температуры от 300 °С до температуры опыта, лежащей в интервале 750–880 °С; при этом скорость нагрева составляла около 10 °С в минуту. После завершения подачи водорода на восстановленный катализатор подавался исходным синтез-газ из баллона. Опыт проводился в течение 2–3 часов и более и заканчивался при стабилизации состава выходной смеси из реактора. После этого в течение часа при температуре 300–400 °С проводилась азотная пассивация материала во избежание вспышки металлического пирофорного железа.
Для исследований было отобрано 4 образца руды-катализатора марки «П» с различным содержанием железа (от 3 до 19 % масс.) и марганца (от 13 до 42 % масс.), а также содержащих SiO2, Al2O3, MgO, K2O, CaO, TiO2, P2O5, Na2O.
Увеличение содержания целевого катализатора (Fe) в материале приводит к интенсификации процесса и увеличивает степень разложения метана, однако при содержании железа в пробе 5,56 % масс. наблюдается повышение степени разложения по сравнению с материалом с несколько большим (9,25 % масс.) содержанием железа. Это может быть объяснено влиянием на процесс разложения метана не только железа, но и марганца.
Марганец является промотором в процессе разложения метана и отвечает за стабильность активности катализатора (Fe), а также, скорее всего, выступает в качестве самостоятельного катализатора [4].
При исследовании результатов влияния температуры на процесс разложения метана для руды, содержащей 18,9 % масс. железа видно, что при 750 °С процесс практически не идет, при 780°С протекает с малой интенсивностью (около 45 %). Повышение температуры до 800 °С и более дает существенное увеличение степени разложения метана до 90–95 %. Степени разложения метана, полученные при температурах 850 и 880 °С приблизительно одинаковы (около 96 %), однако при температуре 880 °С степень разложения достигается гораздо быстрее.
Логарифмическая зависимость константы равновесия, которая рассчитывалась по степени разложения метана, достигнутой при наступлении состояния равновесия, имеет линейную зависимость от обратной температуры проведения процесса.
Для проверки наличия в пробах, полученных после проведения процесса каталитического пиролиза метана, углеродных нанотрубок был применен метод просвечивающей электронной микроскопии (ПЭМ) для двух образцов руды-катализатора с содержанием железа 18,9 % масс., полученных при 800 °С и 850 °С.
Результаты элементного анализа пробы, полученной в опыте при температуре 800 ºС представлены в таблице 1.
Таблица 1
Результаты элементного анализа образца, полученного после разложения метана на руде-катализаторе при температуре 800 ºС
|
Элемент |
Содержание по массе, % |
|
C |
32,24 ± 0,91 |
|
O |
10,4 ± 0,61 |
|
Fe |
34,29 ± 0,89 |
|
Mn |
17,01 ± 0,62 |
|
Si |
3,08 ± 0,26 |
|
Al |
1,22 ± 0,9 |
|
V |
0,99 ± 0,22 |
|
P |
0,55 ± 0,21 |
|
F |
0,19 ± 0,86 |
Результаты элементного анализа пробы, полученной в опыте при температуре 800 °С доказывают присутствие значительного количества углерода в исходном катализаторе (около 32 % от общей массы материла). Были получены углеродные трубки диаметром около 4–8 нм шарообразных частиц графита. В пробе присутствуют как однослойные углеродные нанотрубки (ОУНТ), так и многослойные углеродные нанотрубки (МУНТ), а также цепочки связанных межу собой углеродных трубок.
Спектр образца, полученного разложением метана из модельного синтез-газа при 850 0С, представлен на рисунке 1. На рисунке 2 — его микрофотографии.
Анализ спектральной характеристики показал (рис.1), что углеродный пик сильно выражен по сравнению с пиками железа и марганца, что свидетельствует о большой доле углерода в образце, полученном при 850 ºС.
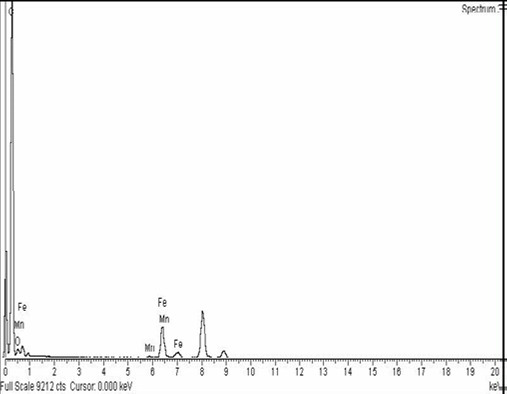
Рис. 1. Спектральная характеристика продукта реакции разложения метана на руде-катализаторе П-4 при 850 ºС

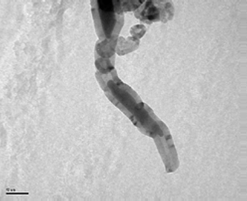
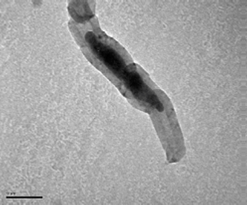
Рис. 2. Электронные микрофотографии полученных углеродных структур для образца, полученного при 850 ºС
Таким образом, результаты исследований подтвердили образование на катализаторе природного происхождения высококачественного углеродного наноструктурированного материала, который может быть пригоден для различных целей (композиционные материалы, электроника, оптика, адсорбенты, водородная энергетика и др. [2,3,5]).
Литература:
1. Перспективы использования природных железомарганцевых сорбентов H2S для высокотемпературной очистки синтез-газа /А. Н. Епихин, И. О. Крылов, А. А.Сомов, С. И. Сучков [и др.] //Электрические станции. — 2012. — № 2. — С. 29–34.
2. Раков Э. Г. Нанотрубки и фуллерены: учебное пособие. — М.: Университетская книга, Логос,2006. — 376 с.
3. Дьячков П. Н. Углеродные нанотрубки: строение, свойства, применения. — М.: БИНОМ. Лаборатория знаний, 2006–293 с.
4. Ткачев А. Г. Разработка технологии и оборудования для промышленного производства наноструктурных материалов: автореф. дис. д.т.н. — Тамбов, 2008. — 34 с.
5. Захарова И. Б. Молекулярная электроника и углеродные наноструктуры. — СПб.: Издательство Политехнического института, 2008. — 123 с.
Похожие статьи
Способ переработки биомассы с использованием солнечной энергии
разложение метана, процесс разложения метана, содержание железа, масса, расход газа, повышение температуры, газификация угля, элементный анализ пробы, каталитический пиролиз метана...
Изучение и разработка технологии получения водоугольной...
Интенсивность процесса газификации по углю достигает 5 т/(м2·ч) при давлении 1,5 МПа.
Исходя из вышеизложеного разработанная и рекомендуемая принципиальная технологическая схема газификации водоугольной суспензии с целью получения газового топлива — метана...
Перспективы использования бурого угля Ангренского...
Ключевые слова: бурый уголь, квазистационарный тепловой режим, диатермическая оболочка, эффективная теплоемкость, теплопроводность угля, пиролиз, синтез-газ.
В связи, с чем значение процесса газификации снова стало возрастать.
Исследование возможности применения ориентированных...
Катализатором выступало железо, образующееся в результате пиролитического разложения ферроцена.
Основным методом его получения является каталитический пиролиз. Суть его состоит в том. (до 60 масс. %), а отмытые в кислоте углеродные нанотрубки (УНТ)...
Эффективность применения пиролизной технологии для...
. Расход тепловой энергии для разложения биомассы (органические отходы) и создания требуемого температурного
mб — масса биомассы, кг; t1 — началная температура биомассы (до переработки), 0С; t2 — конечная температура биомассы (температура пиролиза) 0С
Переработка диоксида углерода с использованием...
Ключевые слова: фотокатализ, диоксид титана, углекислый газ, метан, спектр поглощения.
Дырки влияют на процесс разложения воды: (5).
Аверин И. А., Пронин И. А., Мошников В. А., Димитров Д. Ц., Якушова Н. Д., Карманов А. А., Кузнецова М. В. Анализ каталитических и...
Использование микроволнового излучения в нефтехимии
Марганец является промотором в процессе разложения метана и отвечает за стабильность активности катализатора (Fe), а также, скорее всего, выступает в качестве самостоятельного катализатора [4]. При исследовании результатов влияния температуры на процесс...
К вопросу применения водорода на двигателях внутреннего...
Метан является ценным химическим сырьем, поэтому рассматриваются перспективные способы получения Н2 из воды.
Диффузия водорода в металлы возрастает с повышением температуры. Например, при 1750К в одном объеме железа растворяется до двух объемов...
Окислительная газификация частиц смолисто-сажевого аэрозоля...
Расход плазмообразующего газа— воздуха, нм3/ч. Содержание сажи вотводимом газе, мг/м³.
Способ конверсии метана плазменно-каталитическим окислением и устройство для его осуществления [Текст]: пат.
Похожие статьи
Способ переработки биомассы с использованием солнечной энергии
разложение метана, процесс разложения метана, содержание железа, масса, расход газа, повышение температуры, газификация угля, элементный анализ пробы, каталитический пиролиз метана...
Изучение и разработка технологии получения водоугольной...
Интенсивность процесса газификации по углю достигает 5 т/(м2·ч) при давлении 1,5 МПа.
Исходя из вышеизложеного разработанная и рекомендуемая принципиальная технологическая схема газификации водоугольной суспензии с целью получения газового топлива — метана...
Перспективы использования бурого угля Ангренского...
Ключевые слова: бурый уголь, квазистационарный тепловой режим, диатермическая оболочка, эффективная теплоемкость, теплопроводность угля, пиролиз, синтез-газ.
В связи, с чем значение процесса газификации снова стало возрастать.
Исследование возможности применения ориентированных...
Катализатором выступало железо, образующееся в результате пиролитического разложения ферроцена.
Основным методом его получения является каталитический пиролиз. Суть его состоит в том. (до 60 масс. %), а отмытые в кислоте углеродные нанотрубки (УНТ)...
Эффективность применения пиролизной технологии для...
. Расход тепловой энергии для разложения биомассы (органические отходы) и создания требуемого температурного
mб — масса биомассы, кг; t1 — началная температура биомассы (до переработки), 0С; t2 — конечная температура биомассы (температура пиролиза) 0С
Переработка диоксида углерода с использованием...
Ключевые слова: фотокатализ, диоксид титана, углекислый газ, метан, спектр поглощения.
Дырки влияют на процесс разложения воды: (5).
Аверин И. А., Пронин И. А., Мошников В. А., Димитров Д. Ц., Якушова Н. Д., Карманов А. А., Кузнецова М. В. Анализ каталитических и...
Использование микроволнового излучения в нефтехимии
Марганец является промотором в процессе разложения метана и отвечает за стабильность активности катализатора (Fe), а также, скорее всего, выступает в качестве самостоятельного катализатора [4]. При исследовании результатов влияния температуры на процесс...
К вопросу применения водорода на двигателях внутреннего...
Метан является ценным химическим сырьем, поэтому рассматриваются перспективные способы получения Н2 из воды.
Диффузия водорода в металлы возрастает с повышением температуры. Например, при 1750К в одном объеме железа растворяется до двух объемов...
Окислительная газификация частиц смолисто-сажевого аэрозоля...
Расход плазмообразующего газа— воздуха, нм3/ч. Содержание сажи вотводимом газе, мг/м³.
Способ конверсии метана плазменно-каталитическим окислением и устройство для его осуществления [Текст]: пат.











