Создание и исследование катализаторов на основе солей олеиновой кислоты с ионами d-элементов
Авторы: Алыков Нариман Мирзаевич, Котельникова Мария Николаевна, Тихонова Ксения Сергеевна, Чалышев Сергей Александрович, Алыков Сергей Нариманович
Рубрика: 3. Физическая химия
Опубликовано в
Дата публикации: 03.07.2015
Статья просмотрена: 110 раз
Библиографическое описание:
Создание и исследование катализаторов на основе солей олеиновой кислоты с ионами d-элементов / Н. М. Алыков, М. Н. Котельникова, К. С. Тихонова [и др.]. — Текст : непосредственный // Современная химия: Успехи и достижения : материалы I Междунар. науч. конф. (г. Санкт-Петербург, июль 2015 г.). — Санкт-Петербург : Свое издательство, 2015. — С. 7-12. — URL: https://moluch.ru/conf/chem/archive/122/8480/ (дата обращения: 20.04.2024).
В работе рассмотрены принципы формирования каталитических поверхностей с участием полимерных координационных соединений металлов. Дана оценка взаимодействия частиц в дисперсных системах. В статье описано получение катализаторов на основе солей олеиновой кислоты с ионами d-элементов в области существования жидкокристаллической структуры воды.
Ключевые слова:наночастицы, кластер, катализаторы, полимерные координационные соединения ионов металлов, жидкие кристаллы, диспергированные системы.
В химической, нефтехимической и нефтеперерабатывающей промышленности, а также при очистке газообразных отходов предприятий и выхлопных газов автотранспорта от токсичных веществ широко используют катализаторы на различных носителях (SiO2, α- и γ-Al2O3, цеолитах, оксидах магния и хрома, углеродистых материалах и др.). Для получения эффективного промышленного катализатора необходимо выбрать инертный носитель определенной пористой структуры, нанести на него активный металл или его оксид в виде частиц с заданными составом, размером, структурой и распределить эти частицы по носителю наилучшим образом.
Можно модифицировать носитель с целью создания достаточного количества центров зародышеобразования активных частиц, подбор материалов (носителя и активного компонента), обеспечивающих рост наночастиц благодаря структурному соответствию параметров кристаллических решеток, использование новых носителей с оригинальной геометрией порового пространства и многое другое.
Кластеры с заполненной оболочкой содержат 13(1+12); 55(13+42), 147(55+92), 309(147+162) и т. д. атомов [1]. Повышенную стабильность этим кластерам придает то, что их плотноупакованная структура обеспечивает образование максимального числа связей металл-металл или оксид-металл, или оксид-оксид, тем самым минимальную поверхностную энергию.
Обычно гетерогенный катализатор состоит из материала с высокой площадью поверхности, который служит для катализатора подложкой, и покрывающего ее поверхность слоя собственно катализатора, содержащего активные области типа кислотных центров. Примерами подложек могут быть оксид кремния (SiO2), гамма-оксид алюминия (γ-Al203).
Создание высокоэффективных катализаторов может быть основано на знаниях механизмов формирования кластеров каталитических систем, содержащих различные сочетания активных центров катализатора. Такими являются ионы металлов, имеющие вакантные d-орбитали, к ним можно отнести практически все элементы восьмой группы. Но каталитическая активность этих ионов зависит не столько и не только от количества их в каталитическом пространстве, но также от их взаимного расположения в кластере. Это правило используется для увеличения каталитической активности уже известных катализаторов [2].
Нас интересует формирование каталитических поверхностей, т. е. на поверхностях должны находиться определенным образом сформированные поликоординационые соединения (ПКС) железа, кобальта, никеля, марганца, молибдена, титана и других металлов. Также значительный интерес представляет формирование каталитической поверхности при участии ионов алюминия.
Многие соли не имеют компактного строения и являются координационными высокомолекулярными соединениями, для которых характерны все виды химических связей, например, ковалентные, ионные, координационные. Так известно, что определение молярных масс солей палладия, меди, бериллия, никеля, кобальта, титана и др. приводит к заключению о полимерном строении этих солей [3]
Взаимное расположение ионов в кластере изучалось во многих работах ученых-химиков. Так в [4] было описано формирование полимерных координационных соединений с интересующими нас металлами. Мостиковыми связями могут быть соединены несколько координационных центров. Координационные связи увеличивают число связей между атомами, путем вовлечения большего числа электронов и незаполненных орбиталей. Атомы металлов образуют координационные донорно-акцепторные связи, образуя число связей, превышающих нормальную валентность за счет свободных орбиталей. Неметаллы образуют мостиковые связи, при этом используются неподеленные пары электронов, например -OH, -NH2, -SH, -Cl, -Br и др.
Вместе с тем, в работе [4] рассматривается проблема формирования координационных полимерных соединений в водных и неводных средах. В водных растворах это возможно при определенных значениях рН среды. Начало формирования таких соединений лучше всего оценивать по величинам рН начала гидролиза ионов металлов, которые приведены в [4].
В статье [3] приводится исчерпывающая информация по вопросам формирования координационных полимерных соединений ионов металлов.
Например, гидролиз иона Al3+ был изучен различными авторами, которые подчеркнули присутствие многоядерных комплексов в растворе. В кислой среде образуются ионы состава Al [(OH)5-Al2]x3+x, а в щелочной среде ионы [Al(OH)3]x(OH)-; неизвестно принимает ли x ряд значений или только определенные значения. В кислой среде наиболее вероятно образование комплекса Al6(OH)153+, для которого предполагается циклическое строение.
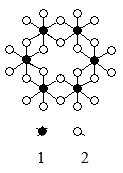
Рис. 1. Строение шестиядерного комплекса Al6(OH)153+ aq. 1- Al, 2- OH или H2O.
Не исключено присутствие в растворе комплексов с большими степенями полимеризации.
Ионы титана в растворе образуют полимерные комплексы вида:
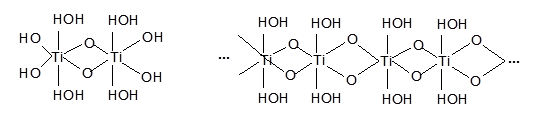
Почти все атомы, интересующих нас металлов, образуют координационные соединения с координационным числом равным 6. Комплексные ионы этих элементов обладают октаэдричексой конфигурацией, т. е. атом металла М окружен шестью аддендами, расположенными в вершинах октаэдра.
Были получены катализаторы из солей олеиновой кислоты, находящейся в форме суспензии в водных растворах на определенно выбранном участке температур [5].
Решение базируется на той основе, что в области температур 4–8оС в воде образуется высоко диспергированные системы солей олеиновой кислоты с ионами металлов. При дальнейшем повышении температуры, дисперсность систем становится меньше, и соли выпадают в осадок. В области температур 4–8оС, в воде, обработанной особым способом присутствуют жидкие кристаллы, т. е. сама вода в этой области состоит в подавляющем количестве из жидких кристаллов [6]. В этих условиях поверхность жидких кристаллов в определенной степени насыщается солями олеиновой кислоты, при этом мицелообразование солей ингибируется плотной сеткой водородных связей поверхности жидких кристаллов. Диспергирование системы, содержащей жидкие кристаллы и соли олеиновой кислоты на холодную поверхность (4–8 оС) сферических, цилиндрических, плоских носителей с последующим высушиванием и прокаливанием, дает возможность получать каталитические системы, в которых поверхность носителя покрыта практически мономолекулярным слоем каталитического компонента.
Были получены катализаторы, представляющие собой пластинки размером 1,0 см2, сферы с диаметром 1 см, цилиндры с диаметром 1,0 и длинной 1,5 см. Носителем являлся оксид алюминия. Образцы катализаторов были испытаны на их активность для окисления парадиметиламиноанилина, при окислении бензальдегида до бензойной кислоты, для окисления пероксида водорода. Активность разработанных катализаторов поясняет таблица 1.
В таблице 1 масса катализатора в виде готового изделия 0,1 г., что составляет молярную концентрацию катализатора на поверхности 10–5 моль/м2, время каталитического действия- 1мин. Каталитический эффект оценивается отношением числа молей субстрата, изменивших свою структуру за 1 секунду к исходному числу молей субстрата (α).
Таблица 1
Результаты испытания катализаторов, полученных по технологии формирования нанокластеров
|
№ |
Катализатор-оксид металла |
Катализируемая реакция |
Каталитическая активность α |
|
1 |
Fe2O3 |
Окисление бензальдегида |
0,95 |
|
2 |
Fe2O3* |
Окисление бензальдегида |
0,10 |
|
3 |
NiO |
Окисление парадиметиламиноальдегида |
0,90 |
|
4 |
NiO* |
Окисление парадиметиламиноальдегида |
0,10 |
|
5 |
CoO |
Окисление пероксида водорода |
0,95 |
|
6 |
CoO* |
Окисление пероксида водорода |
0,05 |
|
7 |
MnO2 |
Окисление пероксида водорода |
0,90 |
|
8 |
MnO2* |
Окисление пероксида водорода |
0,10 |
Формулы без * — предлагаемый катализатор, со * — катализатор промышленный.
Как видно из результатов, приведенных в таблице 1, каталитическая активность новых катализаторов на порядок превосходит активность промышленных катализаторов.
Выводы
Созданы эффективные катализаторы, основой производства которых могут стать реакции образования координационных соединений, солей d-элементов с олеиновой кислотой в области существования жидкокристаллической структуры воды.
Литература:
1. Бухтияров В. И. Металлические наносистемы в катализе [Текст] // Бухтияров В. И., Слинько М. Г. Успехи химии. 2001. Т.70., №.2. С.167.
2. Алыков Н. М. Математическая модель пенообразования растворов, основанная на поляризационных представлениях [Текст] // Алыков Н. М., Котельникова М. Н. Экологические системы и приборы. 2010. №.10. С.28.
3. Хайдук И. Полимерные координационные соединения [Текст] // Хайдук И. Успехи химии. 1961. Т.XXX., вып.9. С.1124–1173.
4. Шарло Г. Методы аналитической химии [Текст] / Шарло Г. М. Химия. 1965. 976с.
5. Котельникова М. Н. Математическое моделирование процессов пенообразования [Текст] / Котельникова М. Н., Алыков Н. М. Инженерная физика. 2010. №.11. С.43.
6. Томилин М. Г. Взаимодействие жидких кристаллов с поверхностью [Текст] / Томилин М. Г. — С.-П. «издательство Политехника». 2001. 322 с.
Ключевые слова
кластер, наночастицы, катализаторы, полимерные координационные соединения ионов металлов, жидкие кристаллы, диспергированные системы., диспергированные системыПохожие статьи
Синтез и исследование каталитической активности ионных...
Обе ионные жидкости следует использовать при температурах до 100 0С, но ТМАГХ-AlCl3 при перегреве показал большую термическую устойчивость, то есть его каталитическая
Наиболее сильное промотирующее действие на активность катализатора 0,86 CaNaY...
Синтез нанопорошков CrMnxFe(1-x) O3 и исследование их...
бензиловый спирт, ромбоэдрическая структура, синтез нанопорошков, реакция окисления, превращение, каталитическая активность, катализатор, жидкая фаза, гусев, JCPDS.
Каталитическое обезвреживание монооксида углерода на...
Изученный катализатор может быть использован в электронных приборах — каталитических преобразователях для контроля загрязнения окружающей среды
На следующих стадиях путём внедрения СО по связям металл-водород образуется формильный лиганд, происходит...
Процесс введения солей никеля и молибдена на...
А ступенчатое удаление хемосорбированной воды, локализованной в различных полостях, для цеолитов типа СаА наиболее интенсивно протекает, в области
При этом, каталитическую активность цеолита можно регулировать подбором его внутри порового объема и состава.
Влияние природы катионов переходных элементов на...
Установлена высокая активность цеолитных катализаторов содержащих два многозарядных
При большей плотности катионов металлов вода удерживается в цеолите прочнее, изменяя
Рис 1. ИК-спектры в области валентных колебаний гидроксильных групп катализаторов: 1-NaY...
Анализ каталитических и адсорбционных свойств...
Целью работы является установление соотношение между каталитической и адсорбционной активностью d-модификатора и
Некоторые авторы отмечают релаксацию приповерхностной области, которая
В этом случае, ион переходного металла будет иметь ту же координацию...
Окисление хиназолонов-4 | Статья в журнале «Молодой ученый»
В отличие от хиназолонов-4 окисление хиназолина в кислой среде перманганатом калия
В качестве оснований используют воду, гидроокиси щелочных металлов, спирт, алкоголяты и
Сильная каталитическая роль кислот в данной реакции заключается в том, что они образуют...
Исследование окислительной активности хлорсодержащих...
Рассмотрены возможные формы существования хлорсодержащих соединений в зависимости от кислотности среды растворов.
В кислой среде разложение идет по следующим реакциям
По данным работ [7,11] активность металлов в качестве катализатора уменьшается в ряду...
Значение и получение терефталевой кислоты | Статья в сборнике...
В области низких температур (менее 200°С) образование СО2 + СО идет, в основном, за счет разложения уксусной кислоты.
Наличие ионов марганца повышает устойчивость каталитической системы к действию воды.
Похожие статьи
Синтез и исследование каталитической активности ионных...
Обе ионные жидкости следует использовать при температурах до 100 0С, но ТМАГХ-AlCl3 при перегреве показал большую термическую устойчивость, то есть его каталитическая
Наиболее сильное промотирующее действие на активность катализатора 0,86 CaNaY...
Синтез нанопорошков CrMnxFe(1-x) O3 и исследование их...
бензиловый спирт, ромбоэдрическая структура, синтез нанопорошков, реакция окисления, превращение, каталитическая активность, катализатор, жидкая фаза, гусев, JCPDS.
Каталитическое обезвреживание монооксида углерода на...
Изученный катализатор может быть использован в электронных приборах — каталитических преобразователях для контроля загрязнения окружающей среды
На следующих стадиях путём внедрения СО по связям металл-водород образуется формильный лиганд, происходит...
Процесс введения солей никеля и молибдена на...
А ступенчатое удаление хемосорбированной воды, локализованной в различных полостях, для цеолитов типа СаА наиболее интенсивно протекает, в области
При этом, каталитическую активность цеолита можно регулировать подбором его внутри порового объема и состава.
Влияние природы катионов переходных элементов на...
Установлена высокая активность цеолитных катализаторов содержащих два многозарядных
При большей плотности катионов металлов вода удерживается в цеолите прочнее, изменяя
Рис 1. ИК-спектры в области валентных колебаний гидроксильных групп катализаторов: 1-NaY...
Анализ каталитических и адсорбционных свойств...
Целью работы является установление соотношение между каталитической и адсорбционной активностью d-модификатора и
Некоторые авторы отмечают релаксацию приповерхностной области, которая
В этом случае, ион переходного металла будет иметь ту же координацию...
Окисление хиназолонов-4 | Статья в журнале «Молодой ученый»
В отличие от хиназолонов-4 окисление хиназолина в кислой среде перманганатом калия
В качестве оснований используют воду, гидроокиси щелочных металлов, спирт, алкоголяты и
Сильная каталитическая роль кислот в данной реакции заключается в том, что они образуют...
Исследование окислительной активности хлорсодержащих...
Рассмотрены возможные формы существования хлорсодержащих соединений в зависимости от кислотности среды растворов.
В кислой среде разложение идет по следующим реакциям
По данным работ [7,11] активность металлов в качестве катализатора уменьшается в ряду...
Значение и получение терефталевой кислоты | Статья в сборнике...
В области низких температур (менее 200°С) образование СО2 + СО идет, в основном, за счет разложения уксусной кислоты.
Наличие ионов марганца повышает устойчивость каталитической системы к действию воды.











