Определение кинетических закономерностей образования твердой фазы сульфида индия (III) в виннокислой системе
Авторы: Туленин Станислав Сергеевич, Марков Вячеслав Филиппович
Рубрика: 3. Физическая химия
Опубликовано в
Дата публикации: 11.03.2015
Статья просмотрена: 54 раза
Библиографическое описание:
Туленин, С. С. Определение кинетических закономерностей образования твердой фазы сульфида индия (III) в виннокислой системе / С. С. Туленин, В. Ф. Марков. — Текст : непосредственный // Современная химия: Успехи и достижения : материалы I Междунар. науч. конф. (г. Санкт-Петербург, июль 2015 г.). — Санкт-Петербург : Свое издательство, 2015. — С. 35-42. — URL: https://moluch.ru/conf/chem/archive/122/7576/ (дата обращения: 19.04.2024).
Исследована кинетика осаждения сульфида индия(III) тиоацетамидом при 333–363 K в условиях самопроизвольного зарождения твердой фазы в объеме раствора.
Ключевые слова: гидрохимический синтез, тонкие пленки, сульфид индия, кинетические закономерности.
На сегодня тонкие пленки сульфида индия нашли широкое применение в области опто- и микроэлектронике в качестве светодиодов, защитных покрытий и материала солнечных элементов. Наиболее эффективным и экономически выгодным методом получения является химическое осаждение из водных сред. Ранее в работе [1] методом гидрохимического осаждения с использованием тиоамида были получены слои сульфида индия(III) толщиной до 700 нм. Однако свойства полученных пленок сильно зависят от параметров проведения эксперимента, поэтому наиболее важным является изучение влияния условий осаждения полупроводникового In2S3.
Кинетику процесса осаждения сульфида индия осуществляли путем отбора проб из раствора. Концентрацию индия определяли комплексонометрическим титрованием согласно общепринятой методике [2] с использованием раствора трилона Б (фиксанал). Титрование проводилось до перехода светло-красной окраски раствора в ярко-желтую. Погрешность объемного комплексонометрического титрования не превышала 0.3 %.
Осаждение сульфида индия проводилось в герметичных реакторах из молибденового стекла в термостатируемых условиях при температурах 333–363 K. Общую реакцию образования сульфида индия при использовании в качестве халькогенизатора тиоамида можно представить так:
2In3+ + 3CSCH3NH2 + 6ОН− = In2S3+ 3H2CN2 + 6H2O, (1)
Кинетическое уравнение образования твердой фазы сульфида любого металла может быть представлено в следующем виде:
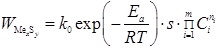
где k0 - предэкспоненциальный множитель, Ea - энергия активации процесса осаждения, R - универсальная газовая постоянная, T - абсолютная температура, s - поверхность твердой фазы, Ci - концентрация по i-ому компоненту, ni - порядок по i-ому компоненту, m - количество компонентов в смеси.
На основе этого полученные результаты экспериментов можно прекрасно интерпретировать с помощью данного математического уравнения с формальными кинетическими порядками по каждому реагенту. В нашем случае, принимая во внимание самопроизвольное зарождении твердой фазы халькогенида [3, 4], скорость осаждения сульфида индия будет описывается уравнением первого порядка:
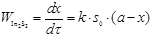
где k - константа скорости реакции; s - поверхность твердой фазы сульфида индия, изменяющаяся во времени и выступающая катализатором; а - начальная концентрация соли в реакционной смеси; х - количество соли индия, перешедшее за время τ в сульфид.
После упрощения вышеприведенное выражение можно выразить через параметр z, который учитывает поверхность зародыша твердой фазы, и тогда получим:
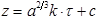
Типичные кинетические кривые превращения соли индия имеют равномерно спадающие кривые характерные для гетерогенных автокаталитических процессов протекающих на границе раздела раствор-подложка. Видно, что твердая фаза сульфида индия образуется практически сразу без индукционного периода. Из-за нестехиометричности по основным компонентам равновесие в системе наступает в различное время от начала процесса.

Рис. 1. Кинетические кривые осаждения In2S3 при различных исходных концентрациях соли индия в растворе. Температура синтеза, K: 353. [In(NO3)3], моль/л - 0.1625 (1), 0.078 (2), 0.052 (3), 0.026 (4), 0.013 (5), 0.004 (6)
Порядок по соли индия определяли графически. Для этого строили зависимость натурального логарифма концентрации соли индия от времени синтеза ln([In(NO3)3]) = f(τ). График в этих координатах дает прямую линию, что подтверждает первый порядок реакции. Порядки реакции по другим компонентам в реакционной смеси находились гарфически после построения соответствующих зависимостей lg(ki) = f(Ci), где Ci — концентрация i-ого компонента реакционной смеси, и нахождения тангенсов углов наклона прямых.

Рис. 2. Кинетические кривые осаждения In2S3 при различных исходных концентрациях тиоацетамида. Температура синтеза, K: 353. [CSCH3NH2], моль/л - 0.02 (1), 0.04 (2), 0.08 (3), 0.14 (4), 0.2 (5)
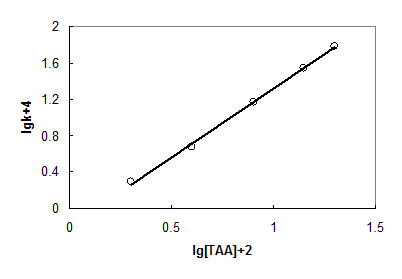
Рис. 3. Определение порядка реакции осаждения сульфида индия по тиоацетамиду. Температура синтеза, K: 353
Используя экспериментально найденные значения x и приведенное выше уравнение, определялись значения z в определенный момент времени τ. Используя значения z,строились графические зависимости z = f(τ), представляющие прямые линии. По тангенсу угла наклона прямых вычислялись константы скоростей реакций k при заданных компонентах реакционной смеси. Так, например, порядок по тиоацетамиду согласно рис. 3 равен 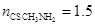 .
.
После обработки кинетических зависимостей, в соответствии с приведенной ранее методикой определения порядков по тиоацетамиду получим, частные порядки реакции осаждения сульфида индия по другим реагентам будут следующими (табл. 1).
Таблица 1
Частные порядки реакции образования In2S3 по реагентам
|
Реагент |
In(NO3)3 |
CSCH3NH2 |
C4H6O6 |
NH2OH∙HCl |
|
n |
1 |
1.5 |
0.13 |
-0.37 |
При изменении температуры синтеза от 333 до 363 K величина индукционного периода уменьшается от 90 до 5 мин. Снижение концентрации индия в растворе до 30 % от исходной проходит соответственно за 540 мин и за 90 мин от начала процесса (рис. 4).

Рис. 4. Кинетические кривые осаждения In2S3 при различных температурах синтеза, K: 333 (1), 343 (2), 353 (3), 363 (4)
Зависимость константы скорости реакции от температуры, описываемая уравнением Аррениуса, позволила вычислить значения энергии активации и предэкспоненциального множителя для изучения процесса. Для нахождения данных величин была использована методика определения частных порядков по реагентам. Для этого строили зависимости рассчитанного параметра z от τ для определения констант скоростей химической реакции с учетом tgβ.
Подставляя необходимые данные для расчета энергии активации и предэспонециального множителя получим:
ΔE = -2.303·R·tgα = -2.303·8.314·(-1.405) = 26.9 кДж/моль.
k0 = 1.18·102 л1.96/c·моль1.96·см2
С учетом рассчитанных значений кинетических порядков по реагентам, энергии активации процесса и предэкспоненциального множителя, формально-кинетическое уравнение скорости образования твердой фазы сульфида индия в условиях самопроизвольного зарождения примет вид:
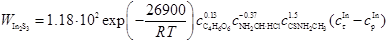
Из полученного уравнения следует, что увеличение концентрации тиоацетамида и температуры реакционной смеси ведет к ускорению процесса осаждения In2S3, а увеличение содержания гидроксиламина солянокислого приводит к замедлению реакции. Сильная зависимость скорости образования сульфида индия от содержания тиоацетамида в растворе объясняется образованием пропорционального количества сероводорода в ходе гидролиза халькогенизатора, который протекает по кислотно-катализируемому механизму. Согласно [5] присутствие ионов металла в растворе при гидрохимическом осаждении, взятых даже в избытке по отношению к концентрации тиоацетамида, не влияет на скорость его гидролиза. Поэтому реакция гидролиза до ацетамида и сероводорода есть реакция первого порядка относительно тиоацетамида и соответственно чем выше концентрация тиоамида в растворе, тем выше концентрация сероводорода и тем быстрее будут связываться свободные ионы индия в сульфид.
Литература:
1. Туленин С. С., Бахтеев С. А., Юсупов Р. А. и др. // ЖФХ. 2013. Т.87. № 10. С.1791.
2. Шварценбах Г., Флашка Г. Комплексонометрическое титрование. М.: Химия, 1970. 360 с.
3. Дельмон Б. Кинетика гетерогенных реакций. М.: Мир, 1972. 554 с.
4. Белова Н. С., Урицкая А. А., Китаев Г. А. // ЖПХ. 2002. Т.75. № 10. С.1598.
5. Swift E. H., Butler E. A. // Anal. Chem. 1956. V.28. P.146.
Ключевые слова
тонкие пленки, гидрохимический синтез, сульфид индия, кинетические закономерностиПохожие статьи
Гидротермальный способ формирования кристаллической фазы...
тонкие пленки, гидрохимический синтез, сульфид индия, кинетические закономерности. Гидротермальный способ формирования кристаллической фазы в тонких пленках сульфида цинка.
Извлечение нефтяных сульфидов и сульфоксидов из...
Кинетику процесса осаждения сульфида индия осуществляли путем отбора проб из раствора. Гидротермальный способ формирования кристаллической фазы в тонких пленках сульфида цинка. Исследование комплексообразования мeди...
Фотоприемники и излучатели на основе халькогенидов свинца
В состав пленки кроме сульфида свинца входят примесные фазы — кислородосодержащие соли свинца. За последние 20–30 лет развитие метода гидрохимического осаждения связано в основном с работами Г. А. Китаева и его учеников [12–14] в Уральском...
Наноструктурирование редкого и рассеянного индия
Некоторые соединения индия (сульфид, селенид, антимонид, фосфид) сами являются полупроводниками; их применяют для изготовления термоэлементов и других
К концу реакции температура смеси достигала 473°К, и наблюдалось присутствие темно-коричневого осадка.
Роль механических примесей и сульфида железа в устойчивости...
Так, например, родственные по своей природе компоненты (тонкодисперсные глины, сульфид железа и др.) являются типичными стабилизаторами водонефтяных
Известно, что сульфид железа содержится не только на оболочках капель воды, но и в объеме нефтяной фазы.
Влияние природы макроциклических колец на скорость транспорта...
Определение кинетических закономерностей образования твердой фазы сульфида индия (III) в виннокислой системе. Исследование радикальной сополимеризации гетероциклических производственных акриловых кислот со стиролом.
Фотокаталитические свойства наноразмерного оксида цинка...
энергетического воздействия на твердое тело.
При анализе дифрактограммы обнаружены следующие фазы: Zn, ZnO, Zn(OH)2, основные рефлексы соответствуют наноразмерному ZnO.
Показана возможность наноструктурирования редкого и рассеянного индия с целью...
Изучение процесса получения цианистого натрия как...
Одним из исходных веществ при синтезе метионина является цианистый натрий.
Реакция поддерживается самостоятельно при температуре от 980°С до 1150 °С.
Реакция сильно экзотермическая, проводится в газовой фазе на катализаторе, которым являются...
Извлечение скандия, тория и РЗЭ фосфиноксидом...
Рис. 3. Зависимость величин коэффициентов распределения (D) Sc, Th, La, Yb от концентрации HNO3 в равновесной водной фазе на фоне 3М Н2SO4.
Сокальский М. А., Сокальская Л. И., Татарников А. В., Утилизация отравляющих веществ и полупродуктов их синтеза: получение...
Исследование структуры пористых материалов по спектрам...
Установлено, что при проведении отжига сульфида свинца наряду с образованием оксидных фаз возможно выделение фазы чистого свинца.
28. Марков В. Ф., Маскаева Л. Н., Иванов П. Н. Гидрохимическое осаждение пленок сульфидов металлов: моделирование и эксперимент.
Похожие статьи
Гидротермальный способ формирования кристаллической фазы...
тонкие пленки, гидрохимический синтез, сульфид индия, кинетические закономерности. Гидротермальный способ формирования кристаллической фазы в тонких пленках сульфида цинка.
Извлечение нефтяных сульфидов и сульфоксидов из...
Кинетику процесса осаждения сульфида индия осуществляли путем отбора проб из раствора. Гидротермальный способ формирования кристаллической фазы в тонких пленках сульфида цинка. Исследование комплексообразования мeди...
Фотоприемники и излучатели на основе халькогенидов свинца
В состав пленки кроме сульфида свинца входят примесные фазы — кислородосодержащие соли свинца. За последние 20–30 лет развитие метода гидрохимического осаждения связано в основном с работами Г. А. Китаева и его учеников [12–14] в Уральском...
Наноструктурирование редкого и рассеянного индия
Некоторые соединения индия (сульфид, селенид, антимонид, фосфид) сами являются полупроводниками; их применяют для изготовления термоэлементов и других
К концу реакции температура смеси достигала 473°К, и наблюдалось присутствие темно-коричневого осадка.
Роль механических примесей и сульфида железа в устойчивости...
Так, например, родственные по своей природе компоненты (тонкодисперсные глины, сульфид железа и др.) являются типичными стабилизаторами водонефтяных
Известно, что сульфид железа содержится не только на оболочках капель воды, но и в объеме нефтяной фазы.
Влияние природы макроциклических колец на скорость транспорта...
Определение кинетических закономерностей образования твердой фазы сульфида индия (III) в виннокислой системе. Исследование радикальной сополимеризации гетероциклических производственных акриловых кислот со стиролом.
Фотокаталитические свойства наноразмерного оксида цинка...
энергетического воздействия на твердое тело.
При анализе дифрактограммы обнаружены следующие фазы: Zn, ZnO, Zn(OH)2, основные рефлексы соответствуют наноразмерному ZnO.
Показана возможность наноструктурирования редкого и рассеянного индия с целью...
Изучение процесса получения цианистого натрия как...
Одним из исходных веществ при синтезе метионина является цианистый натрий.
Реакция поддерживается самостоятельно при температуре от 980°С до 1150 °С.
Реакция сильно экзотермическая, проводится в газовой фазе на катализаторе, которым являются...
Извлечение скандия, тория и РЗЭ фосфиноксидом...
Рис. 3. Зависимость величин коэффициентов распределения (D) Sc, Th, La, Yb от концентрации HNO3 в равновесной водной фазе на фоне 3М Н2SO4.
Сокальский М. А., Сокальская Л. И., Татарников А. В., Утилизация отравляющих веществ и полупродуктов их синтеза: получение...
Исследование структуры пористых материалов по спектрам...
Установлено, что при проведении отжига сульфида свинца наряду с образованием оксидных фаз возможно выделение фазы чистого свинца.
28. Марков В. Ф., Маскаева Л. Н., Иванов П. Н. Гидрохимическое осаждение пленок сульфидов металлов: моделирование и эксперимент.











