Сердечно-сосудистые заболевания занимают ведущее место среди причин смерти лиц пожилого возраста, внезапной смерти. Большинство публикаций посвящено исследованию патологии сердца, меньшее внимание уделяется изменениям крупных кровеносных сосудов, в том числе аорты, приводящим к летальному исходу.
Заболевания аорты делятся на дилатации, аневризмы аорты, атеросклеротические и воспалительные поражения, генетические заболевания (например, синдром Марфана), врожденные аномалии, в том числе коарктация аорты, острый аортальный синдром, включая расслоение (диссекцию) аорты, острые интрамуральные гематомы, пенетрирующие атеросклеротические язвы, травматические повреждения, псевдоаневризмы, разрывы аорты [1]. Международный проект The Global Burden Disease 2010 показал увеличение смертности от аневризм и расслоений аорты с 2,49 на 100 000 до 2,78 на 100 000 человек в период между 1990 и 2010 годами, с более высокими показателями у мужчин [2].
В норме диаметр грудной аорты, измеренный при выполнении эхокардиографии в конце диастолы левого желудочка, колеблется от 2,4 см до 3,7 см, нисходящей грудной аорты — до 2,5 см. Диаметр супраренального отдела брюшной аорты не превышает 2 см [1, 3]. В течение всей жизни отмечается неуклонное увеличение размеров аорты. Диаметр синусов Вальсальвы увеличивается на 0,9 мм у мужчин и на 0,7 мм у женщин каждые 10 лет [1, 3, 4] (рис. 2). Скелетотопия бифуркации аорты зависит от возраста. На протяжении всей жизни отмечается удлинение аорты, что определяет смещение бифуркации в каудальном направлении: от середины IV поясничного позвонка до нижнего края V поясничного позвонка.
Наиболее частой аномалией аорты является дилатация — увеличение диаметра аорты, выходящее за пределы верхней границы нормы для возраста и площади поверхности тела [10].
Согласно директиве Американской ассоциации торакальной хирургии, Американского общества кардиологов под термином «аневризма» следует понимать увеличение диаметра артерии более чем на 50 % по сравнению с нормативным значением диаметра для возраста и площади поверхности тела [5].
Аневризмы аорты могут возникать в любом отделе аорты, однако наиболее уязвимыми сегментами являются восходящая аорта, нисходящая аорта ближе к ligamentum arteriosum и в инфраренальном отделе. Частота аневризм грудного отдела аорты составляет 5,9 случаев на 100000 населения в год. Средний возраст пациентов колеблется от 59 до 69 лет. Мужчины страдают этим заболеванием чаще, чем женщины, соотношение составляет 2:1–4:1 [3].
Различают два морфологических типа аневризмы аорты: мешковидные и веретенообразные аневризмы. При мешковидных аневризмах выпячивается наружу только часть окружности сосудистой стенки. Веретенообразные аневризмы встречаются чаще, в результате диффузного ослабления стенки образуется расширение сосуда во всех направлениях [3] (рис. 1). Стенка аневризмы содержит все три слоя: интиму, медию, адвентицию.

Рис. 1. Схема мешковидной и веретенообразной аневризм грудной аорты [3]
Основной причиной дилатации и аневризмы аорты является атеросклероз. В процесс тяжелого атеросклеротического поражения аорты вовлекается свыше 70 % поверхности аорты у 90 % пациентов [3]. Помимо атеросклероза этиологическими факторами аневризм аорты являются наследственная предрасположенность (семейный синдром аневризмы грудной аорты), генетические заболевания (например, синдром Тернера, синдром Марфана), заболевания соединительной ткани (синдром Элерса-Данлоса IV типа — сосудистый тип), инфекционные заболевания (грибковая инфекция), сифилис, неинфекционный аортит [3].
Атеросклероз — хроническое заболевание, которое характеризуется изменением интимы артерий эластического и мышечно-эластического типа в виде очагового отложения липидов, а также сложных соединений углеводов, элементов крови и циркулирующих в ней макромолекул, образованием соединительной и фиброзной ткани, кальцификацией и сопутствующей трансформацией медии.
Ведущими звеньями развития атеросклероза являются наследственная предрасположенность, обменные, гормональные, гемодинамические нарушения, дисфункция эндотелия, нарушение нервной регуляции сосудистого тонуса, окислительный стресс. К факторам риска атеросклеротического поражения относятся пол (мужской), артериальная гипертензия, активация ренин-ангиотензиновой системы, сахарный диабет, курение, ожирение [6, 7].
Выделяют несколько стадий развития атеросклероза. Долипидная стадия характеризуется повреждением интимы продуктами метаболизма. В стадию липоидоза в сосудистой стенке формируются жировые пятна или полоски. Это наиболее ранние проявления атеросклероза, обнаруживаются у любого человека старше 10 лет, их количество увеличивается до конца жизни [8]. Следующая стадия — липосклероз, характеризуется разрастанием в участках жировых отложений молодой соединительной ткани. Для данной стадии характерно формирование фиброзной атеросклеротической (или атероматозной) бляшки (АСБ) с последующим появлением в ней тонкостенных сосудов. Наиболее подвержены атеросклерозированию участки разветвлений сосудов.
Для стадии атероматоза типично начало осложненных поражений: распад липидных масс, коллагеновых, эластических и гладкомышечных волокон, составляющих центральную часть АСБ с образованием полости, содержащей белково-жировой детрит.
При атерокальцинозе формируется отложение солей кальция в компоненты АСБ, уплотнение ее, что приводит к деформации и сужению просвета артерии, вызывает нарушение кровоснабжения органа. Тромбоз является стадией, с которой начинаются клинические осложнения атеросклероза [8, 9]. Эрозия атеросклеротической бляшки в vasa vasorum может привести к расслоению аорты. Эрозия в адвентицию может обуславливать формирование аневризмы или разрыва аорты, частота разрывов достигает 42 % [11, 12].
Согласно закону Лапласа увеличение напряжения стенки аорты соответствует размеру аневризмы, поэтому большие аневризмы имеют больший риск разрыва. С увеличением размеров аневризмы возрастает скорость их роста: 4,3-кратное увеличение риска разрыва или расслоения аневризмы диаметром 6,0–6,9 см, по сравнению с аневризмой 4,0–4,9 см в диаметре. Темп роста аневризм увеличивается с 0,08 см в год для аневризм ≤ 4,0 см в диаметре до 0,16 см ежегодно для аневризм ≥ 8,0 см в диаметре. У курильщиков и при артериальной гипертензии средние темпы роста аневризмы могут составлять 0,42 см [13].
Расслоение (диссекция) аорты является основным видом осложнений патологии аорты и характеризуется образованием дефекта интимы аорты с последующим ее продольным расслоением в дистальном и, реже, проксимальном направлении и проникновением потока крови в дегенеративно измененный средний слой с образованием двух каналов для кровотока — истинного и ложного [10]. Ложный канал может локализоваться или распространяться вниз вследствие давления крови в нем, часто по спирали. Ведущими факторами риска расслоения аорты являются атеросклероз и артериальная гипертензия. Наибольший риск расслоения существует у пациентов с синдромом Марфана и другими наследственными заболеваниями соединительной ткани, синдромом Тернера, аортитом, сосудистым типом синдрома Элерса-Данлоса [10, 15]. Расслоение аорты более вероятно при существующей аневризме аорты, хотя может возникнуть в отсутствие аневризмы, например, у пациентов с синдромом Марфана [10, 14].
Заболевания аорты в большинстве случаев протекают асимптомно или с неспецифической клинической симптоматикой. Клиническая симптоматика появляется при больших аневризмах, сдавливающих прилежащие органы и ткани, или в случае развития осложнений [1].
Ультразвуковое исследование (УЗИ) аорты является одной из ведущих инструментальных методик диагностики патологии аорты, доступна, воспроизводима, безопасна, не имеет противопоказаний, направлена на получение детальной информации об анатомических характеристиках стенки, просвета сосуда и окружающих тканей в 2D-режиме, а также оценку гемодинамики с применением допплеровских методик.
Цель исследования: изучить сегменты аорты, принятые в ультразвуковой диагностике, основные параметры ультразвукового исследования аорты, ультразвуковые признаки и распространенность приобретенной патологии: атеросклероза, дилатации, аневризм.
Задачи исследования:
1. Провести сравнительный анализ сегментов аорты, принятых в ультразвуковой диагностике, и отделов аорты в анатомии по литературным данным.
2. Изучить ультразвуковые признаки, выраженность, распространенность атеросклеротического поражения, дилатации, аневризм аорты.
Материал и методы. В рамках работы проведено ультразвуковое исследование аорты у 76 пациентов кардиологического профиля в возрасте от 31 до 93 лет, средний возраст пациентов составил 58 лет. Проанализированы сканограммы и протоколы ультразвуковой аортографии, выполненной 263 пациентам, из архива кафедры ультразвуковой диагностики Белорусской медицинской академии последипломного образования (БелМАПО) за 2014 год. Ультразвуковое исследование аорты выполнялось пациентам кардиологического и инфарктных отделений учреждения здравоохранения «1 городская клиническая больница» г. Минска на ультразвуковых аппаратах Toshiba Aplio XG, Voluson 730 Expert.
Результаты и их обсуждение.
В результате изучения данных литературы установлено, что в теоретической и практической медицине есть некоторые различия в определении отделов аорты. Так, анатомически в аорте различают три переходящих друг в друга отдела: восходящую часть, дугу аорты и нисходящую часть, в которой выделяют грудную и брюшную части аорты. Начальный отдел восходящей аорты имеет расширение (луковица аорты) с тремя выпячиваниями — синусами аорты (синусы Вальсальвы). Согласно анатомической классификации восходящий отдел аорты распространяется от аортального кольца до плечеголовного ствола; дуга аорты — от плечеголовного ствола до ligamentum arteriosum; нисходящая аорта — от ligamentum arteriosum до бифуркации аорты. В медицинской литературе, при исследовании генетически детерминированных заболеваний магистральных сосудов синусы Вальсальвы от уровня аортального клапана до синотубулярного перехода называют «корнем аорты». В ультразвуковой диагностике в целях описания анатомических и гемодинамических особенностей патологии выделяют следующие сегменты аорты: аортальное кольцо; синусы Вальсальвы; синотубулярный переход; восходящая аорта; дуга аорты; нисходящая грудная аорта; абдоминальная аорта с супраренальным и инфраренальным отделами (рис. 2). Помимо того, при ультразвуковой диагностике врожденных пороков сердца отдельно осматривается область перешейка аорты, соответствующая переходу дуги в нисходящий отдел аорты, располагающаяся ниже устья левой подключичной артерии, тотчас проксимальнее устья ductus arteriosus, и являющаяся типичным местом локализации коарктации аорты.
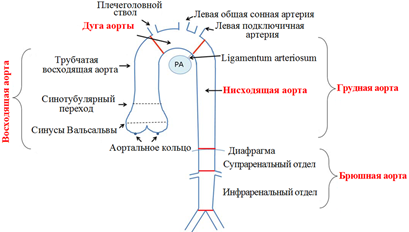
Рис. 2. Схема отделов аорты с позиций нормальной анатомии и ультразвуковой диагностики [1]
Базовым принципом ультразвуковой диагностики заболеваний артериальной сосудистой системы является сопоставление ультразвукового изображения с анатомическими характеристиками артерий:
Геометрия: соответствие хода сосуда анатомическому расположению.
Оценка состояния сосудистой стенки, толщины комплекса интима-медиа (КИМ); равномерное или неравномерное утолщение; эхогенность; отложение солей кальция; ровность внутренней поверхности.
Проходимость сосуда с оценкой состояния просвета, степени стенозирования по диаметру и площади.
Оценка состояния паравазальных тканей для выявления экстравазальной патологии и компрессии, дифференциальной диагностики с патологией, имитирующей сосудистую патологию.
Стенки артерий четко дифференцируются на слои, интима представлена тонкой гиперэхогенной линией, медиа — тонкой гипоэхогенной линией, идентичной по эхогенности просвету неизмененной аорты. Кроме того, нормальная аортальная стенка имеет гладкую, сплошную поверхность. В норме толщина КИМ аорты составляет ≤ 1,0 мм. Любые неравномерные утолщения КИМ ≥ 2 мм считаются атеросклеротическими бляшками [3].
По нашим наблюдениям атеросклеротическое нестенозирующее и стенозирующее поражение аорты имело место у 51 пациента (67 %) (рис. 3), дилатация различных отделов аорты была выявлена у 7 пациентов (9,2 %) со средним возрастом 76,1 год, аневризма восходящего отдела аорты — у одной пациентки 67 лет (1,3 %) (рис. 4). Диагностированная аневризма восходящего отдела аорты имела диаметр 57 мм, наблюдалась умеренная аортальная регургитация III степени. Пациентка с аневризмой аорты была направлена на консультацию к кардиохирургу для решения вопроса о хирургическом лечении. Согласно рекомендациям Европейского общества кардиологов 2014 года операция должна рассматриваться у пациентов без заболеваний соединительной ткани при аневризме восходящей аорты с максимальным диаметром ≥ 55 мм [1].
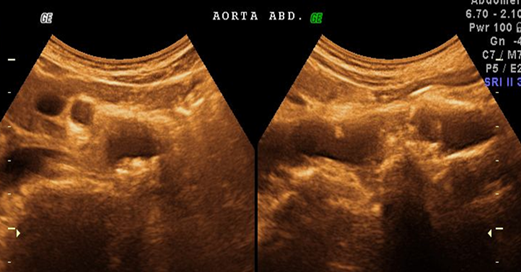
Рис. 3. Атеросклеротическая неоднородная преимущественно гиперэхогенная бляшка инфраренального отдела брюшной аорты с неровной поверхностью, акустической тенью и стенозом просвета аорты 50–60 % по диаметру, поперечный, продольный сканы
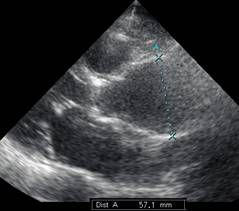
Рис. 4. Пациентка И., 67 лет с аневризмой восходящей аорты диаметром 57 мм, сглаживанием синотубулярного перехода. Парастернальная позиция, длинная ось левого желудочка. Трансторакальная эхокардиография
При анализе ультразвуковых протоколов и сканограмм 263 пациентов из архива кафедры ультразвуковой диагностики БелМАПО за 2014 год, которым была выполнена ультразвуковая аортография, установлено, что дилатации и аневризмы различных отделов грудной и брюшной аорты диагностированы у 11,8 % пациентов (31 человек) со средним возрастом 72,5 лет; из них дилатации и аневризмы грудной аорты составили 9,1 % (24 пациента со средним возрастом 72 года), дилатации и аневризмы инфраренального отдела брюшной аорты — 2,7 % (7 пациентов со средним возрастом 74 года). Острый аортальный синдром с интрамуральной гематомой нисходящего грудного отдела аорты и расслоением брюшной аорты был диагностирован у 1 пациента (0,4 % от выполненных исследований аорты) (рис. 5). Атеросклероз является основным этиологическим фактором формирования окклюзий аорты, кроме того причинами возникновения стеноокклюзирующих поражений аорты и подвздошных артерий являются неспецифический аортоартериит, постэмболическая и посттравматическая закупорка, фибромышечная дисплазия. Окклюзия инфраренального отдела аорты атеросклеротического генеза была выявлена у одного пациента, что составило 0,4 % от количества архивированных наблюдений (рис. 6).
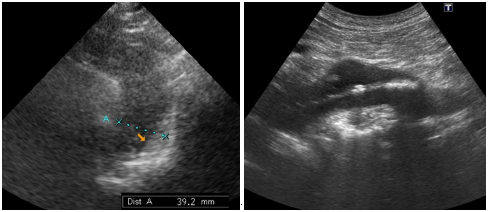
Рис. 5. Острая интрамуральная гематома толщиной 13 мм (стрелка) в дилатированном до 39 мм грудном нисходящем отделе аорты (супрастернальный доступ, левая сканограмма) и расслоение брюшной аорты (продольный скан: в просвете аорты определяется интимальный гиперэхогенный лоскут, делящий просвет аорты на истинный и ложный каналы) у пациента 73 лет с инфекционным эндокардитом. Пациент был переведен в РНПЦ «Кардиология» для хирургического лечения. Сканограммы 2014 года из архива кафедры ультразвуковой диагностики БелМАПО
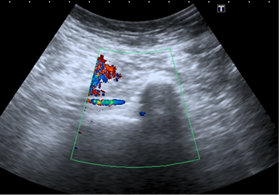
Рис. 6. Окклюзия инфраренального отдела аорты у мужчины 67 лет. В режиме цветового допплеровского картирования заполнение цветом просвета аорты отсутствует, что указывает на окклюзию. Визуализируется кальциноз стенки аорты с дистальной акустической тенью. Сканограмма 2014 года из архива кафедры ультразвуковой диагностики БелМАПО
Выводы:
1. Ультразвуковая диагностика является доступным, безопасным, достоверным методом диагностики заболеваний аорты различного генеза и их осложнений.
2. Базовым принципом ультразвуковой диагностики патологии артериальной сосудистой системы является сопоставление ультразвукового изображения с анатомическими характеристиками артерий:
Геометрия (соответствие хода сосуда анатомической траектории).
Проходимость сосуда с оценкой состояния просвета.
Оценка состояния сосудистой стенки.
Оценка состояния паравазальных тканей.
3. Средний возраст 76 пациентов кардиологического профиля, которым было произведено ультразвуковое исследование аорты, составил 58 лет. Атеросклеротическое поражение аорты было выявлено у 51 пациентов (67 %), дилатации различных отделов аорты — у 7 пациентов (9,2 %), аневризма восходящего отдела аорты — у 1 пациента (1,3 %). Согласно архивным данным за 2014 год дилатации и аневризмы различных отделов грудной и брюшной аорты диагностированы у 11,8 % пациентов кардиологического профиля, острый аортальный синдром — у 1 пациента (0,4 %), атеросклеротическая окклюзия инфраренального отдела аорты была выявлена у 1 пациента (0,4 %).
4. Ультразвуковое исследование, построенное на комплексном анализе анатомических характеристик стенок, просветов сосудов и окружающих тканей, ультразвуковых признаков различных аномалий, позволяет получить целостное представление о сосудах, характере патологического процесса, развивающегося в них, и направить пациента на консультацию и корректирующее лечение к кардиологу, кардиохирургу, ангиохирургу.
5. Ультразвуковое исследование аорты должно выполняться как скрининговое исследование пациентам старшей возрастной группы с учетом широкой распространенности атеросклероза, являющегося основным этиологическим фактором патологии аорты.
Литература:
1. 2014 ESC Guidelines on the diagnosis and treatment of aortic diseases. Document covering acute and chronic aortic diseases of the thoracic and abdominal aorta of the adult. The Task Force for the Diagnosis and Treatment of Aortic Diseases of the European Society of Cardiology (ESC) / R. Erbel [et al.] // Eur. Heart J. — 2014. — Vol. 35. — P. 2873–2926.
2. Global and regional burden of aortic dissection and aneurysms / U.K. A. Sampson [et al.] // Global Heart. — 2014. — Vol. 8. — P. 171–180.
3. Multimodality Imaging of Diseases of the Thoracic Aorta in Adults: From the American Society of Echocardiography and the European Association of Cardiovascular Imaging. Endorsed by the Society of Cardiovascular Computed Tomography and Society for Cardiovascular Magnetic Resonance / St.A. Goldstein [et al.] // J. Am. Soc. Echocardiogr. — 2015. — Vol. 28. — P. 119–182.
4. Aortic root dimensions and stiffness in healthy subjects / O. Vriz [et al.] // Am. J. Cardiol. — 2013. — Vol. 112. — P. 1224–1229.
5. CCF/AHA/AATS/ACR/ASA/SCA/SCAI/SIR/STS/SVM guidelines for the diagnosis and management of patients with Thoracic Aortic Disease: a report of the American College of Cardiology Foundation/ American Heart Association Task Force on Practice Guidelines, American Association for Thoracic Surgery, American College of Radiology, American Stroke Association, Society of Cardiovascular Anesthesiologists, Society for Cardiovascular Angiography and Interventions, Society of Interventional Radiology, Society of Thoracic Surgeons, and Society for Vascular Medicine / L. F. Hiratzka [et al.] // Circulation. — 2010. — Vol. 121. — E266–369.
6. Griggs, R. M. Noninvasive risk assessment for stroke: special emphasis on carotid atherosclerosis, sex-related differences, and the development of an effective screening strategy / R. M. Griggs, E. I. Bluth // Am. J. Roentgenol. — 2011. — Vol. 196. — P. 259–264.
7. Tedgui, A. Cytokines in Atherosclerosis: Pathogenic and Regulatory Pathways / A. Tedgui, Z. Mallat // Physiol. Rev. — 2006. — Vol. 86, № 2. — P. 515–581.
8. Virmani, R. Atherosclerotic plaque progression and vulnerability to rupture: angiogenesis as a source of intraplaque hemorrhage / R. Virmani, F. D. Kolodgie, A. P. Burke [et al.] // Arterioscler. Thromb. Vasc. Biol. — 2005. — Vol. 25. — P. 2054–2061.
9. Thim, T. From vulnerable plaque to atherothrombosis / T. Thim, M. K. Hagensen, J. F. Bentzon, E. Falk // J. Intern. Med. — 2008. — Vol. 263. — P. 506–516.
10. Otto, C. M. Textbook of clinical echocardiography / C. M. Otto. — Philadelphia: W. B. Saunders Elsevier. — 4th ed., 2009. — 519 c.
11. Echocardiography in aortic diseases: EAE recommendations for clinical practice / A. Evangelista [et al.] // Eur. J. Echocardiogr. — 2010. — Vol. 11. — P. 645–658.
12. Meredith, E. L. Echocardiography in the emergency assessment of acute aortic syndromes / E. L. Meredith, N. D. Masani // Eur. J. Echocardiogr. — 2009. — Vol. 10. — I31-I39.
13. Островский, Ю. П. Хирургия сердца / Ю. П. Островский. — М.: Мед. лит., 2007. — 576 с.
14. International Registry of Acute Aortic Dissection Investigators: Aortic diameter ˃ or = 5.5 cm is not a good predictor of type A aortic dissection: observation from the International Registry of Acute Aortic Dissection / L. A. Pape // Circulation. — 2007. — Vol. 116. — P. 1120–1127.







