Целью исследования явилось изучение диагностической эффективности специфической внутрикожной пробы с препаратом Диаскинтест® (ДСТ) в дифференциальной диагностики туберкулёзного плеврита. Для реализации поставленной задачи были определены показатели специфичности и чувствительности пробы Манту и Диаскинтеста®. Рассчитана предсказательная ценность положительного и отрицательного результатов для этих тестов и определена их диагностическая эффективность (точность). В результате исследования установлено, что использование препарата Диаскинтест® позволяет благодаря его высокой диагностической эффективности (87,5 %) ускорить процесс проведения дифференциальной диагностики плевральных выпотов и снизить частоту гипердиагностики случаев экссудативных плевритов туберкулёзной этиологии.
Ключевые слова: Диаскинтест®, проба Манту, туберкулёз, плеврит, плевральный выпот, синдром накопления жидкости в плевральной полости.
В настоящее время синдром плеврального выпота занимает существенную долю в общей структуре заболеваемости (3,8 %) и диагностируется примерно у 10 % больных пульмонологического профиля [12]. Данная патология характеризуется различным генезом и механизмами, что обусловливает признаваемые большинством российских и зарубежных авторов трудности дифференциальной диагностики рассматриваемого синдрома [3]. Между тем, решение данной проблемы крайне важно для выбора адекватной терапии. По информациии наиболее авторитетных пульмонологических центров, структура плевральных выпотов выглядит следующим образом: плеврит туберкулезного происхождения составляет 20–30 %, доля пара- и метапневмонических выпотов достигает 18–20 %, удельный вес кардиогенного гидроторакса — 30–40 %, а частота встречаемости выпотов другой этиологии соответствует 5–10 % [4].При этом отдельные авторы приводят аргументы в пользу того, что туберкулезный плеврит составляет не менее 50 % в структуре плевральных выпотов [9]. Ситуация осложняется тем, что клинические проявления туберкулезного плеврита аналогичны таковым при плевральных выпотах другой этиологии (вследствие злокачественных новообразований в легких или инфекционного процесса нетуберкулезной этиологии) [11], что определяет высокую значимость их этиологической диагностики, как важнейшей составной части дифференциальной диагностики синдрома плеврального выпота.
Верификация туберкулезного плеврита может достигаться обнаружением микобактерий туберкулеза (МБТ) при микроскопическом или культуральном микробиологическом исследовании плеврального экссудата или при морфологическом исследовании (обнаружение казеифицирующихся эпителиоидно-клеточных гранулем) биоптатов плевры. Однако, при наличии туберкулезных изменений в легких МБТ обнаруживаются в экссудате с помощью культурального исследования только в 10–35 % наблюдений [3], и для этого требуется достаточно длительное время (до 3 мес). Инфекционные гранулемы при гистологическом исследовании образцов определяются лишь в 56–82 % случаев (что предполагает использование высокотехнологичных инвазивных методов диагностики — торакоскопия или торакотомия с биопсией плевры) [10]. Кроме того, в процессе дифференциальной диагностики туберкулеза легких определенное значение имеет исследование методом полимеразной цепной реакции (ПЦР). Однако, исследование плеврального экссудата методом ПЦР значительно менее информативно, поскольку его чувствительность составляет только 17 % [17].
В значительной же части случаев диагностика туберкулезного плеврита основана только на клинических данных, что приводит к большому числу ошибок и длительным срокам диагностики, по данным некоторых исследователей частота ошибок достигает 30–40 % случаев [9].
Таким образом, очевидна актуальность своевременной диагностики и дифференциальной диагностики туберкулезного плеврита и в первую очередь с использованием методов быстрого определения этиологии выпота [12].
Одним из направлений оптимизации диагностики туберкулезной инфекции является использование антигенов, специфических для Mycobacterium tuberculosis [8, 14, 15, 18]. Антигены области различия 1 (RD1) были открыты Андерсоном в 1996 г. Расшифровка геномов разных видов микобактерий позволила выделить у Mycobacterium tuberculosis область RD1 (region of difference), которая отсутствует у Mycobacterium bovis и BCG-штаммов [12]. В этой области Mycobacterium tuberculosis кодирует синтез двух секреторных белков ESAT-6 (early secreted antigenic target) и CFP-10 (culture filtrate protein). На моделях зараженных туберкулезом животных установлено, что экспрессия белков ESAT-6 и CFP-10 связана именно с процессом размножения Mycobacterium tuberculosis. В 2004 году стали использовать тесты in vitro, основанные на определении γ-интерферона (IFN-γ), секретируемого Т-лимфоцитами инфицированного человека при контакте с ESAT-6 и CFP-10. Мета-анализ данных о применении тестов Quanti FERON-TB и T-SPOT.TB [13,16] показал, что у больных активным туберкулезом чувствительность данных тестов выше туберкулинового теста (проба Манту). Они гораздо реже давали положительные реакции у лиц неинфицированных и привитых BCG. Вместе с тем, основными их недостатками являются: значительная стоимость, потребность в оснащенной лаборатории, высокие требования к обработке крови с целью поддержания жизнеспособности клеток, а также внутривенные манипуляции при заборе крови. В связи с чем (недостаточная информативность традиционных методов исследования и трудоемкость в сочетании с высокой стоимостью тестов основанных на определении IFN-γ для этиологической диагностики экссудативного плеврита) в последнее время обсуждается диагностическая значимость некоторых специфических тестов, в том числе внутрикожной пробы с препаратом Диаскинтест® (ДСТ).
В Российской Федерации впервые в мировой практике на базе двух рекомбинантных белков ESAT-6/CFP-10 разработан препарат Диаскинтест®, предназначенный для постановки внутрикожной пробы. Техника постановки и учёта результатов данного теста (наличие и измерение папулы через 72 ч после реакции) идентичны пробе Манту, что делает использование удобным для медперсонала лечебных учреждений.
По информации разработчиков, ДСТ позволяет чётко дифференцировать иммунные реакции, обусловленные инфекцией M. tuberculosis, поствакцинальный иммунитет (БЦЖ) и неспецифические реакции [1, 6, 7].
Посредством постановки внутрикожной пробы с препататом ДСТ выявляется аллергическая реакция замедленного типа, которая развивается при туберкулезной инфекции параллельно с формированием иммунитета. Проба позволяет установить наличие инфекции даже в отсутствии клинических проявлений туберкулеза. К месту внутрикожного введения препарата направляются сенсибилизированные лимфоциты (CD4), вызывая местную специфическую реакцию в виде инфильтрата (формирование которого, при положительной ответной реакции на введение препарата, завершается через 2–3 суток), гиперемия вокруг инфильтрата не является отражением аллергической реакции замедленного типа.
Целью настоящего исследования является изучение чувствительности, специфичности и диагностической эффективности внутрикожной пробы с препаратом ДСТ для дифференциальной диагностики синдрома плеврального выпота.
Материалы и методы исследования
Всего обследовано 56 больных с синдромом плеврального выпота в возрасте от 18 до 86 лет. Из них 45мужчин и 11 женщин. Сроки с момента заболевания до поступления в стационар составили от 1 до 6 мес. Следует отметить, что 2/3 пациентов до этого находились на стационарном обследовании в других лечебных учреждениях.
Комплекс обследования включал традиционные методы. Диагностический процесс при синдроме накопления жидкости в плевральной полости строится по принципу — от установления факта наличия плеврального выпота (полипозиционное рентгенологическое обследование и ультразвуковое сканирование плевральной полости), через его характеристику (транссудат или экссудат), к выявлению этиологии этого выпота (компьютерная томография органов грудной клетки, исследование мокроты и плевральной жидкости методом люминесцентной микроскопии (определение кислотоустойчивых микобактерий (КУМ)) и методом культурального исследования для обнаружения МБТ, исследование плевральной жидкости на атипичные клетки и клеточный состав, фибробронхоскопию с браш-биопсией и щипцовой биопсией. В процессе лечения больных с диагностической целью были выполнены следующие оперативные вмешательства: видеоторакоскопия с биопсией плевры — у 3 пациентов; биопсия плевры при мини-торакотомии с видеоподдержкой — у 1 пациента.
При поступлении в стационар всем пациентам одновременно на обеих руках (внутренняя поверхность средней трети предплечий) были поставлены ДСТ и проба Манту (ПМ). Оценка результатов ДСТ и ПМ осуществлялась согласно инструкции по применению тестов в России [5].
Расчёт показателей производился по общепринятым формулам [2,11]: чувствительность: [a/(a + c)], специфичность: [d/(d + b)], предсказательная ценность положительного результата: [a/(a + b)], предсказательная ценность отрицательного результата: [d/(d + c)], диагностическая эффективность: [(a + d)/(a + b + d + c)], где a — положительный результат при наличии заболевания, b — ложноположительный т. е. положительный при отсутствии заболевания, c — ложноотрицательный, т. е. отрицательный при наличии заболевания, где d — отрицательный результат при отсутствии заболевания.
Результаты исследования и их обсуждение
При комплексном обследовании и клиническом наблюдении у 24 из 56 пациентов диагностирован экссудативный плеврит туберкулезной этиологии (1-я группа), у 32 пациентов установлена нетуберкулезная природа выпота в плевральную полость (2-я группа).
Во 2-ю группу (нетуберкулезная этиология плеврита) вошли 9 больных со злокачественными новообразованиями (при этом рак легкого был диагностирован у 7 человек, опухоли молочной железы и яичников у 2 пациенток), парапневмонический выпот был подтвержден у 14 больных. У 6 пациентов 2-й группы накопление жидкости в плевральной полости было связано с сердечной недостаточностью, у 2 с циррозом печени и в 1наблюдении плевральный выпот был обусловлен хронической почечной недостаточностью. При этом у одного пациента с выявленным раком легкого и у одного с парапневмоническим выпотом в легочной ткани определялись мета- и посттуберкулезные изменения не установленной активности.
В первой группе количество положительных проб ДСТ составило 91,67 %±5,64 %, отрицательных — 8,33 %±5,64 %, количество положительных ПМ — 95,83 %±4,08 %, отрицательных — 4,17 %±4,08 %.
Сравнительное изучение результатов двух кожных тестов у пациентов с туберкулёзным плевритом показало, что частота положительных реакций на пробу Манту была несколько выше, чем на Диаскинтест® 95,83 %±4,08 % и 91,67 %±5,64 % соответственно, однако достоверность этих различий доказать не удалось (p>0,05). Средний размер папулы среди пациентов с туберкулёзным плевритом положительно реагирующих на специфические кожные тесты составил при пробе Манту 14,86±0,64 мм, а при ДСТ 13,71±0,91 мм (рис. 1).
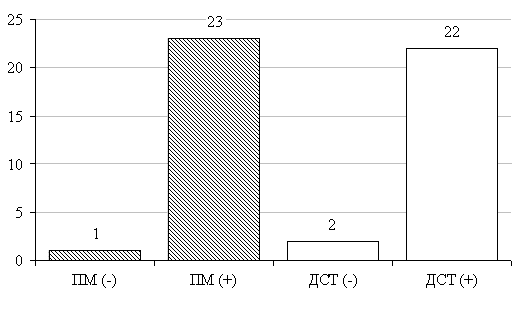
Рис. 1. Результаты реакций на пробу Манту (ПМ) и Диаскинтест (ДСТ) в 1 группе.
Примечание — ПМ (+) и ДСТ (+) — p>0,05, ПМ (-) и ДСТ (-) — p>0,05.
Количество гиперергических реакций при постановке пробы Манту было 4,41 % ± 2,49 % и 35,29 % ±5,8 % при ДСТ (рис. 2).
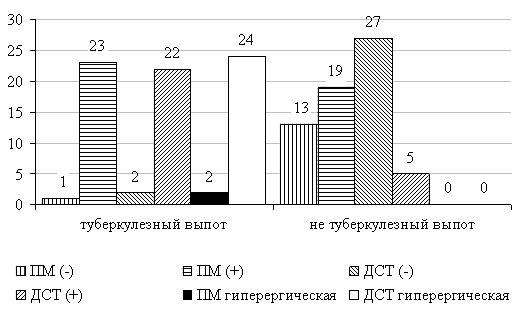
Рис. 2. Результаты реакций на пробу Манту (ПМ) и Диаскинтест (ДСТ) в 1 и 2 группах.
Примечание –ПМ гиперергичекая и ДСТ гиперергическая — p<0,05.
Сравнительное изучение результатов специфических кожных тестов у пациентов с нетуберкулезной этиологией плеврального выпота (рис. 3) показало (2 группа), что частота ложноположительных реакций на пробу Манту была значительно выше, чем на ДСТ (59,38 %±8,68 % и 8,33 %±5,64 % соответственно), различия достоверны (p<0,001).
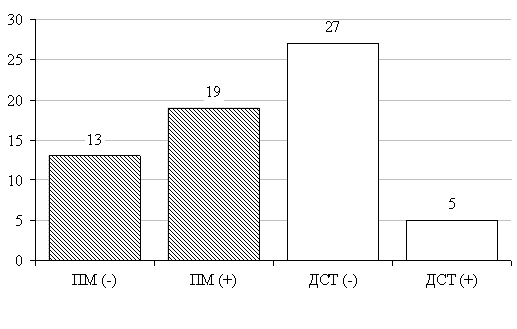
Рис. 3. Результаты реакций на пробу Манту (ПМ) и Диаскинтест (ДСТ) во 2 группе.
Примечание — ПМ (+) и ДСТ (+) — p<0,05, ПМ (-) и ДСТ (-) — p<0,05.
Расчёт показателей эффективности, в рамках настоящего исследования, произведён в соответствии с общепринятыми методиками [2, 11], результат которого приведён в таблице 1.
Таблица 1
Показатели эффективности применения ДСТ и пробы Манту (ПМ)
|
Показатели |
ПМ |
ДСТ |
|
Специфичность % |
40,63 |
84,38 |
|
Чувствительность % |
95,83 |
91,67 |
|
Предсказательная ценность положительного результата % |
54,76 |
81,49 |
|
Предсказательная ценность отрицательного результата % |
92,86 |
93,10 |
|
Диагностическая эффективность (точность) % |
64,43 |
87,50 |
Принимая во внимание полученные результаты, можно обоснованно утверждать, что ДСТ предоставляет более достоверные диагностические оценки по сравнению с ПМ. При этом, несмотря на то, что формально оба данных теста выполняются за равные промежутки времени, во многих практических случаях меньшая диагностическая достоверность ПМ влечёт за собой необходимость проведения дополнительных тестов и, как следствие, существенно увеличивает затраты временных ресурсов.
Выводы
Полученные данные свидетельствуют о том, что чувствительность проб Манту и ДСТ сравнима и достаточно высока, однако ДСТ обладает существенно более высокой специфичностью (ориентировочно в 2 раза).
Общая диагностическая эффективность ДСТ составила 87,5 %, что на 35 % лучше аналогичного показателя пробы Манту.
Являясь наиболее предпочтительной альтернативой кожным тестам, ДСТ обеспечивает снижение временных затрат, необходимых для достоверной диагностики туберкулезного плеврита.
Таким образом, использование препарата ДСТпозволит:
ускорить процесс проведения дифференциальной диагностики плевральных выпотов;
снизить частоту гипердиагностики случаев экссудативных плевритов туберкулёзной этиологии;
уменьшить количество госпитализаций непрофильных больных в противотуберкулезный стационар, число дней проведённых в стационаре и, соответственно, длительность временной нетрудоспособности.
Литература:
1. Аксёнова В. А., Леви Д. Т., Клевно Н. И.и др. Выявление туберкулёза и тактика диспансерного наблюдения за лицами из групп риска по заболеванию туберкулёзом с использованием препарата «ДИАСКИНТЕСТ ®» (аллерген туберкулёзный рекомбинантный) // Пробл. туб. — М. — 2010. — № 2. — С. 13–19
2. Внутренние болезни по Т. Р. Харрисону: в 7 т. / под ред. E. Braunwald [et al.]: Пер. с английского — М.: Практика, 2005. — Т 5.
3. Даренская С. Д., Макарова Н. В., Владимирский М. А.и др.. Значение определения интерферона-γ в диагностике туберкулезного экссудативного плеврита// Пробл. туб. — М. — 2008. — № 2. — С. 29–32
4. Добровольский С. Р., Белостоцкий А. В. Диагностика и лечение экссудативных плевритов // Хирургия. — 2002. — № 3. — С. 52–57
5. Инструкция по применению «ДИАСКИНТЕСТ». Аллерген туберкулёзный рекомбинантный в стандартном разведении, раствор для внутрикожного введения. Утверждена 19.06.2008 г., № 01–11/99–08.
6. Киселёв В. И., Барановский П. М., Пупышев С. А., Рудых И. В., Перельман М. И., Пальцев М. А. Новый кожный тест для диагностики туберкулёза на основе рекомбинантного белка ESAT-CFP // Молекулярная медицина. 2008. — № 4. — С. 4–6
7. Литвинов В. И., Слогоцкая Л. В., Сельцовский П. П. и др. Новый кожный тест для диагностики туберкулёзной инфекции // Рос. мед. журнал. — М. — № 1. — 2009. — C. 52–56
8. Рачина Н. В., Гольев С. С., Петрухина Л. Н., Абрамов А. В., Винников В. Г. Сравнительная оценка специфичности и чувствительности кожного теста «Диаскинтест» и пробы Манту // Туберкулез и болезни легких 2011 № 5. — с. 132–133
9. Стогова Н. А., Тюхтин Н. С. Особенности диагностики парапневмонического и туберкулезного экссудативного плеврита// Пульмонология — 2004. — № 5. — С. 51–54
10. Таганович А. Д., Алинежад Саид М. Диагностические характеристики аденозиндезаминазного теста у больных туберкулезным плевритом—жителей Белоруссии// Пробл. туб. — М. — 2008. — № 8. — С. 38–42
11. Флетчер Р., Флетчер С., Вагнер Э. Клиническая эпидемиология. Основы доказательной медицины. М.: Медиа Сфера, 1998. 352 с.
12. Шмелев Е.И Дифференциальная диагностика плевритов // Рус. Мед. Жур. -2004.-№ 3.- С. 94–99
13. Arend S. A., Franken W. P., Aggerbeck H. et al. Double-blind randomized Phase I study comparing rdESAT-6 to tuberculin as skin test reagent in the diagnosis of tuberculosis infection // Tuberculosis. — 2008. — Vol. 88. — P. 249–261.
14. Brosch, R., Gordon S. V., A. Billault, T. Gamier, K. Eiglmeier, C. Soravito, B. G. Barrel, and S. T. Cole. Use of Mycobacterium tuberculosis H37Rv bacterial artificial chromosome library for genome mapping, sequencing, and comparative genomics.// Infect. Immun.- 1998.- V. 66.- Р.2221–2229.
15. Harboe, M., T. Oettinger, H. G. Wiker, I. Rosenkrands, P. Andersen. Evidence for occurrence of the ESAT-6 protein in Mycobacterium tuberculosis and virulent Mycobacterium bovis and for its absence in Myco-bacteriuin bovis BCG.// Infect. Immun. -1996.- V. 64.- Р. 16–22.
16. Menzies D., Pai M., Comstock G. Meta-analysis: New Tests for the Diagnosis of Latent Tuberculosis Infection: Areas of Uncertainty and Recommendations for Research March // Annals of Internal. Medicine. — 2007. — Vol. 146, № 5. — P. 340–354.
17. Moon J. W., Chang Y. S., Kim S. К et al. The clinical utility of polymerase chain reaction for the diagnosis of pleural tuberculosis // Clin. Infect. Dis. — 2005. — Vol. 41, N 5. — P. 660 -665
18. Session 5. Applications of IGRAs. Int. J. Tuberc. Lung Dis. — 2010. — Vol. 14, supplemental, June, P. 42–47.







