Создание пористых материалов с заданными параметрами (пористостью, распределением пор по размерам, определенной геометрией пористой структуры, контролируемым фазовым составом и др.) является чрезвычайно востребованным и интенсивно развивающимся направлением современного материаловедения.
Пористый кремний (por-Si) обладает рядом свойств, делающих его перспективным материалом для применения в биологии и медицине [1–9]:
- биосовместимость;
- биодеградируемость;
- относительно простая технология получения;
- большие значения удельной площади поверхности;
- возможность управления геометрическими характеристиками пористой структуры (диаметр и геометрия каналов пор, распределение пор по размерам, пористость);
- многофункциональность. Отметим, что специфические оптические и электрические свойства por-Si позволяют использовать его в качестве сенсора для диагностики и лечения заболеваний, а также для лекарственного скрининга;
- пористые контейнеры могут быть использованы для загрузки как гидрофильных, так и гидрофобных молекул;
- кинетика высвобождения лекарств контролируется изменением физико-химических свойств контейнера. Изменяя свойства поверхности контейнера, можно осуществлять контролируемое высвобождение лекарства, продлевая срок эффективного его использования до недель и месяцев.
Можно выделить следующие направления и стратегии применения пористого кремния в медицине.
Лечение онкологических заболеваний [10–12]:
- в качестве сенсоров для обнаружения небольших по размеру опухолей;
- для визуализации не удаленных в процессе хирургической операции остатков опухолевой ткани;
- для брахитерапии, которая основана на локализованной доставке радиоактивного изотопа прямо к месту опухоли. Радиоактивно –устойчивый Si в данном случае является идеальным переносчиком изотопов, снижающим их негативное воздействие на здоровые клетки.
Ортопедия и тканевая инженерия [13–14]:
- переносит ростовые факторы, способствующие росту кости, и встраивается в костную ткань, обеспечивая быстрое ее восстановление;
- переносит стабилизаторы кости, анальгетики, антивоспалительные агенты (для снятия болевых ощущений после операции) и антибиотики.
Лечение диабета [15–16]:
- направленная доставка инсулина;
- векторное перемещение инсулино-подобных лигандов, в том числе и белков,
- имплантация биокапсул, содержащих островки Лангерганса.
Офтальмология:
В работе [17] описана успешная имплантация пористого Si, содержащего лекарство, в радужную оболочку глаза. В течение продолжительного периода времени исследователи наблюдали процесс уменьшения концентрации препарата в радужной оболочке, используя оптические свойства пористого Si. Кроме того, было показано, что имплантированный Si не проявлял какой-либо цитотоксичности в течение более 4 месяцев.
Размер пор, морфологию и химию поверхности можно менять в процессе получения por-Si и его последующей обработки, таким образом можно обеспечить требуемые сорбционные характеристики для конкретного лекарства [18–23] Поэтому важно исследовать взаимосвязь морфологии и состава поверхности пористого кремния в зависимости от технологических условий получения и обработки.
Целью данной работы являлось исследование взаимосвязи морфологии слоев и порошков на основе por-Si и технологических условий получения и хранения. Для этого были поставлены следующие задачи:
- исследовать влияние плотности тока анодирования на морфологию поверхности por-Si;
- исследовать особенности агрегации порошков на основе por-Si n- и p- типа проводимости в различных средах;
- исследовать процессы эволюции во времени порошков на основе por-Si p- типа проводимости в воде.
Получение слоев пористого кремния с разной плотностью тока анодирования
Основным методом получения por-Si является электрохимическое анодное растворение кремния (обычно монокристаллического). Важными достоинствами технологии электрохимического травления (ЭХТ) por-Si являются низкая температура получения образцов, дешевизна и совместимость формирования por-Si с технологическими процессами микроэлектроники. При получении por-Si методом ЭХТ, в зависимости от условий травления и характеристик исходного материала параметры образующегося пористого слоя могут меняться в широком диапазоне значений пористости, диаметров пор, типа пористой структуры и т. п. [24–27]. Массив пор может представлять собой в разной степени упорядоченную систему.
В настоящей работе получение слоев por-Si осуществлялось методом Унно-Имаи. Данная методика позволяет получать слои por-Si с наиболее однородным распределением параметров пористых слоев по площади травления. В методе Унно-Имаи повышение однородности параметров por-Si достигается за счет более однородного распределения электрического поля в образце, так как электрический контакт к катодной стороне кремниевой пластины осуществляется за счет контакта кремния с электролитом.
Электрохимическая обработка проводилась в электролите на основе водного раствора HF с добавлением изопропанола. В качестве подложек был использован кремний марки КЭФ-5 (111). Образцы были получены при плотностях тока анодирования 30 и 80 мА/см2, время травления одинаково.
Таблица 1
Условия получения слоев пористого кремния
|
Образец |
Ja, мА/см2 |
t, мин. |
|
I |
30 |
15 |
|
II |
80 |
15 |
Зависимость морфологии поверхности слоев пористого кремния от плотности тока анодирования
Исследование морфологии образцов por-Si I и II (рис. 1), технологические условия получения которых указаны в табл. 1, показало, что на поверхности присутствуют макропоры диаметром ≈ 200 нм для образца I, и ≈ 0,5–1 мкм для образца II, характеризующиеся треугольной формой (это связано с исходной кристаллографической ориентацией пластин — (111)).
В табл. 2 приведены результаты статистических данных по площади поверхности 10х10 мкм. Показано, что при более высокой плотности тока шероховатость поверхности пористого кремния меньше, так как при значении плотности тока анодирования равном 80 мА/см2 условия близки к условиям электрополировки.
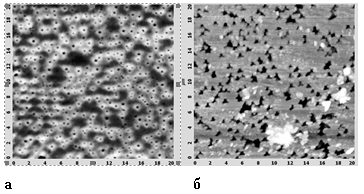
Рис. 1. Изображения атомно-силовой микроскопии образцов по площади сканирования 20х20 мкм: а — образец I; б — образец II
Таблица 2
Характеристики профилей поверхности
|
Серия |
I |
II |
|
Размер поля |
10х10 мкм |
10х10 мкм |
|
Размах высот, Sy, нм |
864 |
1468 |
|
Среднее значение высоты, нм |
478 |
954 |
|
Ср. арифметическая шероховатость, Sa, нм |
178 |
82 |
|
Ср. квадратичная шероховатость, Sq, нм |
206 |
141 |
Влияние многостадийного анодирования на морфологию поверхности слоев пористого кремния
Исследование влияния второго этапа анодирования показало следующее. После 1 этапа анодирования на поры двух типов: макропоры диаметром ≈ 500 нм и мезопоры диаметром порядка 20–40 нм (рис. 3, б).

Рис. 3. Пористый кремний, полученный в 1 этап анодирования: а, б — данные АСМ поверхности при размерах областей сканирования 50 х 50 мкм и 800 х 800 нм соответственно; в — данные ионно-электронной микроскопии среза слоя por-Si
Макропоры характеризуются треугольной формой, что очевидно обусловлено кристаллографической ориентацией подложки (111). При этом поры по глубине слоя характеризуются кристаллографической огранкой и диаметром сечения порядка ≈ 150 нм (рис. 3, в).
При проведении электрохимического анодного травления в два этапа (образец № 2) полученный материал характеризуется губчатой структурой, высокой пористостью, не типичной для макропористого кремния, специфическим и более развитым строением поверхности (рис. 4, а, б). В таблице 3 приведены данные статистических данных по площади поверхности 5х5 мкм, 10х10 мкм и 20х20 мкм.
Таблица 3
Характеристики профилей поверхности при электрохимическом анодировании, проведенном в 1 и в 2 этапа
|
Число этапов |
1 |
2 |
||||
|
Область сканирования, мкм |
5х5 |
10х10 |
20х20 |
5х5 |
10х10 |
20х20 |
|
Размах высот, Sy, нм |
100 |
105 |
312 |
697 |
1310 |
1407 |
|
Средняя высота, нм |
65 |
72,2 |
86,3 |
359 |
734 |
521 |
|
Ср. арифметическая шероховатость, Sa, нм |
5,7 |
6,3 |
6,9 |
80,1 |
163,8 |
115,3 |
|
Ср. квадратичная шероховатость, Sq, нм |
7,8 |
8,3 |
9,8 |
99,9 |
202,2 |
145,4 |
Диаметр отверстий пор на поверхности составил порядка 200–300 нм. Характер поверхности, диаметр пор и специфическое строение одинаковы по всей области травления. Очевидно, форма пор диктуется кристаллографической ориентацией подложки (111), направления лучей и стенок пор, по-видимому, принадлежат семейству <110>.

Рис. 4. Пористый кремний, полученный в 2 этапа анодирования: а, б — данные АСМ поверхности при размерах областей сканирования 50 х 50 мкм и 6 х 6 мкм соответственно; в — данные ионно-электронной микроскопии среза слоя por-Si
Исследование пористого слоя по толщине показало (рис. 4, в) показало, что por-Si обладает сложной системой пересекающихся пор, диаметр которых варьируется от мезо- до макропор: ≈ 50–400 нм.
Показано, что на втором этапе при j2<<j1 не происходит образование второго слоя, толщина слоя практически остается неизменной, происходит изменение пористой структуры слоя, сформированного на 1 этапе. По статистически данным приведенным в таблице 3 видно, что после проведения второго этапа увеличилась развитость (шероховатость) поверхности. В пористом кремнии такого типа можно ожидать качественное изменение свойств (механических, электрофизических, оптических свойств).
Выводы
В результате работы было показано, что изменяя плотность тока анодирования можно управлять рельефом поверхности, при этом при увеличении плотности тока увеличивается диаметр пор, но рельеф поверхности более плоский. По-видимому, это связано с тем, что при увеличении плотности тока анодирования условия травления близки к режиму электрополировки кремния. Выявлено, что проведение второго этапа электрохимического травления при меньшей плотности тока анодирования (j2<<j1) приводит к увеличению развитости поверхности. Это может быть удобно для регулировки скорости растворения ПК в физиологической среде. Обнаружено, что дисперсия порошков на основе ПК эволюционирует: в дисперсиях порошков пористого кремния происходит перераспределение частиц por-Si по объему раствора и агрегация. Вид агрегатов существенно зависит от типа проводимости исходного Si и состава дисперсионной среды. Для дисперсии порошка на основе пористого кремния р- типа в воде доказано, что агрегация в объеме раствора значительно меньше, чем на подложке, при ее присутствии в растворе в течение всего времени выдержки. С течением времени увеличивается размер и число агрегатов. Приведенные результаты исследований могут быть полезны при создании на основе пористого кремния контейнеров для направленной доставки лекарств и при выборе условий хранения контейнеров ПК с лекарствами. Работа выполнялась в рамках госзадания Минобрнауки РФ No 16.2112.2014/К.
Литература:
1. Ксенофонтова О. И., Васин А. В., Егоров В. В. и др. Пористый кремний и его применение в биологии и медицине // ЖТФ, 2014. Т. 84, вып. 1, с. 67–77.
2. Улин В. П., Улин Н. В., Солдатенков Ф. Ю. и др. Поверхность пористого кремния в процессах гидрофилизации и гидролитической деградации. Физика и техника полупроводников, 2014, том 48, вып. 9 с. 1243–1248
3. Porous silicon in drug delivery devices and materials / E. J. Anglin, L. С. Cheng, W. R. \47150
4. Freeman, and all// Adv Drug Deliv Rev. — 2008. — Vol. 60. — P.1–32.
5. Dong-JieGuo, Hao Zhang, Jia-Bo Li, etc., Fabrication and adhesion of a bio-inspired microarray: capillarity-induced casting using porous silicon mold // J. Mater. Chem. B, 2013,1, 379–386.
6. S. Dhanekar, S. Jain, J. M. Islamia, etc. Porous silicon biosensor: Current status // Biosensors and Bioelectronics, 2013. Vol 41.Pages 54–64.
7. M. Arroyo-Hernández,R. J. Martín-Palma, V. Torres-Costa,J. M. MartínezDuart. Porous silicon optical filters for biosensing applications // Journal of Non-Crystalline Solids, 2006. Vol.352,is. 23–25.Pages 2457–2460.
8. T. J. Barnes, Karyn L J., C. A. Prestidge. Recent advances in porous silicon technology for drug delivery // Therapeutic Delivery, 2013. Vol. 4, No. 7. PP. 811–823.
9. Spivak Yu. M., Maraeva E. V., Belorus A. O., Molchanova A. V., Nigmadzyanova N. R. Preparation and investigation of porous silicon nanoparticles for targeted drug delivery // Smart Nanocomposites, 2014. — v.4. № 1. p. 115–118
10. Белорус А. О. Применение пористого кремния в биомедицине // Молодой ученый. 2013. № 8. С. 69–74.
11. Arruebo M. // WIREs Nanomed. Nanobiotech. 2012. Vol. 4. P. 16–30.
12. Xiao L., Gu L., Howell S. B., Sailor M. J. // ACS Nano. 2011. Vol. 5. N 5. P. 3651–3659.
13. Vaccari L., Canton D., Zaffaroni N., Villa R., Tormen M., Fabrizio E. // Microelectron. Eng. 2006. Vol. 83. P. 1598– 1601.
14. Kumar D. S., Banji D., Madhavi B., Bodanapu V., Dondapati S., Sri A. P. // Int. J. Pharm. Pharm. Sci. 2009. Vol. 1. P. 8–16.
15. Colilla M., Izquierdo-Barba I., Vallet-Regi M. // Expert Opin. Ther. Pat. 2008. Vol. 18. N 6. P. 639–656.
16. Foraker A. B., Walczak R. J., Cohen M. H., Boiarski T. A., Grove C. F., Swaan P. W. // Pharmaceut. Res. 2003. Vol. 20. N 1. P. 110–116.
17. Ravaine V., Ancla C., Catargi B. // J. Control. Release. 2008. Vol. 132. P. 2–11.
18. Cheng L., Anglin E., Cunin F., Kim D., Sailor M. J., Falkenstein I., Tammewar A., Freeman W. R. // Br. J. Ophtalmol. 2008. Vol. 92. P. 705–71
19. Атомно-силовая микроскопия для исследования наноструктурированных материалов и приборных структур: Учеб.пособие. В. А. Мошников, Ю. М. Спивак, В. А. Алексеев, Н. В. Пермяков СПб.: Изд-во СПбГЭТУ «ЛЭТИ», 2014
20. Канагеева Ю. М., Савенко А. Ю., Лучинин В. В., Мошников В. А., Зимин С. П., Бучин Э. Ю. Изучение структурно-морфологических особенностей макропористого кремния при препарировании образцов остросфокусированным ионным пучком. Петербургский журнал электроники. 2007. № 1. С. 30–34.
21. Babayan V., Kazantseva N. E., Moučka R., Sapurina I., Spivak Yu.M., Moshnikov V. A. Сombined effect of demagnetizing field and induced magnetic anisotropy on the magnetic properties of manganesezinc ferrite composites. Journal of Magnetism and Magnetic Materials. 2012. Т. 324. № 2. С. 161–172.
22. Травкин П. Г., Воронцова Н. В., Высоцкий С. А., Леньшин А. С., Спивак Ю. М., Мошников В. А. Исследование закономерностей формирования структуры пористого кремния при многостадийных режимах электрохимического травления. Известия СПбГЭТУ «ЛЭТИ». 2011. № 4. С. 3–9.
23. Леньшин А. С., Кашкаров В. М., Середин П. В., Спивак Ю. М., Мошников В. А. Исследование электронного строения и химического состава пористого кремния, полученного на подложках n- и p-типа, методами xanes и ик спектроскопии. Физика и техника полупроводников. 2011. Т. 45. № 9. С. 1229–1234.
24. Спивак Ю. М., Муратова С. Е. Н., Петенко О. С., Травкин П. Г. Определение параметров пористой структуры в por-si и por-al2o3 путем компьютерной обработки данных растровой и атомно-силовой микроскопии. Молодой ученый. 2012. № 5. с. 1–4.
25. Мошников В. А., Спивак Ю. М. «Электрохимические методы получения пористых материалов для топливных элементов» // Глава в монографии: Основы водородной энергетики / Под ред. В. А. Мошникова и Е. И. Терукова. 2-е изд. СПб.: Изд-во СПбГЭТУ «ЛЭТИ», 2011. 288с.
26. Афанасьев А. В., Ильин В. А., Мошников В. А., Соколова Е. Н., Спивак Ю. М. Синтез нано- и микропористых структур электрохимическими методами. Биотехносфера. 2011. № 1–2. С. 39–45.
27. Спивак Ю. М. Наноструктурированные материалы. Особенности получения и диагностики // Известия высших учебных заведений России. Радиоэлектроника. 2013. Т. 6. С. 54–64.
28. Травкин П. Г., Соколова Е. Н., Спивак Ю. М., Мошников В. А. Электрохимическая ячейка для получения пористых анодных оксидов металлов и полупроводников. Патент на полезную модель RUS 122385 01.06.2012







